解题方法
1 . 某科研团队以溴苯与catB—Br的偶联联反应构建C-B键,反应机理如图,下列说法正确的是

| A.过程中Ni的化合价未发生改变 |
| B.L-Ni-Br为中间产物 |
| C.catB·为催化剂 |
D.理论上产生1mol  消耗Zn与溴苯的物质的量之比为1∶1 消耗Zn与溴苯的物质的量之比为1∶1 |
您最近半年使用:0次
解题方法
2 . 已知化合物 与
与  在一定条件下反应生成化合物
在一定条件下反应生成化合物 与
与 ,其反应历程如图所示,其中
,其反应历程如图所示,其中 表示过渡态,
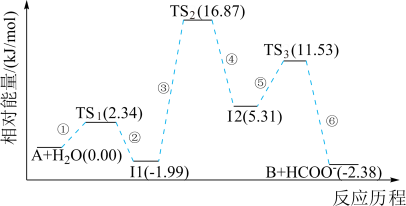
表示过渡态, 表示中间体。下列说法中正确的是
表示中间体。下列说法中正确的是
 与
与  在一定条件下反应生成化合物
在一定条件下反应生成化合物 与
与 ,其反应历程如图所示,其中
,其反应历程如图所示,其中 表示过渡态,
表示过渡态, 表示中间体。下列说法中正确的是
表示中间体。下列说法中正确的是
| A.由图可知反应历程中有三个基元反应 |
B.该历程中的最大能垒(活化能)  |
| C.使用更高效的催化剂可降低反应所需的活化能和反应热 |
| D.升高温度,有利于该反应正向进行 |
您最近半年使用:0次
名校
解题方法
3 . 苯与 的催化反应历程如图所示,关于该反应历程,下列说法正确的是
的催化反应历程如图所示,关于该反应历程,下列说法正确的是
 的催化反应历程如图所示,关于该反应历程,下列说法正确的是
的催化反应历程如图所示,关于该反应历程,下列说法正确的是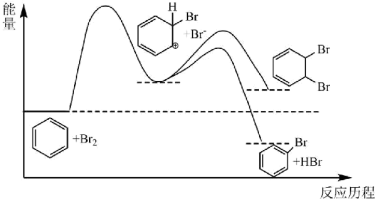
A.苯与 的催化反应一定为放热反应 的催化反应一定为放热反应 |
| B.使用催化剂可以降低该反应的活化能 |
C.该历程中,苯与 的催化反应可生成溴苯、邻二溴苯 的催化反应可生成溴苯、邻二溴苯 |
D.苯与 的催化反应主反应为取代反应,是因为从中间产物生成溴苯的反应速率较快 的催化反应主反应为取代反应,是因为从中间产物生成溴苯的反应速率较快 |
您最近半年使用:0次
名校
解题方法
4 . 某同学对甲苯与高锰酸钾水溶液反应速率做了如下两个探究实验:
实验Ⅰ: 取一定量的甲苯与一定体积,一定浓度的高锰酸钾水溶液混合,振荡 缓慢褪色。
缓慢褪色。
实验Ⅱ: 在实验Ⅰ的试剂取量基础上,再加入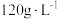 的冠醚(18—冠—6),振荡,
的冠醚(18—冠—6),振荡,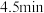 褪色。
褪色。
实验Ⅰ: 取一定量的甲苯与一定体积,一定浓度的高锰酸钾水溶液混合,振荡
 缓慢褪色。
缓慢褪色。实验Ⅱ: 在实验Ⅰ的试剂取量基础上,再加入
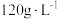 的冠醚(18—冠—6),振荡,
的冠醚(18—冠—6),振荡,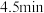 褪色。
褪色。
| A.冠醚是该反应的催化剂 |
B. 与冠醚形成的超分子可溶于甲苯 与冠醚形成的超分子可溶于甲苯 |
C.冠醚与 之间以弱配位键作用实现对 之间以弱配位键作用实现对 的识别 的识别 |
D.实验Ⅰ反应速率小的原因是高锰酸钾不溶于甲苯,氧化剂 与还原剂甲苯接触不充分 与还原剂甲苯接触不充分 |
您最近半年使用:0次
名校
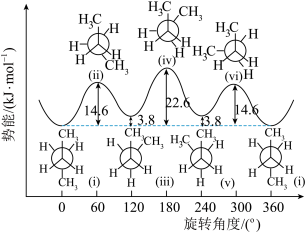
5 . 由单键旋转而产生的异构体称为构象异构体,将正丁烷分子中的 和
和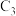 旋转不同的角度可以得到正丁烷的构象势能关系图。下列说法正确的是
旋转不同的角度可以得到正丁烷的构象势能关系图。下列说法正确的是
 和
和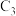 旋转不同的角度可以得到正丁烷的构象势能关系图。下列说法正确的是
旋转不同的角度可以得到正丁烷的构象势能关系图。下列说法正确的是
| A.正丁烷的构象异构体中占比最大的是iv |
| B.原子或基团之间的排斥作用决定了构象异构体的稳定性 |
| C.相同条件下,i转化成iii的速率比逆向转化慢 |
| D.构象异构体间的转化存在化学键的断裂和生成 |
您最近半年使用:0次
2024·安徽安庆·二模
解题方法
6 . 中科大某课题组通过自由基杂环反应直接合成各种 稠合的内酰胺,应用于钙钛矿电池器件中。底物与Cu(Ⅰ)物种通过电子转移经历两种途径得到目标产物D。下列说法错误的是
稠合的内酰胺,应用于钙钛矿电池器件中。底物与Cu(Ⅰ)物种通过电子转移经历两种途径得到目标产物D。下列说法错误的是
 稠合的内酰胺,应用于钙钛矿电池器件中。底物与Cu(Ⅰ)物种通过电子转移经历两种途径得到目标产物D。下列说法错误的是
稠合的内酰胺,应用于钙钛矿电池器件中。底物与Cu(Ⅰ)物种通过电子转移经历两种途径得到目标产物D。下列说法错误的是
| A.Cu(Ⅰ)物种是催化剂 | B.底物具有氧化性 |
| C.两种途径不同,总反应的反应热也不同 | D.合成过程中 中碳碳双键断裂 中碳碳双键断裂 |
您最近半年使用:0次
名校
解题方法
7 . 中国科学院理化所发现利用Pd-CdS可使PLA(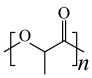 )转化为丙酮酸(
)转化为丙酮酸(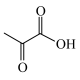 )的速率显著提高,并且优异的稳定性确保了Pd—CdS可以维持100h的反应性能,其反应机理如图所示,Pd-CdS在光照条件下产生带正电空穴(用h+表示,可捕获电子)和电子。下列说法错误的是
)的速率显著提高,并且优异的稳定性确保了Pd—CdS可以维持100h的反应性能,其反应机理如图所示,Pd-CdS在光照条件下产生带正电空穴(用h+表示,可捕获电子)和电子。下列说法错误的是
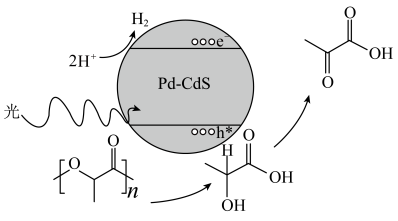
| A.Pd-CdS可作乳酸制备丙酮酸的催化剂 |
| B.在相同条件下,适当增加光的强度有利于加快反应速率 |
| C.整个过程中,氧化产物与还原产物的物质的量之比为1:1 |
| D.当180gPLA完全转化成丙酮酸时,理论上Pd-CdS中至少产生4molh+ |
您最近半年使用:0次
2024-03-27更新
|
548次组卷
|
2卷引用:山东省济南市2023-2024学年高三下学期3月模拟(一模)考试化学试题
解题方法
8 . 下列实验操作及现象、得出的结论及解释,均正确的是
选项 | 实验操作及现象 | 结论及解释 |
A | 常温下,用胶头滴管将待测NaClO溶液滴在pH试纸上,与标准比色卡对照, | NaClO溶液显碱性 |
B | 在KSCN与 的混合液中再加入少量KCl固体,溶液颜色加深 的混合液中再加入少量KCl固体,溶液颜色加深 | 增大 浓度,平衡正向移动 浓度,平衡正向移动 |
C | 在相同条件下,向一支试管中加入2 mL 5% 溶液,向另一支试管中加入2 mL 5% 溶液,向另一支试管中加入2 mL 5% 溶液和1 mL 溶液和1 mL 溶液,可观察到后者产生气泡速率更快 溶液,可观察到后者产生气泡速率更快 |  可加快 可加快 分解速率 分解速率 |
D | 在室温下,用pH计分别测定 的 的 溶液、 溶液、 的 的 溶液的pH,前者大于后者 溶液的pH,前者大于后者 | 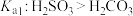 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-03-26更新
|
31次组卷
|
2卷引用:山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题
解题方法
9 . 二氧化碳加氢制甲烷过程中的主要反应为
Ⅰ.CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H1<0
Ⅱ.CO2(g)+H2(g)=CO(g)+H2O(g) △H2>0
Ⅲ.2CO(g)+2H2(g)=CO2(g)+CH4(g) △H3
在密闭容器中,1.01×105Pa、n起始(CO2):n起始(H2)=1:4时,在催化剂作用下反应相同时间所测得的CO2平衡转化率、CO2实际转化率随温度的变化如图2所示。CH4的选择性可表示为 ×100%。
×100%。
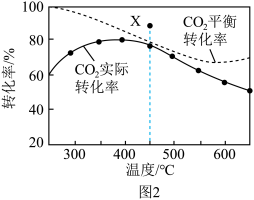
(1)各物质的相对能量如图1所示,△H3=______ kJ•mol-1,平衡时CH4的选择性随着温度的升高______ ,用该催化剂催化二氧化碳反应的最佳温度为______ ,450℃时,使CO2平衡转化率达到X点的值,可以采用的措施为_______ (写出一条)。
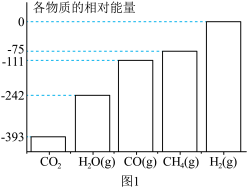
(2)在密闭容器中,1.01×105Pa,CO2和H2的起始物质的量分别为1mol和4mol,平衡后反应体系中各物质的物质的量随温度的变化如图3所示,图中表示CH4的物质的量的曲线为______ 。在505℃,反应Ⅱ的平衡常数K=______ 。(保留两位有效数字)
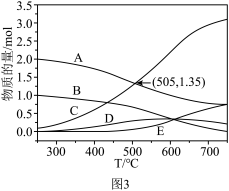
(3)CeO2催化CO2与H2转化为CH4的机理如图4所示。反应体系中Ce呈现______ 种价态,催化剂中掺入少量CaO,用Ca2+替代CeO2结构中部分Ce4+形成CaxCe1-xOy,可提高催化效率的原因是_______ 。

Ⅰ.CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H1<0
Ⅱ.CO2(g)+H2(g)=CO(g)+H2O(g) △H2>0
Ⅲ.2CO(g)+2H2(g)=CO2(g)+CH4(g) △H3
在密闭容器中,1.01×105Pa、n起始(CO2):n起始(H2)=1:4时,在催化剂作用下反应相同时间所测得的CO2平衡转化率、CO2实际转化率随温度的变化如图2所示。CH4的选择性可表示为
 ×100%。
×100%。
(1)各物质的相对能量如图1所示,△H3=

(2)在密闭容器中,1.01×105Pa,CO2和H2的起始物质的量分别为1mol和4mol,平衡后反应体系中各物质的物质的量随温度的变化如图3所示,图中表示CH4的物质的量的曲线为

(3)CeO2催化CO2与H2转化为CH4的机理如图4所示。反应体系中Ce呈现

您最近半年使用:0次
10 . 18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为如下所示:
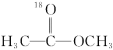 +OH-
+OH-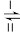
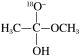
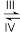
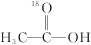 +CH3O-
+CH3O-
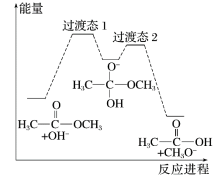
已知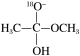

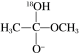 为快速平衡,下列说法正确的是
为快速平衡,下列说法正确的是
| A.反应Ⅱ、Ⅲ为决速步 |
| B.反应结束后,溶液中存在18OH- |
| C.反应结束后,溶液中存在CH318OH |
| D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变 |
您最近半年使用:0次



