解题方法
1 . 丙烯是重要的化工原料,丙烷直接脱氢制丙烯的相关反应及能量变化如图。
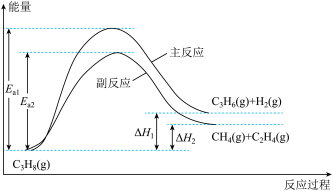
回答下列问题:
(1)主反应的焓变
______ 0(填“>”或“<”);在600℃、1MPa条件下,丙烷脱氢制丙烯反应到达平衡,测得 、
、 的体积分数均为30%,则此时
的体积分数均为30%,则此时 的体积分数为
的体积分数为____________ 。
(2)向密闭容器中充入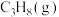 ,发生主反应:
,发生主反应: (忽略副反应的发生)。
(忽略副反应的发生)。
①测得反应速率方程为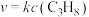 ,k为反应速率常数。已知:
,k为反应速率常数。已知: (R、C为常数,T为温度,Ea为活化能)。实验测得其他条件相同,不同催化剂Cat1、Cat2对k的影响如图甲所示,则催化效能较高的是
(R、C为常数,T为温度,Ea为活化能)。实验测得其他条件相同,不同催化剂Cat1、Cat2对k的影响如图甲所示,则催化效能较高的是______ (填“Catl”或“Cat2”)。
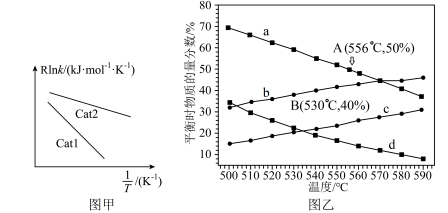
②在100 kPa、10 kPa不同起始压强下达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图乙所示。起始压强为10 kPa,丙烷、丙烯随温度变化的物质的量分数曲线分别是______ 、______ (填代号);A点对应的平衡常数
______ kPa( 为以分压表示的平衡常数);B点丙烷的平衡转化率为
为以分压表示的平衡常数);B点丙烷的平衡转化率为______ 。

回答下列问题:
(1)主反应的焓变

 、
、 的体积分数均为30%,则此时
的体积分数均为30%,则此时 的体积分数为
的体积分数为(2)向密闭容器中充入
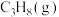 ,发生主反应:
,发生主反应: (忽略副反应的发生)。
(忽略副反应的发生)。①测得反应速率方程为
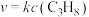 ,k为反应速率常数。已知:
,k为反应速率常数。已知: (R、C为常数,T为温度,Ea为活化能)。实验测得其他条件相同,不同催化剂Cat1、Cat2对k的影响如图甲所示,则催化效能较高的是
(R、C为常数,T为温度,Ea为活化能)。实验测得其他条件相同,不同催化剂Cat1、Cat2对k的影响如图甲所示,则催化效能较高的是
②在100 kPa、10 kPa不同起始压强下达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图乙所示。起始压强为10 kPa,丙烷、丙烯随温度变化的物质的量分数曲线分别是

 为以分压表示的平衡常数);B点丙烷的平衡转化率为
为以分压表示的平衡常数);B点丙烷的平衡转化率为
您最近一年使用:0次
名校
解题方法
2 . 某密闭容器中充入等物质的量的A和B,一定温度下发生反应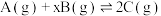 ,达到平衡后,在不同的时间段内反应物的浓度随时间的变化如甲图所示,正逆反应速率随时间的变化如乙图所示。下列说法错误的是
,达到平衡后,在不同的时间段内反应物的浓度随时间的变化如甲图所示,正逆反应速率随时间的变化如乙图所示。下列说法错误的是
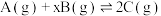 ,达到平衡后,在不同的时间段内反应物的浓度随时间的变化如甲图所示,正逆反应速率随时间的变化如乙图所示。下列说法错误的是
,达到平衡后,在不同的时间段内反应物的浓度随时间的变化如甲图所示,正逆反应速率随时间的变化如乙图所示。下列说法错误的是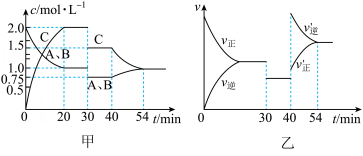
A.前20minB的平均反应速率为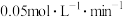 |
| B.30~40min间该反应使用了催化剂 |
C.化学方程式中的 ,正反应为放热反应 ,正反应为放热反应 |
| D.30min、40min时分别改变的条件是减小压强、升高温度 |
您最近一年使用:0次
2022-12-08更新
|
734次组卷
|
5卷引用:山东省烟台市2023届高三上学期期中学业水平诊断化学试卷
山东省烟台市2023届高三上学期期中学业水平诊断化学试卷山东省德州市第一中学2022-2023学年高二上学期期末线上考试化学试题山东省济宁市泗水县2023-2024学年高二上学期期中考试化学试题(已下线)题型18 化学反应原理综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)通关练08 聚焦反应热、速率及化学平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
解题方法
3 . 某温度下,向10mL0.40mol•L-1H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算标况)如表所示。
资料显示,反应分两步进行:
①2Fe3++H2O2=2Fe2++O2↑+2H+
②H2O2+2Fe2++2H+=2H2O+2Fe3+
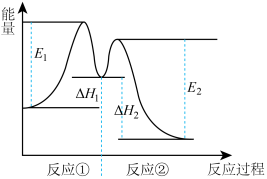
反应过程中能量变化如图所示:
下列说法不正确的是
| t/min | 0 | 2 | 4 | 6 |
| V(O2)/mL | 0 | 9.9 | 17.2 | 22.4 |
①2Fe3++H2O2=2Fe2++O2↑+2H+
②H2O2+2Fe2++2H+=2H2O+2Fe3+
反应过程中能量变化如图所示:

下列说法不正确的是
| A.Fe3+的作用是增大过氧化氢的分解速率 |
| B.0~6min的平均反应速率;v(H2O2)=3.33×10-2mol•L-1•min-1 |
| C.反应2H2O2(aq)=2H2O(l)+O2(g)的△H=E1-E2<0 |
| D.反应①是吸热反应、反应②是放热反应 |
您最近一年使用:0次
2022-11-16更新
|
427次组卷
|
32卷引用:山东省莱州一中2022-2023学年高二上学期第一次月考化学试题
山东省莱州一中2022-2023学年高二上学期第一次月考化学试题北京市海淀区2018届高三上学期期中考试化学试题山东省师范大学附属中学2018届高三第三次模拟考试化学试题山东师范大学附属中学2018届高三上学期第三次模拟考试化学试题四川省德阳市三校2018届高三联合测试化学试题河北省故城县高级中学2018届高三12月月考化学试题(已下线)2017-2018学年上学期期末复习备考之精准复习模拟题高二化学选修4(C卷)江西省莲塘一中、临川二中2018届高三上学期第一次联考化学试题(已下线)黄金30题系列 高三化学 小题易丢分(已下线)黄金30题系列 高二化学(选修4) 小题好拿分【提升版】山东省枣庄市第八中学东校区2018届高三1月月考理科综合化学试题四川省攀枝花市2017-2018学年高二上学期调研检测化学试题【全国百强校】福建省泉州第五中学2017届高三上学期期中检测化学试题【全国百强校】北京市北京四中2019届高三上学期期中考试化学试题安徽省六安市第一中学2020届高三下学期自测卷(一)陕西省汉中市五校2020-2021学年高二上学期第一次月考化学试题山东省济南市济北中学2021届高三11月月考化学试题江西省南昌市第二中学2020-2021学年高二上学期第三次月考化学试题广东省梅州市2020-2021学年度高二上学期期末联考化学试题江西省抚州市黎川县第一中学2020-2021学年高二上学期第三次月考化学试题江西省宜春市奉新县第一中学2020-2021学年高二下学期第一次月考化学试题江苏省徐州市邳州市运河中学2020-2021学年高一下学期期中考试(普通班)化学试题选择性必修1 专题2 第一单元综合训练(已下线)第18讲 化学反应速率(练) — 2022年高考化学一轮复习讲练测(新教材新高考)北京市中国农业大学附属中学2021-2022学年高三上学期开学考试化学试题河南省重点高中2021-2022学年高二下学期阶段性调研联考一化学试题浙江省嘉兴市2021-2022学年高二下学期期末检测化学试题天津市部分区2022-2023学年高三上学期期中考试化学试题 天津市武清区2022-2023学年高三上学期11月期中化学试题黑龙江省鹤岗市第一中学2023-2024学年高二上学期开学考试化学试题(已下线)第1讲 化学反应速率及其影响因素北京市中国人民大学附属中学2021-2022学年高一下学期期末考试化学试题
名校
4 . 某小组研究催化剂a、b对反应2M→N的影响。在相同条件下,测得各物质浓度c随反应时间t的部分变化曲线如图。下列说法错误的是


| A.使用催化剂无法改变化学反应的方向 |
| B.催化剂a的催化效率比催化剂b更高 |
| C.曲线l表示无催化剂时M的浓度随t的变化 |
| D.若反应达到平衡,无催化剂时生成物N的产率最低 |
您最近一年使用:0次
2022-11-10更新
|
217次组卷
|
3卷引用:山东省烟台市2022-2023学年高二上学期期中考试化学试题
5 . 反应Ⅰ、Ⅱ、Ⅲ均会在工业生产硝酸过程中发生,其中反应Ⅰ、Ⅱ发生在氧化炉中,反应Ⅲ发生在氧化塔中,不同温度下各反应的化学平衡常数如下表所示。下列说法正确的是
| 温度/K | 化学平衡常数 | |||
| 反应Ⅰ:4NH3+5O2=4NO+6H2O | 反应Ⅱ:4NH3+3O2=2N2+6H2O | 反应Ⅲ:2NO+O2=2NO2 | ||
| 500 | 1.1×1026 | 7.1×1034 | 1.3×102 | |
| 700 | 2.1×1019 | 2.6×1025 | 1.0 | |
| A.使用选择性催化反应Ⅰ的催化剂不能增大氧化炉中NO的含量 |
| B.通过改变氧化炉的温度可促进反应Ⅰ而抑制反应Ⅱ |
| C.通过改变氧化炉的压强可促进反应Ⅰ而抑制反应Ⅱ |
| D.氧化炉出气在进入氧化塔前应进一步降低温度 |
您最近一年使用:0次
2022-10-11更新
|
114次组卷
|
2卷引用:山东省莱州一中2022-2023学年高二上学期第一次月考化学试题
名校
6 . 在一定的温度和压强下,将按一定比例混合的 和
和 通过装有催化剂的反应器可得到甲烷。已知:
通过装有催化剂的反应器可得到甲烷。已知:
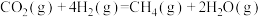
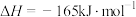


催化剂的选择是 甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测得温度对
甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测得温度对 转化率和生成
转化率和生成 选择性的影响如图所示。
选择性的影响如图所示。 选择性=
选择性=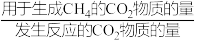 ×100%
×100%
下列有关说法正确的是
 和
和 通过装有催化剂的反应器可得到甲烷。已知:
通过装有催化剂的反应器可得到甲烷。已知: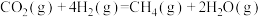
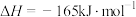


催化剂的选择是
 甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测得温度对
甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测得温度对 转化率和生成
转化率和生成 选择性的影响如图所示。
选择性的影响如图所示。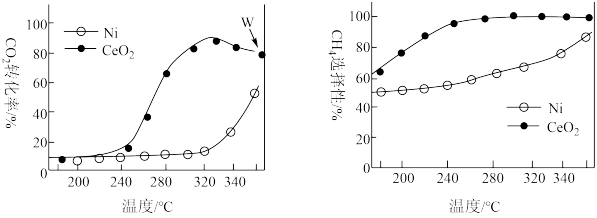
 选择性=
选择性=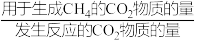 ×100%
×100%下列有关说法正确的是
A.在260℃~320℃间,以 为催化剂,升高温度 为催化剂,升高温度 的产率增大 的产率增大 |
B.延长W点的反应时间,一定能提高 的转化率 的转化率 |
C.选择合适的催化剂,有利于提高 的平衡转化率 的平衡转化率 |
D.高于320℃后,以Ni为催化剂,随温度的升高 转化率上升的原因是平衡正向移动 转化率上升的原因是平衡正向移动 |
您最近一年使用:0次
2022-08-28更新
|
1277次组卷
|
19卷引用:山东省莱州一中2022-2023学年高二上学期第一次月考化学试题
山东省莱州一中2022-2023学年高二上学期第一次月考化学试题江苏省百校大联考2021-2022学年高三上学期第二次考试化学试题(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)押新高考卷09题 速率和平衡-备战2022年高考化学临考题号押题(新高考通版)(已下线)回归教材重难点07 图像数据和结果的分析-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点07 图像数据和结果的分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)江苏省镇江市2022-2023学年高三上学期开学考试化学试题(已下线)2022年北京高考真题变式题1-14(已下线)化学(江苏A卷)-学易金卷:2023年高考第一次模拟考试卷河北省邯郸市第一中学2022-2023学年高三上学期一轮复习收官考试(二)化学试题(已下线)江苏省2022年普通高中学业水平选择性考试变式题(选择题11-13)江苏省南京市第二十九中学2022-2023学年高二下学期3月月考化学试题(已下线)2022年北京高考真题化学试题变式题(选择题11-14)江苏省扬州中学2023届高三下学期模拟预测化学试题河北省保定市2022-2023学年高三上学期12月月考化学试题(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点2 化学平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)江苏省兴化中学2023-2024学年高三上学期阶段性测试(三)化学试题江苏省常州市第一中学2023-2024学年高二下学期4月期中考试化学试题
解题方法
7 . 以软锰矿(含 和少量
和少量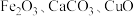 )和辉铜矿(含
)和辉铜矿(含 和少量
和少量 、
、 )为原料生产高纯
)为原料生产高纯 和
和 的工艺流程如下:
的工艺流程如下:
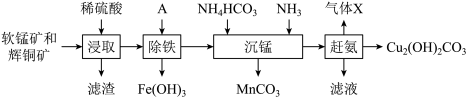
已知有关金属离子形成氢氧化物沉淀的pH范围如下:
(1)“浸取”所得滤渣经 提取后可获得一种淡黄色副产品,则滤渣的主要成分是
提取后可获得一种淡黄色副产品,则滤渣的主要成分是_______ (填化学式)。浸取时,发生主要反应的离子方程式为_______ 。
(2)试剂A最好选用_______ (填序号),其调节溶液pH的范围是_______ 。
A.氨水 B.CuO C.NaOH
(3)上述流程中可循环利用的物质是_______ 。除铁后检验溶液中是否含有 的试剂名称是
的试剂名称是_______ ;研究发现,若软锰矿和辉铜矿中不含 ,浸取速率明显变慢,浸取速率明显变慢的可能原因除了
,浸取速率明显变慢,浸取速率明显变慢的可能原因除了 有氧化性外,还可能是
有氧化性外,还可能是_______ 。
(4)“沉锰”所得溶液中铜元素主要以 形式存在,则生成
形式存在,则生成 的离子方程式是
的离子方程式是_______ 。
 和少量
和少量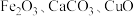 )和辉铜矿(含
)和辉铜矿(含 和少量
和少量 、
、 )为原料生产高纯
)为原料生产高纯 和
和 的工艺流程如下:
的工艺流程如下:
已知有关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 |  |  |  |  |
| 开始沉淀的pH | 7.5 | 2.7 | 5.6 | 8.3 |
| 沉淀完全的pH | 9.0 | 3.7 | 6.7 | 9.8 |
 提取后可获得一种淡黄色副产品,则滤渣的主要成分是
提取后可获得一种淡黄色副产品,则滤渣的主要成分是(2)试剂A最好选用
A.氨水 B.CuO C.NaOH
(3)上述流程中可循环利用的物质是
 的试剂名称是
的试剂名称是 ,浸取速率明显变慢,浸取速率明显变慢的可能原因除了
,浸取速率明显变慢,浸取速率明显变慢的可能原因除了 有氧化性外,还可能是
有氧化性外,还可能是(4)“沉锰”所得溶液中铜元素主要以
 形式存在,则生成
形式存在,则生成 的离子方程式是
的离子方程式是
您最近一年使用:0次
名校
解题方法
8 . 以H2O2和HCl为原料制备高纯度次氯酸的机理如图,V为元素钒,其最高化合价为+5, N(His404)、N(His496)为氨基酸,下列说法错误的是


| A.该机理中化合物A是催化剂 |
| B.反应过程中,钒的成键数目没有改变 |
| C.该催化循环过程中有氢氧键的断裂和形成 |
| D.制备机理的总反应的离子方程式为: H2O2+C1-+H+ =HClO+H2O |
您最近一年使用:0次
2022-07-10更新
|
157次组卷
|
2卷引用:山东省烟台市2021-2022学年高二下学期期末考试化学试题
名校
解题方法
9 . 下列做法的目的与反应速率无关的是
| A.将煤块粉碎后燃烧 | B.食盐中添加碘酸钾 |
| C.合成氨反应中加催化剂Fe | D.医护人员冷藏存放“新冠”疫苗 |
您最近一年使用:0次
2022-05-19更新
|
655次组卷
|
7卷引用:山东省烟台市第二中学等校2021-2022学年高一下学期期中考试化学试题(等级考)
山东省烟台市第二中学等校2021-2022学年高一下学期期中考试化学试题(等级考)(已下线)第07练 化学反应速率及其影响因素-2022年【暑假分层作业】高一化学(人教版2019必修第二册)云南省楚雄天人中学2021-2022学年高一6月月考化学试题吉林省松原市油田第十一中学2021-2022学年高一下学期期末考试化学试题浙江省湖州市三贤联盟2022-2023学年高二上学期期中联考化学试题(已下线)【2022】【高二上】【期中考】【三贤联盟】【高中化学】【李鼎收集】新疆维吾尔自治区皮山县高级中学2023-2024学年高二上学期1月期末化学试题
解题方法
10 . 已知HNO自由基与 的反应:
的反应:
① (产物a)。
(产物a)。
②HNO+O2

 (产物b)。
(产物b)。
反应进程中能量变化如图所示。下列说法正确的是

 的反应:
的反应:①
 (产物a)。
(产物a)。②HNO+O2


 (产物b)。
(产物b)。反应进程中能量变化如图所示。下列说法正确的是

A. 大小关系:①<② 大小关系:①<② |
| B.升高温度①和②的反应速率都加快,有利于提高反应物的转化率 |
| C.产物b比产物a更稳定,故中间产物Z生成b的反应更容易发生 |
| D.反应①共分4步进行,其中第3步对反应①的快慢起决定性作用 |
您最近一年使用:0次



