解题方法
1 . 某化学课外兴趣小组探究过氧化钠与水的反应,探究过程如下:
(1)实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来。请分析脱脂棉燃烧的原因_______ 。
(2)实验2:取一支试管,向其中加入少量过氧化钠固体,然后加入少量蒸馏水,有气泡冒出,充分振荡后再滴入酚酞试液,溶液先变红后褪色。
提出问题:溶液为什么先变红,过了一会,红色又褪去了呢?
猜想:甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色。
查阅资料:
i.H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;
ii.NaOH溶液浓度过高,酚酞不变色或变色后迅速褪色。
设计实验方案:
①取少量褪色后的溶液于试管中,加入MnO2固体,若有气泡冒出,用_______ 检验该气体,则证明该反应过程中生成了_______ (填化学式)使溶液褪色。
②另取少量褪色后的溶液于试管中,加入蒸馏水稀释,若溶液变红,则证明溶液褪色原因可能为_______ 。
(3)为进一步探究过氧化钠与水反应的实质,运用pH传感器、温度传感器、氧气传感器等仪器进行实验探究,得到如下图象。
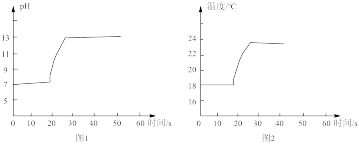
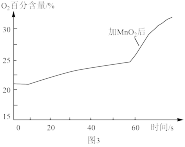
根据图象,得出结论:过氧化钠与水反应过程的方程式为_______ 、_______ 。
(1)实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来。请分析脱脂棉燃烧的原因
(2)实验2:取一支试管,向其中加入少量过氧化钠固体,然后加入少量蒸馏水,有气泡冒出,充分振荡后再滴入酚酞试液,溶液先变红后褪色。
提出问题:溶液为什么先变红,过了一会,红色又褪去了呢?
猜想:甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色。
查阅资料:
i.H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;
ii.NaOH溶液浓度过高,酚酞不变色或变色后迅速褪色。
设计实验方案:
①取少量褪色后的溶液于试管中,加入MnO2固体,若有气泡冒出,用
②另取少量褪色后的溶液于试管中,加入蒸馏水稀释,若溶液变红,则证明溶液褪色原因可能为
(3)为进一步探究过氧化钠与水反应的实质,运用pH传感器、温度传感器、氧气传感器等仪器进行实验探究,得到如下图象。


根据图象,得出结论:过氧化钠与水反应过程的方程式为
您最近一年使用:0次
2 . 研究化学反应速率和化学反应限度具有重要意义。回答下列问题:
(Ⅰ)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
(1)实验①和②的目的是____________________________ 。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进措施是_________________________________________ 。
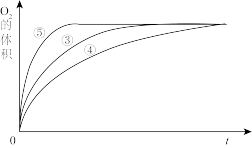
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图。分析图能够得出的实验结论是__________________________________ 。
(Ⅱ)丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈CH3CN等。
(3)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下:
①CH2=CHCH3(g)+NH3(g)+ O2(g)→ CH2=CHCN(g)+3H2O(g) △H=-515 kJ/mol
O2(g)→ CH2=CHCN(g)+3H2O(g) △H=-515 kJ/mol
②CH2=CHCH3(g)+ O2(g)→C3H4O(g)+H2O(g) △H=-353 kJ/mol
有利于提高丙烯腈平衡产率的反应条件是_______________ ;提高丙烯腈反应选择性的关键因素是__________ 。
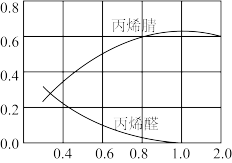
(4)丙烯腈和丙烯醛的产率与n(NH3)/n (丙烯)的关系如图所示。由图可知,最佳n(NH3)/n (丙烯)约为________ ,理由是________________ 。氨、丙烯、空气的进料理论体积比约为__________ 。
(Ⅰ)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol•L-1FeCl3溶液 |

(1)实验①和②的目的是
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图。分析图能够得出的实验结论是
(Ⅱ)丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈CH3CN等。
(3)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下:
①CH2=CHCH3(g)+NH3(g)+
 O2(g)→ CH2=CHCN(g)+3H2O(g) △H=-515 kJ/mol
O2(g)→ CH2=CHCN(g)+3H2O(g) △H=-515 kJ/mol②CH2=CHCH3(g)+ O2(g)→C3H4O(g)+H2O(g) △H=-353 kJ/mol
有利于提高丙烯腈平衡产率的反应条件是
(4)丙烯腈和丙烯醛的产率与n(NH3)/n (丙烯)的关系如图所示。由图可知,最佳n(NH3)/n (丙烯)约为

您最近一年使用:0次
名校
3 . 我国科学家研究了活性炭催化条件下煤气中H2S和Hg的协同脱除,部分反应机理如图所示(吸附在催化剂表面的物种用*标注)。下列说法正确的是
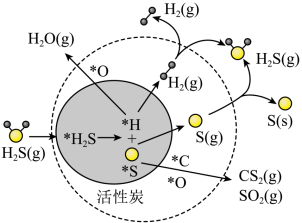
| A.图示反应过程中有极性共价键的断裂,没有非极性共价键的生成 |
| B.H2S活性炭分解生成H2(g)和S(s)的过程释放能量 |
| C.整个脱硫过程中硫元素既表现出氧化性又表现出还原性 |
| D.该机理由于活性炭的参与降低了H2S分解的热效应,使反应更易进行 |
您最近一年使用:0次
2023-04-29更新
|
244次组卷
|
5卷引用:山东省菏泽市2022-2023学年高一下学期期中考试化学(A)试题
名校
4 . 某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
为了探究浓度对反应速率的影响,小组成员设计了三组平行实验,实验时,溶液迅速混合并开始计时通过溶液褪色所需时间来判断反应快慢。(控制反应过程中溶液温度为室温)
【实验原理】
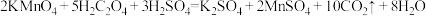
【实验内容及记录】
请回答下列问题:
(1)第三组实验中,所加蒸馏水的体积为x=___________ mL
(2)利用实验2中数据计算,
___________ 。
(3)根据上表中的实验数据,可以得到的结论是___________ 。
(4)该化学小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。

①该小组同学提出的假设是___________ 。
②请你帮助该小组同学完成实验方案,并填写表中空白。
实验4中向试管中加入少量固体___________ 。
③若该小组同学提出的假设成立,室温下溶液颜色褪至无色所需时间___________ (填大于、等于或小于)4 min。
为了探究浓度对反应速率的影响,小组成员设计了三组平行实验,实验时,溶液迅速混合并开始计时通过溶液褪色所需时间来判断反应快慢。(控制反应过程中溶液温度为室温)
【实验原理】
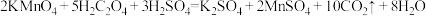
【实验内容及记录】
| 编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | 调控溶液温度 | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/LKMnO4溶液 | 3 mol/L稀硫酸 | |||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 | 298K |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.0 | 298K |
| 3 | 3.0 | x | 1.0 | 2.0 | 6.4 | 298K |
(1)第三组实验中,所加蒸馏水的体积为x=
(2)利用实验2中数据计算,

(3)根据上表中的实验数据,可以得到的结论是
(4)该化学小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。

①该小组同学提出的假设是
②请你帮助该小组同学完成实验方案,并填写表中空白。
| 编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/LKMnO4溶液 |  稀硫酸 稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | ___________ | ___________ |
③若该小组同学提出的假设成立,室温下溶液颜色褪至无色所需时间
您最近一年使用:0次
2023-05-30更新
|
108次组卷
|
4卷引用:山东省滨州市部分学校2022-2023学年高一下学期5月联考化学试题
名校
解题方法
5 . 学习小组在实验室探究催化剂对双氧水分解的作用,查阅资料得知催化剂参与化学反应,通过改变反应历程以改变化学反应速率。回答下列问题:

(1)设计实验探究 对
对 分解反应的催化效果。
分解反应的催化效果。
①结合图中实验,补充操作证明 是
是 分解反应的催化剂
分解反应的催化剂_____________ 。
②分别量取50mL 3% 于三支洁净干燥的试管中,分别加入不同质量的
于三支洁净干燥的试管中,分别加入不同质量的 粉末,40s后测量所得气体体积,数据如下:
粉末,40s后测量所得气体体积,数据如下:
分析数据得出的实验结论是_____ ,分析三支试管中 分解速率不同的可能原因是
分解速率不同的可能原因是______ 。
(2)设计如下实验探究 和
和 对
对 分解反应的催化效果。
分解反应的催化效果。
①试管I、II、III中均盛有10mL 5% :
:
试管I中反应速率大于试管II中反应速率的原因可能是:
ⅰ. 做催化剂且试管I中
做催化剂且试管I中 大
大
ⅱ.__________________________
经查阅资料知 无催化作用,请设计实验证明
无催化作用,请设计实验证明_______________________________________ 。
② 溶液加入
溶液加入 溶液后,溶液中会发生两个氧化还原反应,且两个反应中
溶液后,溶液中会发生两个氧化还原反应,且两个反应中 均参加了反应,从催化剂的角度分析两个氧化还原反应的离子方程式分别是
均参加了反应,从催化剂的角度分析两个氧化还原反应的离子方程式分别是__________________________ 和___________________________________________ (按反应发生的顺序写)。

(1)设计实验探究
 对
对 分解反应的催化效果。
分解反应的催化效果。①结合图中实验,补充操作证明
 是
是 分解反应的催化剂
分解反应的催化剂②分别量取50mL 3%
 于三支洁净干燥的试管中,分别加入不同质量的
于三支洁净干燥的试管中,分别加入不同质量的 粉末,40s后测量所得气体体积,数据如下:
粉末,40s后测量所得气体体积,数据如下:
| 0.1 | 0.2 | 0.4 |
40s时 | 49 | 61 | 86 |
 分解速率不同的可能原因是
分解速率不同的可能原因是(2)设计如下实验探究
 和
和 对
对 分解反应的催化效果。
分解反应的催化效果。①试管I、II、III中均盛有10mL 5%
 :
:试管 | I | II | III |
滴加试剂 | 5滴0.1 | 5滴0.1 | 5滴蒸馏水 |
现象 | 较快产生细小气泡 | 缓慢产生细小气泡 | 无明显现象 |
ⅰ.
 做催化剂且试管I中
做催化剂且试管I中 大
大ⅱ.
经查阅资料知
 无催化作用,请设计实验证明
无催化作用,请设计实验证明②
 溶液加入
溶液加入 溶液后,溶液中会发生两个氧化还原反应,且两个反应中
溶液后,溶液中会发生两个氧化还原反应,且两个反应中 均参加了反应,从催化剂的角度分析两个氧化还原反应的离子方程式分别是
均参加了反应,从催化剂的角度分析两个氧化还原反应的离子方程式分别是
您最近一年使用:0次
解题方法
6 . 酯在碱性条件下发生水解反应的历程如图,下列说法正确的是

| A.反应①为该反应的决速步 |
B.若用 进行标记,反应结束后醇和羧酸钠中均存在 进行标记,反应结束后醇和羧酸钠中均存在 |
| C.该反应历程中碳原子杂化方式没有发生改变 |
D.反应①中 攻击的位置由碳和氧电负性大小决定 攻击的位置由碳和氧电负性大小决定 |
您最近一年使用:0次
7 . 根据实验操作和现象,对应结论正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 将 固体粉末加入过量NaOH溶液,搅拌 固体粉末加入过量NaOH溶液,搅拌 | 固体完全溶解,形成无色溶液 |  既体现酸性又体现碱性 既体现酸性又体现碱性 |
B | 用洁净的铂丝蘸取某溶液在酒精灯火焰灼烧 | 火焰呈黄色 | 该溶液是钠的盐溶液 |
C | 将银和硝酸银溶液与铜和硫酸铜稀溶液组成原电池,连通后一段时间 | 银表面有金属沉积,铜附近溶液蓝色变深 | 铜的金属性比银强 |
D | 向两支均盛有5mL 10%  溶液的试管中,分别加入0.1 溶液的试管中,分别加入0.1 的 的 溶液和0.1 溶液和0.1  溶液 溶液 | 产生气泡,加入 溶液的试管中产生气泡快 溶液的试管中产生气泡快 |  比 比 的催化效果更好 的催化效果更好 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 下列实验操作及现象正确,且与解释或结论存在对应关系是
| 选项 | 实验操作及现象 | 解释或结论 |
| A | 向双氧水中滴加酸性 溶液,迅速有气泡生成 溶液,迅速有气泡生成 |  对 对 分解具有催化作用 分解具有催化作用 |
| B | 向 溶液中滴入足量氯水和 溶液中滴入足量氯水和 ,振荡、静置、分层;再向上层溶液中加入KSCN溶液,下层溶液呈紫红色,上层溶液变为血红色。 ,振荡、静置、分层;再向上层溶液中加入KSCN溶液,下层溶液呈紫红色,上层溶液变为血红色。 | 证明还原性: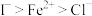 |
| C | 向硫酸酸化的食盐溶液中加入KI溶液和几滴淀粉溶液,溶液未变蓝色 | 该食盐不是含碘盐 |
| D | 向 溶液中滴入稀盐酸,出现白色凝胶 溶液中滴入稀盐酸,出现白色凝胶 | 非金属性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-30更新
|
80次组卷
|
2卷引用:山东省滨州市部分学校2022-2023学年高一下学期5月联考化学试题
名校
解题方法
9 . 以 为原料制备甲烷、甲醇等能源物质具有较好的发展前景。回答下列问题:
为原料制备甲烷、甲醇等能源物质具有较好的发展前景。回答下列问题:
(1) 在固体催化表面加氢合成甲烷过程中发生以下两个反应:
在固体催化表面加氢合成甲烷过程中发生以下两个反应:
主反应: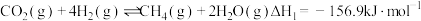
副反应: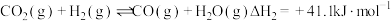
①已知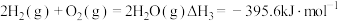 ,则
,则 燃烧的热化学方程式
燃烧的热化学方程式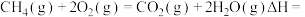
_______  。
。
②对于主反应,在一定条件下存在: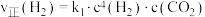 或
或 ,相应的速率与温度关系如图所示。
,相应的速率与温度关系如图所示。
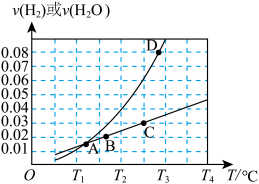
则主反应的平衡常数
_______ (用含 的代数式表示);图中
的代数式表示);图中 四个点中,能表示反应已达到平衡状态的是
四个点中,能表示反应已达到平衡状态的是_______ 。
(2)某研究小组采用双合金团簇催化甲烷干法重整法(DRM)取得了良好的效果。通过大量的研究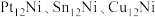 三种双金属合金团簇可用于催化
三种双金属合金团簇可用于催化 反应,在催化剂表面涉及多个基元反应,分别为过程1:甲烷逐步脱氢,过程2:
反应,在催化剂表面涉及多个基元反应,分别为过程1:甲烷逐步脱氢,过程2: 的活化(包括直接活化和氢诱导活化),过程3:
的活化(包括直接活化和氢诱导活化),过程3: 和
和 的氧化,过程4:扩散吸附反应。其反应机理如图所示。
的氧化,过程4:扩散吸附反应。其反应机理如图所示。
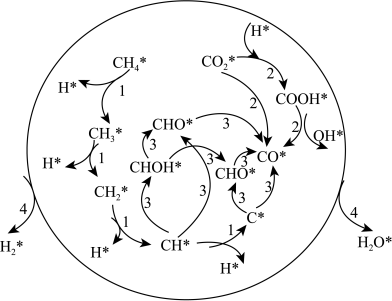
则过程3的最终产物为_______ ,过程4发生扩散吸附反应的微粒为_______ 。
(3)光催化 制甲醇技术也是研究热点。铜基纳米光催化材料还原
制甲醇技术也是研究热点。铜基纳米光催化材料还原 的机理为:光照时,低能价带失去电子并产生空穴(
的机理为:光照时,低能价带失去电子并产生空穴( ,具有强氧化性)。
,具有强氧化性)。
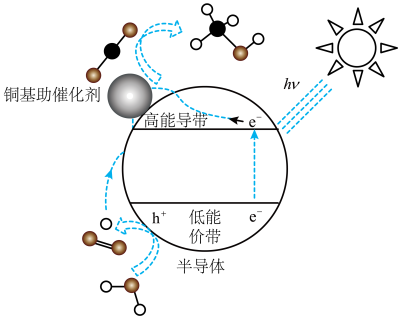
光催化原理与电解原理类似,写出高能导带的电极反应式:_______ 。太阳光激发下,在导带和价带中除了产生电子和空穴外,还会生成_______ (填写微粒名称)参与 的还原再生。
的还原再生。
 为原料制备甲烷、甲醇等能源物质具有较好的发展前景。回答下列问题:
为原料制备甲烷、甲醇等能源物质具有较好的发展前景。回答下列问题:(1)
 在固体催化表面加氢合成甲烷过程中发生以下两个反应:
在固体催化表面加氢合成甲烷过程中发生以下两个反应:主反应:
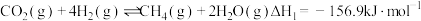
副反应:
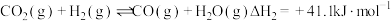
①已知
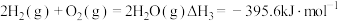 ,则
,则 燃烧的热化学方程式
燃烧的热化学方程式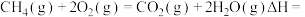
 。
。②对于主反应,在一定条件下存在:
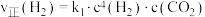 或
或 ,相应的速率与温度关系如图所示。
,相应的速率与温度关系如图所示。
则主反应的平衡常数

 的代数式表示);图中
的代数式表示);图中 四个点中,能表示反应已达到平衡状态的是
四个点中,能表示反应已达到平衡状态的是(2)某研究小组采用双合金团簇催化甲烷干法重整法(DRM)取得了良好的效果。通过大量的研究
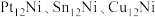 三种双金属合金团簇可用于催化
三种双金属合金团簇可用于催化 反应,在催化剂表面涉及多个基元反应,分别为过程1:甲烷逐步脱氢,过程2:
反应,在催化剂表面涉及多个基元反应,分别为过程1:甲烷逐步脱氢,过程2: 的活化(包括直接活化和氢诱导活化),过程3:
的活化(包括直接活化和氢诱导活化),过程3: 和
和 的氧化,过程4:扩散吸附反应。其反应机理如图所示。
的氧化,过程4:扩散吸附反应。其反应机理如图所示。
则过程3的最终产物为
(3)光催化
 制甲醇技术也是研究热点。铜基纳米光催化材料还原
制甲醇技术也是研究热点。铜基纳米光催化材料还原 的机理为:光照时,低能价带失去电子并产生空穴(
的机理为:光照时,低能价带失去电子并产生空穴( ,具有强氧化性)。
,具有强氧化性)。
光催化原理与电解原理类似,写出高能导带的电极反应式:
 的还原再生。
的还原再生。
您最近一年使用:0次
2024·安徽安庆·二模
解题方法
10 . 中科大某课题组通过自由基杂环反应直接合成各种 稠合的内酰胺,应用于钙钛矿电池器件中。底物与Cu(Ⅰ)物种通过电子转移经历两种途径得到目标产物D。下列说法错误的是
稠合的内酰胺,应用于钙钛矿电池器件中。底物与Cu(Ⅰ)物种通过电子转移经历两种途径得到目标产物D。下列说法错误的是
 稠合的内酰胺,应用于钙钛矿电池器件中。底物与Cu(Ⅰ)物种通过电子转移经历两种途径得到目标产物D。下列说法错误的是
稠合的内酰胺,应用于钙钛矿电池器件中。底物与Cu(Ⅰ)物种通过电子转移经历两种途径得到目标产物D。下列说法错误的是
| A.Cu(Ⅰ)物种是催化剂 | B.底物具有氧化性 |
| C.两种途径不同,总反应的反应热也不同 | D.合成过程中 中碳碳双键断裂 中碳碳双键断裂 |
您最近一年使用:0次

 体积/mL
体积/mL


