甲醇是重要的化工原料,可以使用多种方法制备甲醇。
I.利用反应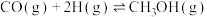
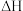 ,若在体积一定的密闭容器中按物质的量之比1:2充入CO和
,若在体积一定的密闭容器中按物质的量之比1:2充入CO和 ,测得平衡混合物中
,测得平衡混合物中 的体积分数在不同压强下随温度的变化情况如如图所示。
的体积分数在不同压强下随温度的变化情况如如图所示。
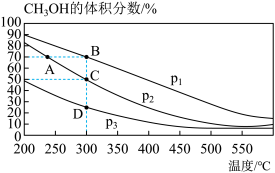
(1)该反应的
______ 0(填“>”“<”或“=”)
(2)达到平衡时,反应速率:A点____ B点(填“>”“<”或“=”)。在C点时,CO的转化率为____ 。
(3)要提高CO的平衡转化率,可以采取的措施是______ (填字母)。
A.加入催化剂 B.增大CO的浓度 C.通入 D.通入惰性气体 E.分离出甲醇
D.通入惰性气体 E.分离出甲醇
(4)关于该反应,下列说法正确的是___________(填字母)。
Ⅱ.利用 与在催化剂的作用下合成甲醇。主反应:
与在催化剂的作用下合成甲醇。主反应: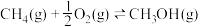 ,在温度为 T℃、压强为
,在温度为 T℃、压强为 条件下,向容器中充入
条件下,向容器中充入 、
、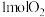 ,充分反应达平衡时
,充分反应达平衡时 的转化率为
的转化率为 。
。
(5)求平衡时 的物质的量为
的物质的量为______ 。
(6)主反应的相对压力平衡常数
___________ ( 表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。用含p的式子表示)。
表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。用含p的式子表示)。
I.利用反应
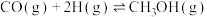
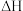 ,若在体积一定的密闭容器中按物质的量之比1:2充入CO和
,若在体积一定的密闭容器中按物质的量之比1:2充入CO和 ,测得平衡混合物中
,测得平衡混合物中 的体积分数在不同压强下随温度的变化情况如如图所示。
的体积分数在不同压强下随温度的变化情况如如图所示。
(1)该反应的

(2)达到平衡时,反应速率:A点
(3)要提高CO的平衡转化率,可以采取的措施是
A.加入催化剂 B.增大CO的浓度 C.通入
 D.通入惰性气体 E.分离出甲醇
D.通入惰性气体 E.分离出甲醇(4)关于该反应,下列说法正确的是___________(填字母)。
| A.该反应在任何温度下都能自发进行 | B.使用催化剂,不能提高CO的平衡转化率 |
| C.升高温度,正反应速率增大,逆反应速率减小 | D.增大压强,该反应的化学平衡常数不变 |
Ⅱ.利用
 与在催化剂的作用下合成甲醇。主反应:
与在催化剂的作用下合成甲醇。主反应: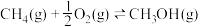 ,在温度为 T℃、压强为
,在温度为 T℃、压强为 条件下,向容器中充入
条件下,向容器中充入 、
、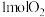 ,充分反应达平衡时
,充分反应达平衡时 的转化率为
的转化率为 。
。(5)求平衡时
 的物质的量为
的物质的量为(6)主反应的相对压力平衡常数

 表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。用含p的式子表示)。
表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。用含p的式子表示)。
更新时间:2023-12-23 17:12:00
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学实验小组用酸性KMnO4溶液与草酸(H2C2O4)溶液反应,研究外界条件对反应速率的影响,实验操作及现象如下:
(1)写出高锰酸钾与草酸反应的离子方程式:_______ 。
(2)由实验Ⅰ、Ⅱ可得出的结论是_______ 。
(3)关于实验Ⅱ中3 min后溶液颜色迅速变浅的原因,该小组提出猜想:反应中生成的Mn2+对该反应有催化作用。利用提供的试剂设计实验Ⅲ,验证猜想。
提供的试剂:0.01 mol/L酸性KMnO4溶液,0.1 mol/L草酸溶液,3 mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水
补全实验Ⅲ的操作:向试管中先加入1 mL0.01 mol/L酸性KMnO4溶液,再加10滴3mol/L硫酸,_______ ,最后加入1 mL0.1 mol/L草酸溶液。
(4)该小组拟采用如下图所示的实验方案继续探究KMnO4溶液浓度对反应速率的影响。经测定乙试管溶液褪色的时间比甲试管长,得出结论:浓度越大,反应速率越慢。你认为他们的实验方案_______ (填“合理”或“不合理”),理由是_______ 。

| 编号 | 实验操作 | 实验现象 |
| Ⅰ | 向一支试管中先加入1 mL0.01 mol/L酸性KMnO4溶液,再加入1滴3 mol/L硫酸和9滴蒸馏水,最后加入1 mL0.1 mol/L草酸溶液 | 前10 min内溶液紫色无明显变化,后颜色逐渐变浅,30 min后几乎变为无色 |
| Ⅱ | 向另一支试管中先加入1 mL0.01 mol/L酸性KMnO4溶液,再加入10滴3mol/L硫酸,最后加入1 mL0.1 mol/L草酸溶液 | 1 min内溶液紫色无明显变化,后颜色迅速变浅,约3 min后几乎变为无色 |
(2)由实验Ⅰ、Ⅱ可得出的结论是
(3)关于实验Ⅱ中3 min后溶液颜色迅速变浅的原因,该小组提出猜想:反应中生成的Mn2+对该反应有催化作用。利用提供的试剂设计实验Ⅲ,验证猜想。
提供的试剂:0.01 mol/L酸性KMnO4溶液,0.1 mol/L草酸溶液,3 mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水
补全实验Ⅲ的操作:向试管中先加入1 mL0.01 mol/L酸性KMnO4溶液,再加10滴3mol/L硫酸,
(4)该小组拟采用如下图所示的实验方案继续探究KMnO4溶液浓度对反应速率的影响。经测定乙试管溶液褪色的时间比甲试管长,得出结论:浓度越大,反应速率越慢。你认为他们的实验方案

您最近一年使用:0次
【推荐2】CO2的资源化利用和转化已成为当今科学研究的热点。
(1) CO2和环氧乙烷在MgO作催化剂的条件下合成碳酸乙烯酯。
①MgCl2溶液中加入尿素 生成
生成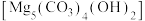 沉淀和
沉淀和 ,并产生CO2气体。该反应的离子方程式为
,并产生CO2气体。该反应的离子方程式为__________ 。
②MgCl2与氢氧化钠反应生成沉淀,过滤后将沉淀焙烧得到MgO。与氢氧化钠作沉淀剂相比,用尿素作沉淀剂焙烧生成的MgO作催化剂效果更好,其原因是__________ 。
(2)以CH4和CO2催化重整制备合成气。
恒压,750℃时,CH4和CO2按物质的量之比1∶3投料,经过如下流程可实现CO2高效转化。
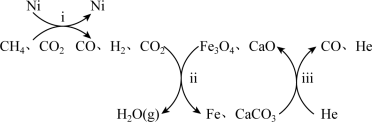
①写出过程ⅱ产生H2O(g)的化学方程式:__________ 。
②上述流程中参与反应且可循环利用的物质有______ 。
A.Fe3O4 B.CaO C.H2O D.He
(3)我国科学家研发了一种水系可逆Zn-CO2电池,电极材料为金属锌和选择性催化材料。电池工作时,双极隔膜(由阴、阳膜复合而成)层间的H2O解离成H+和OH-,在外加电场中可透过相应的离子膜定向移动。电池工作原理如题图所示:
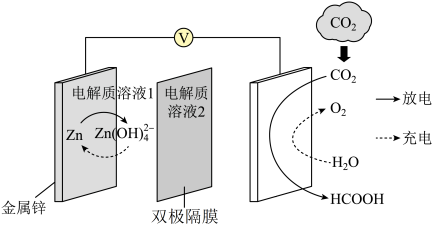
放电时,电池正极反应为__________ 。
(1) CO2和环氧乙烷在MgO作催化剂的条件下合成碳酸乙烯酯。
①MgCl2溶液中加入尿素
 生成
生成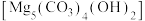 沉淀和
沉淀和 ,并产生CO2气体。该反应的离子方程式为
,并产生CO2气体。该反应的离子方程式为②MgCl2与氢氧化钠反应生成沉淀,过滤后将沉淀焙烧得到MgO。与氢氧化钠作沉淀剂相比,用尿素作沉淀剂焙烧生成的MgO作催化剂效果更好,其原因是
(2)以CH4和CO2催化重整制备合成气。
恒压,750℃时,CH4和CO2按物质的量之比1∶3投料,经过如下流程可实现CO2高效转化。

①写出过程ⅱ产生H2O(g)的化学方程式:
②上述流程中参与反应且可循环利用的物质有
A.Fe3O4 B.CaO C.H2O D.He
(3)我国科学家研发了一种水系可逆Zn-CO2电池,电极材料为金属锌和选择性催化材料。电池工作时,双极隔膜(由阴、阳膜复合而成)层间的H2O解离成H+和OH-,在外加电场中可透过相应的离子膜定向移动。电池工作原理如题图所示:

放电时,电池正极反应为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】“碳达峰•碳中和”是我国社会发展重大战略之一, 和
和 的转化和利用是实现“双碳”经济的有效途径,相关的主要反应有:
的转化和利用是实现“双碳”经济的有效途径,相关的主要反应有:
Ⅰ:
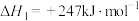 ,
,
Ⅱ:
 ,
,
请回答:
(1) 的电子式为
的电子式为___________ 。
(2)反应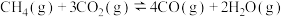 的
的
___________  ,
,
___________ (用 ,
, 表示)。
表示)。
(3)科学家提出利用太阳能由 制取C,工艺如图。已知“重整系统”发生的反应中
制取C,工艺如图。已知“重整系统”发生的反应中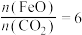 ,则
,则 的化学式为
的化学式为___________ 。

(4) 和
和 合成乙醇反应为:
合成乙醇反应为: 。将等物质的量的
。将等物质的量的 和
和 充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图。
充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图。
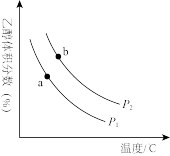
①压强
___________  (填“>”“=”或“<”,下同),a,b两点的平衡常数
(填“>”“=”或“<”,下同),a,b两点的平衡常数
___________  。
。
②已知Arrhenius经验公式为 (
( 为活化能,k为速率常数,R和C为常数)。为探究m,n两种催化剂的催化效能,某实验小组进行了实验探究,依据实验数据获得如图曲线。
为活化能,k为速率常数,R和C为常数)。为探究m,n两种催化剂的催化效能,某实验小组进行了实验探究,依据实验数据获得如图曲线。
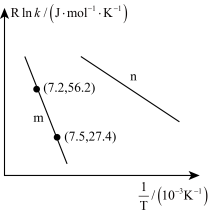
在m催化剂作用下,该反应的活化能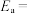
___________  。从图中信息获知催化效能较高的催化剂是
。从图中信息获知催化效能较高的催化剂是___________ (“m”或“n”)。
 和
和 的转化和利用是实现“双碳”经济的有效途径,相关的主要反应有:
的转化和利用是实现“双碳”经济的有效途径,相关的主要反应有:Ⅰ:

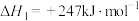 ,
,
Ⅱ:

 ,
,
请回答:
(1)
 的电子式为
的电子式为(2)反应
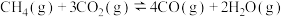 的
的
 ,
,
 ,
, 表示)。
表示)。(3)科学家提出利用太阳能由
 制取C,工艺如图。已知“重整系统”发生的反应中
制取C,工艺如图。已知“重整系统”发生的反应中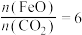 ,则
,则 的化学式为
的化学式为
(4)
 和
和 合成乙醇反应为:
合成乙醇反应为: 。将等物质的量的
。将等物质的量的 和
和 充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图。
充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图。
①压强

 (填“>”“=”或“<”,下同),a,b两点的平衡常数
(填“>”“=”或“<”,下同),a,b两点的平衡常数
 。
。②已知Arrhenius经验公式为
 (
( 为活化能,k为速率常数,R和C为常数)。为探究m,n两种催化剂的催化效能,某实验小组进行了实验探究,依据实验数据获得如图曲线。
为活化能,k为速率常数,R和C为常数)。为探究m,n两种催化剂的催化效能,某实验小组进行了实验探究,依据实验数据获得如图曲线。
在m催化剂作用下,该反应的活化能
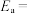
 。从图中信息获知催化效能较高的催化剂是
。从图中信息获知催化效能较高的催化剂是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】处理、回收利用CO是环境科学研究的热点课题。回答下列问题:
(1)CO用于处理大气污染物N2O的反应为CO(g)+N2O(g) CO2(g)+N2(g)。在Zn+作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。
CO2(g)+N2(g)。在Zn+作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。

总反应:CO(g)+N2O(g) CO2(g)+N2(g) ΔH=
CO2(g)+N2(g) ΔH=_______ kJ·mol-1,该总反应的决速步是反应_______ (填“①”或“②”),该判断的理由是_______ 。
(2)已知:CO(g)+N2O(g)
 CO2(g)+N2(g)的速率方程为v=k·c(N2O),k为速率常数,只与温度有关。为提高反应速率,可采取的措施是_______(填字母序号)。
CO2(g)+N2(g)的速率方程为v=k·c(N2O),k为速率常数,只与温度有关。为提高反应速率,可采取的措施是_______(填字母序号)。
(3)在总压为100kPa的恒容密闭容器中,充入一定量的CO(g)和N2O(g)发生上述反应,在不同条件下达到平衡时,在T1K时N2O的转化率与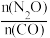 、在
、在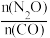 =1时N2O的转化率与
=1时N2O的转化率与 的变化曲线如图3所示:
的变化曲线如图3所示:

①表示N2O的转化率随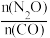 的变化曲线为
的变化曲线为_______ 曲线(填“I”或“Ⅱ”);
②T1_______ T2(填“>”或“<”);
(4)已知:该反应的标准平衡常数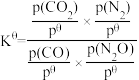 ,其中pθ为标准压强(100kPa),p(CO2)、p(N2)、p(N2O)和p(CO)为各组分的平衡分压,则T4时,该反应的标准平衡常数Kθ=
,其中pθ为标准压强(100kPa),p(CO2)、p(N2)、p(N2O)和p(CO)为各组分的平衡分压,则T4时,该反应的标准平衡常数Kθ=_______ (计算结果保留两位有效数字,P分=P总×物质的量分数)。
(1)CO用于处理大气污染物N2O的反应为CO(g)+N2O(g)
 CO2(g)+N2(g)。在Zn+作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。
CO2(g)+N2(g)。在Zn+作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。
总反应:CO(g)+N2O(g)
 CO2(g)+N2(g) ΔH=
CO2(g)+N2(g) ΔH=(2)已知:CO(g)+N2O(g)

 CO2(g)+N2(g)的速率方程为v=k·c(N2O),k为速率常数,只与温度有关。为提高反应速率,可采取的措施是_______(填字母序号)。
CO2(g)+N2(g)的速率方程为v=k·c(N2O),k为速率常数,只与温度有关。为提高反应速率,可采取的措施是_______(填字母序号)。| A.恒容时,再充入CO | B.恒压时,再充入N2O | C.恒压时,再充入N2 | D.升温 |
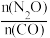 、在
、在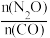 =1时N2O的转化率与
=1时N2O的转化率与 的变化曲线如图3所示:
的变化曲线如图3所示:
①表示N2O的转化率随
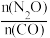 的变化曲线为
的变化曲线为②T1
(4)已知:该反应的标准平衡常数
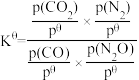 ,其中pθ为标准压强(100kPa),p(CO2)、p(N2)、p(N2O)和p(CO)为各组分的平衡分压,则T4时,该反应的标准平衡常数Kθ=
,其中pθ为标准压强(100kPa),p(CO2)、p(N2)、p(N2O)和p(CO)为各组分的平衡分压,则T4时,该反应的标准平衡常数Kθ=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】气候变化是目前全球最重要、最紧迫的议题之一,中国作为负责任大国,自主提出力争2030年碳达峰、2060年碳中和的目标。 的综合利用是解决该问题的有效途径。
的综合利用是解决该问题的有效途径。
(1)将 转化为乙醇可以实现降碳,过程中发生的反应如下:
转化为乙醇可以实现降碳,过程中发生的反应如下:
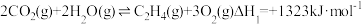


则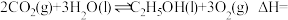
___________ 。
(2)将 转化为甲醇也可以实现降碳。
转化为甲醇也可以实现降碳。
一定条件下,发生反应 。往
。往 恒容密闭容器中充入
恒容密闭容器中充入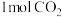 和
和 ,在甲、乙不同催化剂作用下,反应时间均为
,在甲、乙不同催化剂作用下,反应时间均为 时,测得甲醇的物质的量分数随温度变化如图所示:
时,测得甲醇的物质的量分数随温度变化如图所示:

①相同温度下催化剂效果更好的催化剂是___________ (填“甲”或“乙”), 温度下甲醇的平均反应速率
温度下甲醇的平均反应速率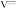
___________ 。
②在甲催化作用下,甲醇的物质的量分数随温度的升高呈现如图变化的原因是___________ 。
③在 和
和 温度下,平衡常数
温度下,平衡常数
___________  (填“>”、“<”或“=”)。下列能够说明该反应达到平衡状态的是
(填“>”、“<”或“=”)。下列能够说明该反应达到平衡状态的是___________ 。
a.混合气体的密度不变 b.容器内压强不变
c.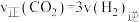 d.混合气体平均相对分子质量不变
d.混合气体平均相对分子质量不变
④已知气体分压=气体总压×气体的物质的量分数。 温度下,反应开始时容器中的总压为
温度下,反应开始时容器中的总压为 ,该温度下反应的平衡常数
,该温度下反应的平衡常数
___________ (只列出计算式,不必化简)。
 的综合利用是解决该问题的有效途径。
的综合利用是解决该问题的有效途径。(1)将
 转化为乙醇可以实现降碳,过程中发生的反应如下:
转化为乙醇可以实现降碳,过程中发生的反应如下: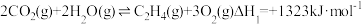


则
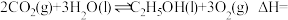
(2)将
 转化为甲醇也可以实现降碳。
转化为甲醇也可以实现降碳。一定条件下,发生反应
 。往
。往 恒容密闭容器中充入
恒容密闭容器中充入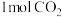 和
和 ,在甲、乙不同催化剂作用下,反应时间均为
,在甲、乙不同催化剂作用下,反应时间均为 时,测得甲醇的物质的量分数随温度变化如图所示:
时,测得甲醇的物质的量分数随温度变化如图所示:
①相同温度下催化剂效果更好的催化剂是
 温度下甲醇的平均反应速率
温度下甲醇的平均反应速率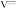
②在甲催化作用下,甲醇的物质的量分数随温度的升高呈现如图变化的原因是
③在
 和
和 温度下,平衡常数
温度下,平衡常数
 (填“>”、“<”或“=”)。下列能够说明该反应达到平衡状态的是
(填“>”、“<”或“=”)。下列能够说明该反应达到平衡状态的是a.混合气体的密度不变 b.容器内压强不变
c.
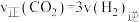 d.混合气体平均相对分子质量不变
d.混合气体平均相对分子质量不变④已知气体分压=气体总压×气体的物质的量分数。
 温度下,反应开始时容器中的总压为
温度下,反应开始时容器中的总压为 ,该温度下反应的平衡常数
,该温度下反应的平衡常数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】温室气体的利用是当前环境和能源领域的研究热点,合理利用燃料废气中的CO2,也是实现“碳中和”的途径之一。
I.温室气体CO2转化为重要的工业原料甲酸是目前科学研究的热点。回答下列问题:
(1)已知:①CO(g)+H2O(g) HCOOH(g) △H1=−72.6kJ·mol−1
HCOOH(g) △H1=−72.6kJ·mol−1
②2CO(g)+O2(g) 2CO2(g) △H2=−566.0kJ·mol−1
2CO2(g) △H2=−566.0kJ·mol−1
则反应③的平衡常数表达式K=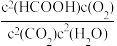 ,写出反应③的热化学方程式
,写出反应③的热化学方程式_______ 。
(2)刚性绝热密闭容器中,等物质的量的CO2(g)和H2O(g)发生反应③,下列可判断反应达到平衡的是_______(填标号)。
Ⅱ.CO2−CH4催化重整对减少温室气体的排放、改善大气环境具有重要的意义。
(3)在密闭容器中通入物质的量均为0.2mol的CH4和CO2,在一定条件下发生反应CH4(g)+CO2(g) ⇌2CO(g)+2H2(g),CH4的平衡转化率与温度及压强的关系如图所示。

①由如图可知:压强p1_______ p2(填“>”、“<”或“=”)。
②Y点:υ(正)_______ υ(逆)(填“>”、“<”或“=”)。
I.温室气体CO2转化为重要的工业原料甲酸是目前科学研究的热点。回答下列问题:
(1)已知:①CO(g)+H2O(g)
 HCOOH(g) △H1=−72.6kJ·mol−1
HCOOH(g) △H1=−72.6kJ·mol−1②2CO(g)+O2(g)
 2CO2(g) △H2=−566.0kJ·mol−1
2CO2(g) △H2=−566.0kJ·mol−1则反应③的平衡常数表达式K=
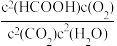 ,写出反应③的热化学方程式
,写出反应③的热化学方程式(2)刚性绝热密闭容器中,等物质的量的CO2(g)和H2O(g)发生反应③,下列可判断反应达到平衡的是_______(填标号)。
| A.CO2(g)和H2O(g)的物质的量之比不变 | B.容器中气体平均摩尔质量不变 |
| C.2υ正(CO2)= υ逆(O2) | D.容器内温度不变 |
Ⅱ.CO2−CH4催化重整对减少温室气体的排放、改善大气环境具有重要的意义。
(3)在密闭容器中通入物质的量均为0.2mol的CH4和CO2,在一定条件下发生反应CH4(g)+CO2(g) ⇌2CO(g)+2H2(g),CH4的平衡转化率与温度及压强的关系如图所示。

①由如图可知:压强p1
②Y点:υ(正)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】用CH4催化还原NOx可以消除氮氧化物的污染。例如:
反应1:CH4(g)+4NO2(g) 4NO(g)+CO2(g)+2H2O(g) ∆H1=-574kJ·mol-1
4NO(g)+CO2(g)+2H2O(g) ∆H1=-574kJ·mol-1
反应2:CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(g) ∆H2=-1160kJ·mol-1
2N2(g)+CO2(g)+2H2O(g) ∆H2=-1160kJ·mol-1
(1)1mol CH4还原NO2至N2,写出该过程的热化学方程式___________ 。
(2)用CH4催化还原NO,能提高N2的平衡产率的措施是___________(填字母)。
(3)一定温度下,在初始体积为2L恒容密闭容器中通入1mol CH4和4mol NO(假设只发生反应2)。
①下列能说明该反应已经达到平衡状态的是___________ (填字母)。
A.c(CH4)和c(CO2)的浓度比保持不变 B.混合气体的密度保持不变
C.CH4的消耗速率等于CO2的消耗速率 D.容器内气体压强保持不变
② 后该反应达到平衡,测得容器中N2的物质的量为
后该反应达到平衡,测得容器中N2的物质的量为 。则从反应开始至刚达到平衡用NO表示的反应速率v(NO)=
。则从反应开始至刚达到平衡用NO表示的反应速率v(NO)=___________ 。
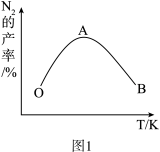
(4)为了提高CH4和NO转化为N2的产率,种学家寻找了一种新型的催化剂。将CH4和NO按一定比例、一定流速通过装有上述新型催化剂的反应器中,反应相同时间,测得N2的产率与温度的关系如图1所示,OA段N2产率随温度升高而增大的原因是___________ 。
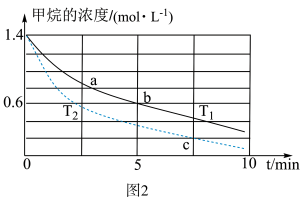
(5)对于反应2而言,不同温度下,CH4的浓度变化如图2所示,下列说法正确的是___________(填字母)。
反应1:CH4(g)+4NO2(g)
 4NO(g)+CO2(g)+2H2O(g) ∆H1=-574kJ·mol-1
4NO(g)+CO2(g)+2H2O(g) ∆H1=-574kJ·mol-1反应2:CH4(g)+4NO(g)
 2N2(g)+CO2(g)+2H2O(g) ∆H2=-1160kJ·mol-1
2N2(g)+CO2(g)+2H2O(g) ∆H2=-1160kJ·mol-1(1)1mol CH4还原NO2至N2,写出该过程的热化学方程式
(2)用CH4催化还原NO,能提高N2的平衡产率的措施是___________(填字母)。
| A.升高温度 | B.增大压强 | C.降低温度 | D.降低压强 |
①下列能说明该反应已经达到平衡状态的是
A.c(CH4)和c(CO2)的浓度比保持不变 B.混合气体的密度保持不变
C.CH4的消耗速率等于CO2的消耗速率 D.容器内气体压强保持不变
②
 后该反应达到平衡,测得容器中N2的物质的量为
后该反应达到平衡,测得容器中N2的物质的量为 。则从反应开始至刚达到平衡用NO表示的反应速率v(NO)=
。则从反应开始至刚达到平衡用NO表示的反应速率v(NO)=(4)为了提高CH4和NO转化为N2的产率,种学家寻找了一种新型的催化剂。将CH4和NO按一定比例、一定流速通过装有上述新型催化剂的反应器中,反应相同时间,测得N2的产率与温度的关系如图1所示,OA段N2产率随温度升高而增大的原因是

(5)对于反应2而言,不同温度下,CH4的浓度变化如图2所示,下列说法正确的是___________(填字母)。

| A.T1大于T2 |
| B.c点二氧化碳的浓度为0.2 mol·L-1 |
| C.a点正反应速率大于b点的正反应速率 |
| D.a点的反应速率一定比c点的反应速率小 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】二甲醚(CH3OCH3)被称为21世纪的新型燃料,25℃,101kPa时呈气态,它清洁、高效、具有优良的环保性能。92g气态二甲醚25℃,101kPa时燃烧放热2910kJ。
(1)写出二甲醚燃烧热的热化学方程式_______________________________________________ ;当燃烧放出582kJ热量时,转移的电子数为_______________ 。
(2)已知H2(g)和C(s)的燃烧热分别是285.8kJ/mol、393.5kJ/mo;计算反应4C(s)+6H2(g)+O2(g)═2CH3OCH3(g)的反应热为______________________________ ;
(3)工业上利用H2和CO2合成二甲醚的反应如下:
6H2(g)+2CO2(g) CH3OCH3(g)+3H2O(g)△H<0
CH3OCH3(g)+3H2O(g)△H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应.下列能判断反应达到化学平衡状态的是______________________________ (选填字母编号)
A. c(H2)与c(H2O)的比值保持不变
B.单位时间内有2mol H2消耗时有1mol H2O生成
C.容器中气体密度不再改变
D.容器中气体压强不再改变
E.反应产生的热量不再变化
②温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产量将_______________ (填“变大”、“变小”或“不变”,下同),混合气体的平均摩尔质量将_______________ 。
(1)写出二甲醚燃烧热的热化学方程式
(2)已知H2(g)和C(s)的燃烧热分别是285.8kJ/mol、393.5kJ/mo;计算反应4C(s)+6H2(g)+O2(g)═2CH3OCH3(g)的反应热为
(3)工业上利用H2和CO2合成二甲醚的反应如下:
6H2(g)+2CO2(g)
 CH3OCH3(g)+3H2O(g)△H<0
CH3OCH3(g)+3H2O(g)△H<0①一定温度下,在一个固定体积的密闭容器中进行该反应.下列能判断反应达到化学平衡状态的是
A. c(H2)与c(H2O)的比值保持不变
B.单位时间内有2mol H2消耗时有1mol H2O生成
C.容器中气体密度不再改变
D.容器中气体压强不再改变
E.反应产生的热量不再变化
②温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产量将
您最近一年使用:0次
【推荐3】近年来,中国华北华中地区发生了严重的雾霾天气。汽车尾气、燃煤废气、冬季取暖排放的CO2等都是雾霾形成的原因。
(1)汽车尾气中排放的NOx和CO污染环境,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。已知:① 2CO(g)+O2(g)⇌2CO2(g) ΔH=−566.0 kJ/mol,② N2(g)+O2(g)⇌2NO(g) ΔH=+180.5 kJ/mol,③ 2NO(g)+O2(g)⇌2NO2(g) ΔH=−116.5 kJ/mol。回答下列问题:
CO的燃烧热为________ 。CO将NO2还原为单质的热化学方程式为______________ 。
(2)改变煤的利用方式可减少环境污染,通常可将煤气化转化为水煤气,其反应原理为:C(s)+H2O(g)⇌CO(g)+H2(g);△H=+131.3kJ/mol。
①该反应在_________ 下能自发进行(填“高温”或“低温”)。
②水煤气燃烧过程中产生的CO2气体可以与“84消毒液”的主要成分NaClO发生反应,该反应的离子方程式为:___________________________________________________ 。(已知:酸性HCO3-<HClO<H2CO3)
(3)已知反应:CO(g)+H2O(g)⇌CO2(g)+H2(g),现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
①实验1条件下平衡常数K=________________ (保留小数点后二位)。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是______ 。
③该反应的△H____ 0(填填“小于”,“大于”)。
(1)汽车尾气中排放的NOx和CO污染环境,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。已知:① 2CO(g)+O2(g)⇌2CO2(g) ΔH=−566.0 kJ/mol,② N2(g)+O2(g)⇌2NO(g) ΔH=+180.5 kJ/mol,③ 2NO(g)+O2(g)⇌2NO2(g) ΔH=−116.5 kJ/mol。回答下列问题:
CO的燃烧热为
(2)改变煤的利用方式可减少环境污染,通常可将煤气化转化为水煤气,其反应原理为:C(s)+H2O(g)⇌CO(g)+H2(g);△H=+131.3kJ/mol。
①该反应在
②水煤气燃烧过程中产生的CO2气体可以与“84消毒液”的主要成分NaClO发生反应,该反应的离子方程式为:
(3)已知反应:CO(g)+H2O(g)⇌CO2(g)+H2(g),现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
| 实验 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | |
| CO | H2O | H2 | |||
| 1 | 650 | 4 | 2 | 1.6 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 3 |
| 3 | 900 | a | b | c | t |
①实验1条件下平衡常数K=
②实验3中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是
③该反应的△H
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】我国含煤量和煤使用量均为全球第一,所以如何提高煤的使用效率,同时减少对环境的危害一直是我国科学家研究的重要课题。其中重要的汽化反应为:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
(1)已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ/mol;2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol,则反应CO和水蒸气反应生成CO2和H2的热化学方程式:_______ 。
(2)为提高该汽化反应的CO转化率,可采用的方法有_______(填编号)。
(3)在3L密闭容器中,将4.0 mol CO与8.0 mol H2O混合迅速加热到600℃,在600℃时跟踪测定CO的物质的量变化如图所示:
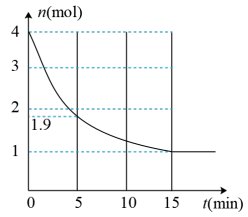
①该体系在第_______ min时达到化学平衡,从反应开始到5 min时,用CO2表示的反应速率为_______ ,600℃的平衡常数为_______ 。
②保持温度不变,15 min后向该密闭容器中再次充入3 mol CO、1 mol H2O(g)、1 mol CO2(g)、1 mol H2(g),此时平衡_______ (填“正移”、“不移”或“逆移”),其原因是_______ 。
 CO2(g)+H2(g)
CO2(g)+H2(g)(1)已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ/mol;2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol,则反应CO和水蒸气反应生成CO2和H2的热化学方程式:
(2)为提高该汽化反应的CO转化率,可采用的方法有_______(填编号)。
| A.选择适当的催化剂 | B.增大压强 |
| C.升高温度 | D.及时分离出CO2 |
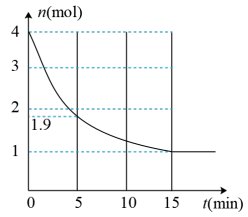
①该体系在第
②保持温度不变,15 min后向该密闭容器中再次充入3 mol CO、1 mol H2O(g)、1 mol CO2(g)、1 mol H2(g),此时平衡
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】I.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表,回答下列问题:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表,回答下列问题:
(1)该反应的化学平衡常数表达式为K=___ 。
(2)该反应为___ 反应(选填吸热、放热)。
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为___ K。
II.将气体A、B置于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。
2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。
(1)用C表示10s内反应的平均反应速率为___ 。
(2)反应前A的物质的量浓度是___ 。
(3)10s末,生成物D的浓度为____ 。
 CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表,回答下列问题:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表,回答下列问题:| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=
(2)该反应为
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
II.将气体A、B置于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)
 2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。
2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。(1)用C表示10s内反应的平均反应速率为
(2)反应前A的物质的量浓度是
(3)10s末,生成物D的浓度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】钼(Mo)是人体及动植物必须的微量元素,且在芯片制作、药物和医学造影等方面也有重要作用。用辉钼矿冶炼金属钼的某反应如下:MoS(s)+2Na2CO3(s)+4H2(g) Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)。该反应中氢气的平衡转化率与温度、压强的关系如图所示。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)。该反应中氢气的平衡转化率与温度、压强的关系如图所示。

回答下列问题:
(1)Na2S的电子式为:____ 。应物和生成物中属于极性分子的是____ (填写化学式)。举出一个事实,说明硫的非金属性比碳强(用化学方程式表示):____ 。
(2)写出上述反应的平衡常数表达式K=____ 。上述正反应是反应____ (填“吸热”或“放热”)。A、B、C三点代表的平衡状态的平衡常数的大小为:KA____ KB____ KC(填“>”“<”或“=”)。
(3)1100℃,2L恒容密闭容器中,加入0.1molMoS2、0.2molNa2CO3、0.4molH2,反应至20min时达到的平衡状态恰好处于图中的A点。此过程中,用H2表示的平均速率为____ 。其他条件一定时,B点的速率____ C点(填“大于”“等于”或“小于”),说明理由:____ 。
(4)比较H2O和H2S的热稳定性强弱,并说明理由:_____ 。
 Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)。该反应中氢气的平衡转化率与温度、压强的关系如图所示。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)。该反应中氢气的平衡转化率与温度、压强的关系如图所示。
回答下列问题:
(1)Na2S的电子式为:
(2)写出上述反应的平衡常数表达式K=
(3)1100℃,2L恒容密闭容器中,加入0.1molMoS2、0.2molNa2CO3、0.4molH2,反应至20min时达到的平衡状态恰好处于图中的A点。此过程中,用H2表示的平均速率为
(4)比较H2O和H2S的热稳定性强弱,并说明理由:
您最近一年使用:0次



