名校
解题方法
1 . 用下列实验装置进行相应实验,能达到实验目的的是
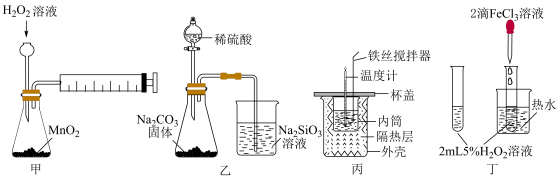

| A.用装置甲定量测定化学反应速率 |
| B.证明非金属性:S>C>Si |
| C.用装置丙准确测定中和反应的反应热 |
D.用装置丁验证 对 对 分解反应有催化作用 分解反应有催化作用 |
您最近一年使用:0次
2 . 某同学进行影响草酸溶液与高锰酸钾酸性溶液反应速率因素的研究。室温下,实验数据如下:
(1)草酸溶液与高锰酸钾酸性溶液反应的离子方程式为___________________ 。
(2)该实验结论是_______________________ 。
(3)进行上述三个实验后,该同学进行反思,认为实验①的现象可以证明上述结论。请写出实验①的现象为____________________ 。
(4)实验②选用MnSO4固体而不是MnCl2固体的原因是_________________ 。
(5)该同学拟采用如下图所示的实验方案继续探究外界条件对反应速率的影响。

a.该同学拟研究的影响因素是___________________ 。
b.你认为该同学的实验方案_______________ (填“合理”或“不合理”),理由是____________________________ 。
| 实验序号 | ① | ② | ③ |
| 加入试剂 | 4mL 0.01mol/L KMnO4 2mL 0.1mol/L H2C2O4 | 4mL 0.01mol/L KMnO4 2mL 0.1mol/L H2C2O4 少量MnSO4固体 | 4mL 0.01mol/L KMnO4 2mL 0.1mol/L H2C2O4 少量Na2SO4固体 |
| 褪色时间/s | 116 | 6 | 117 |
(2)该实验结论是
(3)进行上述三个实验后,该同学进行反思,认为实验①的现象可以证明上述结论。请写出实验①的现象为
(4)实验②选用MnSO4固体而不是MnCl2固体的原因是
(5)该同学拟采用如下图所示的实验方案继续探究外界条件对反应速率的影响。

a.该同学拟研究的影响因素是
b.你认为该同学的实验方案
您最近一年使用:0次
名校
解题方法
3 . 氮是自然界各种生物体生命活动不可缺少的重要元素。
(1)下列说法中,不正确的是___________ (填字母序号)。
a.氮原子的最外层有5个电子,氮气分子中存在氮氮三键,常温下化学性质稳定
b.氮元素位于元素周期表的第二周期,第VA族
c.氮元素的最低化合价为-3价,最高化合价为+5价
d.根据元素周期律推测,氮化硅的化学式为SiN
(2)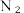 分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是
分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是 (铵根离子),将
(铵根离子),将 转化为
转化为  需与
需与___________ (填“酸”或“碱”)反应。写出该反应离子方程式:___________ 和 的电子式
的电子式___________ 。
(3)大自然通过闪电可将空气中的氮气转化为含氮化合物,从而实现自然固氮。该过程中生成的含氮化合物是___________ 。
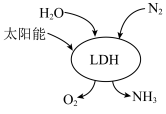
(4)我国科研团队借助一种固体催化剂(LDH),在常温常压和可见光作用下实现了人工固氮。其过程如图所示。写出该过程中反应的化学方程式:___________ 。___________ 。
(6)上述流程中,需要使用催化剂的反应是___________ (填“Ⅰ”、“Ⅱ”或“Ⅲ”),使用催化剂的目的是___________ 。
(7)工业合成氨反应为: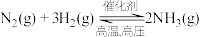 对其描述正确的是___________(填序号)。
对其描述正确的是___________(填序号)。
(8)采用上述工业制硝酸的流程,若 (已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为
(已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为___________ g。
(1)下列说法中,不正确的是
a.氮原子的最外层有5个电子,氮气分子中存在氮氮三键,常温下化学性质稳定
b.氮元素位于元素周期表的第二周期,第VA族
c.氮元素的最低化合价为-3价,最高化合价为+5价
d.根据元素周期律推测,氮化硅的化学式为SiN
(2)
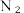 分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是
分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是 (铵根离子),将
(铵根离子),将 转化为
转化为  需与
需与 的电子式
的电子式(3)大自然通过闪电可将空气中的氮气转化为含氮化合物,从而实现自然固氮。该过程中生成的含氮化合物是
(4)我国科研团队借助一种固体催化剂(LDH),在常温常压和可见光作用下实现了人工固氮。其过程如图所示。写出该过程中反应的化学方程式:
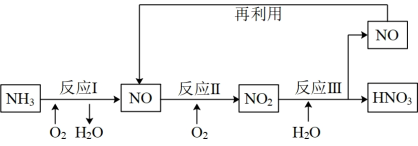
(6)上述流程中,需要使用催化剂的反应是
(7)工业合成氨反应为:
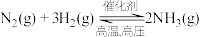 对其描述正确的是___________(填序号)。
对其描述正确的是___________(填序号)。A.在上述条件下,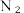 能全部转化为 能全部转化为 |
| B.若其他条件一定时,增大氮气的浓度,可增大反应速率 |
| C.达到平衡时,体系中各物质的浓度一定相等 |
| D.当正反应速率等于逆反应速率且不为零时,该反应达到平衡状态 |
(8)采用上述工业制硝酸的流程,若
 (已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为
(已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为
您最近一年使用:0次
名校
解题方法
4 . 工业上制备硫酸的一步重要反应是 在400~500℃下的催化氧化反应:
在400~500℃下的催化氧化反应:
 。下列有关说法错误的是
。下列有关说法错误的是
 在400~500℃下的催化氧化反应:
在400~500℃下的催化氧化反应:
 。下列有关说法错误的是
。下列有关说法错误的是A.常通入过量的空气,以提高 的平衡转化率 的平衡转化率 |
| B.为提高反应速率和平衡转化率,采用的压强越大越好 |
| C.控制温度为400~500℃既能提升反应速率,又能使催化剂有较高的活性 |
| D.要综合考虑影响速率与平衡的各种因素、设备条件和经济成本等,寻找适宜的生产条件 |
您最近一年使用:0次
2023-08-12更新
|
407次组卷
|
8卷引用:天津市天津中学2023-2024学年高二上学期第一次月考化学试题
天津市天津中学2023-2024学年高二上学期第一次月考化学试题河南省周口市无锡天一企业管理有限公司等2校2022-2023学年高二上学期12月期末考试化学试题山东省鄄城县第一中学2023-2024学年高二上学期9月月考化学试题黑龙江省哈尔滨市第一中学校2023-2024学年高二上学期第一次质量检测化学试题(已下线)专题05 化学反应的方向 化学反应的调控 -【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)(已下线)寒假作业04 化学反应的方向及调控-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)四川省宜宾市叙州区第二中学校2023-2024学年高二上学期12月月考化学试题安徽省六安市裕安区新安中学2023-2024学年高二下学期第一次月考化学试题
解题方法
5 . 光催化固氮合成氨的机理如图所示,下列说法不正确的是
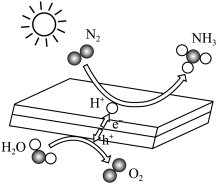

| A.NH3分子是极性分子 |
| B.此反应中氮气做氧化剂 |
| C.无论使用哪种催化剂,同一个反应的活化能是不变的 |
D.此反应的化学反应方程式是:2N2+6H2O 4NH3+3O2 4NH3+3O2 |
您最近一年使用:0次
6 . 工厂的氨氮废水可用电化学催化氧化法加以处理,其中NH3在电极表面的氧化过程的微观示意图如图:
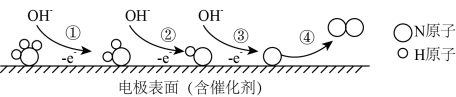
下列说法中,不正确的是

下列说法中,不正确的是
| A.过程①②均有N-H键断裂 |
B.过程③的电极反应式为: |
| C.过程④中没有非极性键形成 |
| D.催化剂可以降低该反应的活化能 |
您最近一年使用:0次
2023-01-12更新
|
208次组卷
|
2卷引用:天津市河西区新华中学2022-2023学年高二上学期期末考试化学试题
名校
7 . 一定温度下,向2L恒容密闭容器中充入1mol  (g)和3mol
(g)和3mol  (g),发生合成氨反应。10min末,测得
(g),发生合成氨反应。10min末,测得 的物质的量为1.5mol。在铁触媒催化剂的表面上合成氨反应的反应历程和能量变化如图所示,其中吸附在铁触媒表面上的物质用·标注。下列说法错误的是
的物质的量为1.5mol。在铁触媒催化剂的表面上合成氨反应的反应历程和能量变化如图所示,其中吸附在铁触媒表面上的物质用·标注。下列说法错误的是
 (g)和3mol
(g)和3mol  (g),发生合成氨反应。10min末,测得
(g),发生合成氨反应。10min末,测得 的物质的量为1.5mol。在铁触媒催化剂的表面上合成氨反应的反应历程和能量变化如图所示,其中吸附在铁触媒表面上的物质用·标注。下列说法错误的是
的物质的量为1.5mol。在铁触媒催化剂的表面上合成氨反应的反应历程和能量变化如图所示,其中吸附在铁触媒表面上的物质用·标注。下列说法错误的是
| A.催化剂能改变反应历程,影响化学反应速率 |
| B.过渡态Ⅱ比过渡态Ⅰ更稳定 |
C.10min时, |
D.0~10min内, |
您最近一年使用:0次
解题方法
8 . 乙烯氢化的化学方程式为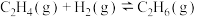
 ,使用不同含Au催化剂的反应进程如下图所示。下列说法
,使用不同含Au催化剂的反应进程如下图所示。下列说法不正确 的是
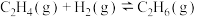
 ,使用不同含Au催化剂的反应进程如下图所示。下列说法
,使用不同含Au催化剂的反应进程如下图所示。下列说法
A.效果较好的催化剂是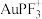 |
B.该反应的 |
| C.过渡态物质的稳定性:过渡态1>过渡态2 |
D.1mol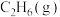 的能量小于1mol 的能量小于1mol 与1mol 与1mol 具有的能量之和 具有的能量之和 |
您最近一年使用:0次
名校
解题方法
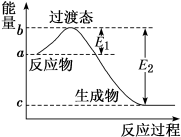
9 . 如图为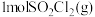 和
和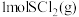 反应生成
反应生成 过程中的能量变化示意图,已知
过程中的能量变化示意图,已知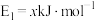 、
、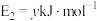 ,下列有关说法中正确的是
,下列有关说法中正确的是
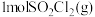 和
和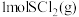 反应生成
反应生成 过程中的能量变化示意图,已知
过程中的能量变化示意图,已知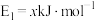 、
、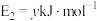 ,下列有关说法中正确的是
,下列有关说法中正确的是
| A.若在反应体系中加入催化剂,E1不变 |
| B.若在反应体系中加入催化剂,△H减小 |
C.反应的活化能等于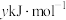 |
D.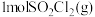 和 和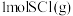 反应生成 反应生成 的 的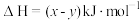 |
您最近一年使用:0次
2022-10-08更新
|
489次组卷
|
10卷引用:天津汇文中学2022-2023学年高二上学期第一次阶段性测试化学试题
天津汇文中学2022-2023学年高二上学期第一次阶段性测试化学试题天津市第二中学2022-2023学年高二上学期期中检测化学试题2017届江苏省南通市高三高考全真模拟(一)化学试卷辽宁省六校协作体2016-2017学年高一下学期期中考试化学试题吉林省延边安图第一中学2016-2017学年高二练习化学试题河北省邢台市第二中学2018届高三上学期第一次月考(开学考试)化学试题陕西省咸阳市武功县普集高中2017-2018学年高二上学期第二次月考(9月)化学试题贵州省思南中学2019-2020学年高二9月月考化学试题江苏省启东中学2020-2021学年高二上学期期初考试化学试题四川省阆中中学校2020-2021学年高一(仁智班)下学期第一次月考化学试题
解题方法
10 . Ⅰ.含硫化合物是实验室和工业上的常用化学品。请回答:
(1)实验室可用铜与浓硫酸反应制备少量 :
: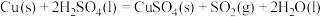
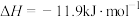 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由___________ 。
(2)已知
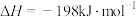 。850K时,在一恒容密闭反应器中充入一定量的
。850K时,在一恒容密闭反应器中充入一定量的 和
和 ,当反应达到平衡后测得
,当反应达到平衡后测得 、
、 和
和 的浓度分别为
的浓度分别为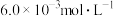 、
、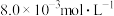 和
和 。
。
①该温度下反应的平衡常数为___________ 。
②平衡时 的转化率为
的转化率为___________ 。
(3)工业上主要采用接触法由含硫矿石制备硫酸。
①下列说法不正确的是___________ 。
A.须采用高温高压的反应条件使 氧化为
氧化为
B.进入接触室之前的气流无需净化处理
C.通入过量的空气可以提高含硫矿石和 的转化率
的转化率
D.在吸收塔中宜采用水或稀硫酸吸收 以提高吸收速率
以提高吸收速率
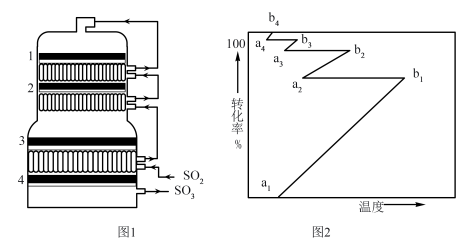
②接触室结构如图1所示,其中1~4表示催化剂层。图2所示进程中表示热交换过程的是___________ 。
A. B.
B. C.
C. D.
D. E.
E. F.
F. G.
G.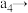
Ⅱ.一定条件下,用 、NiO或
、NiO或 作催化剂对燃煤烟气回收。反应为
作催化剂对燃煤烟气回收。反应为
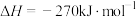 。
。
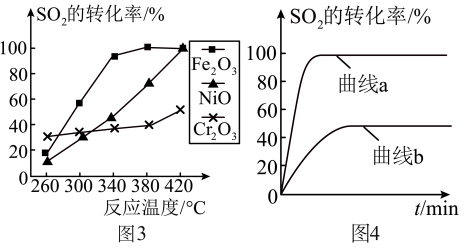
(4)其他条件相同、催化剂不同, 的转化率随反应温度的变化如图3,
的转化率随反应温度的变化如图3, 和NiO作催化剂均能使
和NiO作催化剂均能使 的转化率达到最高,不考虑催化剂价格因素,选择
的转化率达到最高,不考虑催化剂价格因素,选择 的主要优点是:
的主要优点是:___________ 。
(5)某科研小组用 作催化剂。在380℃时,分别研究了
作催化剂。在380℃时,分别研究了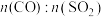 为1:1、3:1时
为1:1、3:1时 转化率的变化情况图4。则图4中表示
转化率的变化情况图4。则图4中表示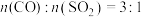 的变化曲线为
的变化曲线为___________ 。
(1)实验室可用铜与浓硫酸反应制备少量
 :
: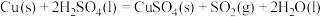
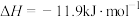 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由(2)已知

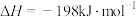 。850K时,在一恒容密闭反应器中充入一定量的
。850K时,在一恒容密闭反应器中充入一定量的 和
和 ,当反应达到平衡后测得
,当反应达到平衡后测得 、
、 和
和 的浓度分别为
的浓度分别为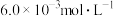 、
、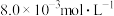 和
和 。
。①该温度下反应的平衡常数为
②平衡时
 的转化率为
的转化率为(3)工业上主要采用接触法由含硫矿石制备硫酸。
①下列说法不正确的是
A.须采用高温高压的反应条件使
 氧化为
氧化为
B.进入接触室之前的气流无需净化处理
C.通入过量的空气可以提高含硫矿石和
 的转化率
的转化率D.在吸收塔中宜采用水或稀硫酸吸收
 以提高吸收速率
以提高吸收速率②接触室结构如图1所示,其中1~4表示催化剂层。图2所示进程中表示热交换过程的是

A.
 B.
B. C.
C. D.
D. E.
E. F.
F. G.
G.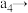
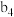
Ⅱ.一定条件下,用
 、NiO或
、NiO或 作催化剂对燃煤烟气回收。反应为
作催化剂对燃煤烟气回收。反应为
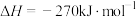 。
。(4)其他条件相同、催化剂不同,
 的转化率随反应温度的变化如图3,
的转化率随反应温度的变化如图3, 和NiO作催化剂均能使
和NiO作催化剂均能使 的转化率达到最高,不考虑催化剂价格因素,选择
的转化率达到最高,不考虑催化剂价格因素,选择 的主要优点是:
的主要优点是:(5)某科研小组用
 作催化剂。在380℃时,分别研究了
作催化剂。在380℃时,分别研究了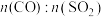 为1:1、3:1时
为1:1、3:1时 转化率的变化情况图4。则图4中表示
转化率的变化情况图4。则图4中表示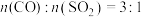 的变化曲线为
的变化曲线为
您最近一年使用:0次



