名校
1 . 用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的外界因素,离子方程式为2 +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。设计实验方案如下(KMnO4溶液已酸化):
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。设计实验方案如下(KMnO4溶液已酸化):
请回答:
(1)该实验探究的是_____________ 因素对化学反应速率的影响。
(2)请完成上述实验设计表:V1=_________ ,V2=__________ 。
(3)利用实验1中数据计算,平均反应速率:v(KMnO4)=______________________ 。
(4)小组同学发现反应速率总是如图1,其中t1~t2时间内速率变快的主要原因可能是:
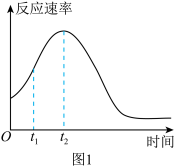
①、产物Mn2+是该反应的催化剂;②、_____________________ 。
(5)该小组同学查阅已有的实验资料发现,该实验过程中Mn2+对反应有催化作用,并继续进行实验探究。请你帮助该小组同学完成实验方案。
①所加试剂X最好选用________________
A、0.1mol/LMnCl2B、0.1mol/LMnSO4C、MnSO4粉末D、MnCl2粉末
②如果查阅资料正确,预计应观察到的现象是_______________________________ 。
 +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。设计实验方案如下(KMnO4溶液已酸化):
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。设计实验方案如下(KMnO4溶液已酸化):| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 溶液褪色至无色所需时间/min | |||
| 0.6mol/LH2C2O4溶液 | H2O | 0.1mol/LKMnO4溶液 | 3mol/LH2SO4溶液 | ||
| 1 | 3.0 | 13.0 | 2.0 | 2.0 | 8.0 |
| 2 | 2.0 | 14.0 | 2.0 | 2.0 | 10.4 |
| 3 | 1.0 | V1 | V2 | 2.0 | 12.8 |
请回答:
(1)该实验探究的是
(2)请完成上述实验设计表:V1=
(3)利用实验1中数据计算,平均反应速率:v(KMnO4)=
(4)小组同学发现反应速率总是如图1,其中t1~t2时间内速率变快的主要原因可能是:

①、产物Mn2+是该反应的催化剂;②、
(5)该小组同学查阅已有的实验资料发现,该实验过程中Mn2+对反应有催化作用,并继续进行实验探究。请你帮助该小组同学完成实验方案。
| 实验编号 | 室温下,试管中所加试剂及其用量 | 室温下溶液褪色至无色所需时间/min | ||||
| 0.6mol/LH2C2O4溶液 | H2O | 0.1mol/LKMnO4溶液 | 3mol/LH2SO4溶液 | 少量 | ||
| 4 | 3.0mL | 13.0mL | 2.0mL | 2.0mL | X | t |
①所加试剂X最好选用
A、0.1mol/LMnCl2B、0.1mol/LMnSO4C、MnSO4粉末D、MnCl2粉末
②如果查阅资料正确,预计应观察到的现象是
您最近一年使用:0次



