名校
1 . 为比较 和
和 对
对 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
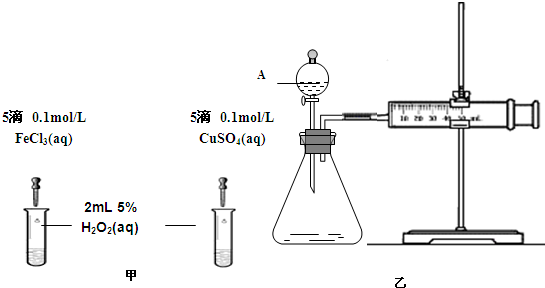
(1)定性分析:如图甲可通过观察_______ 的快慢,定性比较得出结论。有同学提出将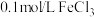 改为
改为_______  更为合理,其理由是
更为合理,其理由是_______ ;
(2)定量分析。如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是_______ ;
(3)查阅资料得知:将作为催化剂的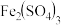 溶液加入
溶液加入 溶液后,溶液中会发生两个氧化还原反应,且两个反应中
溶液后,溶液中会发生两个氧化还原反应,且两个反应中 均参加了反应,试从
均参加了反应,试从催化剂的角度 分析,这两个氧化还原反应的离子方程式分别是: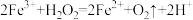 和
和_______ 。
II.欲用下图所示实验来证明 是
是 分解反应的催化剂。
分解反应的催化剂。
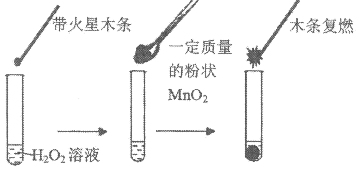
(1)该实验不能达到目的,若想证明 是催化剂还需要确认
是催化剂还需要确认_______ ;
(2)加入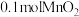 粉末于
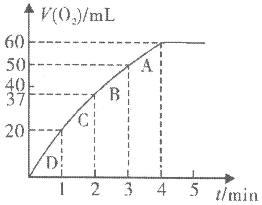
粉末于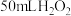 溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
①写出 在二氧化锰作用下发生反应的化学方程式
在二氧化锰作用下发生反应的化学方程式_______ ;
②A、B、C、D各点反应速率快慢的顺序为_______ >_______ >_______ >_______ 。
 和
和 对
对 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
(1)定性分析:如图甲可通过观察
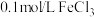 改为
改为 更为合理,其理由是
更为合理,其理由是(2)定量分析。如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是
(3)查阅资料得知:将作为催化剂的
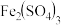 溶液加入
溶液加入 溶液后,溶液中会发生两个氧化还原反应,且两个反应中
溶液后,溶液中会发生两个氧化还原反应,且两个反应中 均参加了反应,试从
均参加了反应,试从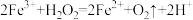 和
和II.欲用下图所示实验来证明
 是
是 分解反应的催化剂。
分解反应的催化剂。
(1)该实验不能达到目的,若想证明
 是催化剂还需要确认
是催化剂还需要确认(2)加入
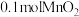 粉末于
粉末于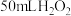 溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
①写出
 在二氧化锰作用下发生反应的化学方程式
在二氧化锰作用下发生反应的化学方程式②A、B、C、D各点反应速率快慢的顺序为
您最近一年使用:0次
名校
解题方法
2 . 草酸与高锰酸钾在酸性条件下能够发生如下反应: +H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:
+H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:
(1)该反应中氧化剂和还原剂的物质的量之比为______ 。
(2)我们可以通过观察_____ ,来判断反应速率的大小
(3)如果研究催化剂对化学反应速率的影响,使用实验______ 和_____ (用Ⅰ~Ⅳ表示,下同),如果研究温度对化学反应速率的影响,使用实验_______ 和______ (用Ⅰ~Ⅳ表示,下同)。
(4)实验Ⅰ和Ⅳ研究浓度对反应速率的影响,Ⅳ中加入1mL蒸馏水的目的是_____ 。
(5)反应I、III、IV中都可观察到反应速率先慢后快的现象,引起这种现象的原因是_____ 。
 +H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:
+H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
Ⅰ | 2 | 20 | |
Ⅱ | 2 | 20 | 5滴饱和MnSO4溶液 |
Ⅲ | 2 | 30 | |
Ⅳ | 1 | 20 | 1 mL蒸馏水 |
(2)我们可以通过观察
(3)如果研究催化剂对化学反应速率的影响,使用实验
(4)实验Ⅰ和Ⅳ研究浓度对反应速率的影响,Ⅳ中加入1mL蒸馏水的目的是
(5)反应I、III、IV中都可观察到反应速率先慢后快的现象,引起这种现象的原因是
您最近一年使用:0次
3 . 研究氨的合成和分解对工业生产和防治污染有重要意义,回答下列问题:
(1)化学键键能数据如下:
氨分解反应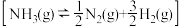 的活化能
的活化能 ,由此计算合成氨反应
,由此计算合成氨反应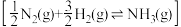 的活化能
的活化能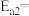
_______  。
。
(2)在Fe催化剂作用下由氮气和氢气直接合成氨的反应历程为(*表示吸附态):化学吸附: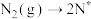 ;
;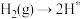 ;表面反应:
;表面反应: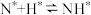 ;
; ;
; ;脱附:
;脱附: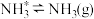 ;其中,
;其中, 的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。实际生产中,原料气中
的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。实际生产中,原料气中 和
和 物质的量之比为
物质的量之比为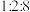 。从速率和转化率角度说明原料气中
。从速率和转化率角度说明原料气中 适度过量的理由:
适度过量的理由:
①速率角度:_______ ;
②转化率角度:_______ 。
(3)已知反应: 标准平衡常数
标准平衡常数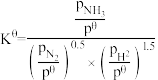 ,其中
,其中 为标准压强(
为标准压强(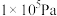 ),
),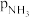 、
、 和
和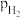 为各组分的平衡分压,如:
为各组分的平衡分压,如: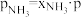 ,p为平衡总压,
,p为平衡总压,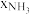 为平衡系统中
为平衡系统中 的物质的量分数。若
的物质的量分数。若 和
和 起始物质的量之比为
起始物质的量之比为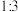 ,反应在恒定温度和标准压强下进行,
,反应在恒定温度和标准压强下进行, 的平衡转化率为
的平衡转化率为 ,则
,则
_______ (用含 的最简式表示)
的最简式表示)
(4)氨催化分解既可防治氨气污染,又能得到氢能源。在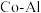 催化剂体系中,压强
催化剂体系中,压强 下氨气以一定流速通过反应器得到不同催化剂下相同时间内
下氨气以一定流速通过反应器得到不同催化剂下相同时间内 转化率随温度变化的关系如图所示。
转化率随温度变化的关系如图所示。

使活化能最小的催化剂为_______ ;温度一定时,如果增大气体流速,则b点对应的点可能是____ (填“a”“c”“d”“e”或“f”)。
(1)化学键键能数据如下:
| 化学键 | H—H | N≡N | N—H |
 | 436 | 946 | 391 |
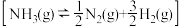 的活化能
的活化能 ,由此计算合成氨反应
,由此计算合成氨反应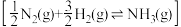 的活化能
的活化能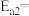
 。
。(2)在Fe催化剂作用下由氮气和氢气直接合成氨的反应历程为(*表示吸附态):化学吸附:
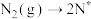 ;
;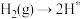 ;表面反应:
;表面反应: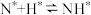 ;
; ;
; ;脱附:
;脱附: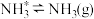 ;其中,
;其中, 的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。实际生产中,原料气中
的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。实际生产中,原料气中 和
和 物质的量之比为
物质的量之比为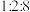 。从速率和转化率角度说明原料气中
。从速率和转化率角度说明原料气中 适度过量的理由:
适度过量的理由:①速率角度:
②转化率角度:
(3)已知反应:
 标准平衡常数
标准平衡常数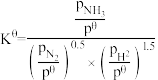 ,其中
,其中 为标准压强(
为标准压强(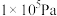 ),
),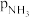 、
、 和
和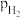 为各组分的平衡分压,如:
为各组分的平衡分压,如: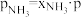 ,p为平衡总压,
,p为平衡总压,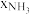 为平衡系统中
为平衡系统中 的物质的量分数。若
的物质的量分数。若 和
和 起始物质的量之比为
起始物质的量之比为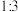 ,反应在恒定温度和标准压强下进行,
,反应在恒定温度和标准压强下进行, 的平衡转化率为
的平衡转化率为 ,则
,则
 的最简式表示)
的最简式表示)(4)氨催化分解既可防治氨气污染,又能得到氢能源。在
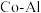 催化剂体系中,压强
催化剂体系中,压强 下氨气以一定流速通过反应器得到不同催化剂下相同时间内
下氨气以一定流速通过反应器得到不同催化剂下相同时间内 转化率随温度变化的关系如图所示。
转化率随温度变化的关系如图所示。
使活化能最小的催化剂为
您最近一年使用:0次
2020-12-20更新
|
337次组卷
|
2卷引用:湖南省长沙市长郡中学、师大附中、长沙市一中联考联合体2021届高三12月联考化学试题
名校
解题方法
4 . 实验一:已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O,甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。
设计如下(所取溶液体积均为10mL):
(1)其他条件不变时:探究温度对化学反应速率的影响,应选择实验____________ (填实验编号);若同时选择实验①、实验②、实验③,测定混合液变浑浊的时间,可探究______________ 对化学反应速率的影响。
实验二:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,乙同学通过室温下溶液颜色褪至无色所需时间,研究外界条件对化学反应速率的影响。
【实验内容及记录】
请回答:
(2)表中V1=___________ ,V2=___________ 。
(3)利用实验1中数据计算,若用KMnO4的浓度变化表示的反应速率为:υ(KMnO4)=________________________ 。
(4)在开始一段时间内,反应速率较小,溶液褪色不明显;但不久突然褪色,反应速率明显增大。针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率增大。从影响化学反应速率的因素看,你猜想还可能是______________________ 的影响。
(5)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入______________ (填字母序号)。
A.硫酸钾B.硫酸锰C.氯化锰D.水
设计如下(所取溶液体积均为10mL):
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/(mol·L-1) | c(H2SO4)/(mol·L-1) |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
实验二:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,乙同学通过室温下溶液颜色褪至无色所需时间,研究外界条件对化学反应速率的影响。
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6mol/LH2C2O4溶液 | H2O | 3mol/L稀硫酸 | 0.05mol/LKMnO4溶液 | ||
| 1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
| 2 | 2.0 | 3.0 | 2.0 | V1 | 2.7 |
| 3 | 1.0 | V2 | 2.0 | 3.0 | 3.9 |
(2)表中V1=
(3)利用实验1中数据计算,若用KMnO4的浓度变化表示的反应速率为:υ(KMnO4)=
(4)在开始一段时间内,反应速率较小,溶液褪色不明显;但不久突然褪色,反应速率明显增大。针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率增大。从影响化学反应速率的因素看,你猜想还可能是
(5)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入
A.硫酸钾B.硫酸锰C.氯化锰D.水
您最近一年使用:0次
2020-11-26更新
|
304次组卷
|
5卷引用:福建省漳州市平和县第一中学2020-2021学年高二上学期期中考试化学试题
名校
解题方法
5 . 铁及铁的氧化物广泛应于生产、生活、航天、科研领域。
(1)Fe2O3与CH4反应可制备“纳米级”金属铁,其反应为:3 CH4(g)+Fe2O3(s) Fe(s)+6H2(g)+3CO(g) ΔH
Fe(s)+6H2(g)+3CO(g) ΔH
①在容积均为VL的Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中加入足量“纳米级”金属铁,然后分别充入amolCO和2amolH2,三个容器的反应温度分别保持T1、T2、T3,在其它条件相同的情况下,实验测得反应均进行到tmin时CO的体积分数如图1所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定处于化学平衡状态的是____ (填Ⅰ、Ⅱ、Ⅲ);制备“纳米级”金属铁的反应:ΔH______ 0(填“>”“<”)
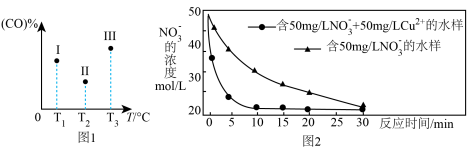
②在T℃时,向某恒容密闭容器中加入3molCH4(g)和2molFe2O3(s),进行上述反应,反应起始时压强为P0,反应进行至10min时达到平衡,测得此时容器的气体压强是起始压强的2倍。T℃下该反应的KP=_______ ;T℃下若起始时该容器中加入2molCH4(g)、4molFe2O3(s)、1molFe(s)、2molH2(g)、2molCO(g),则起始时v(正)_____ v(逆)(填“>”“<”或“=”)
(2)纳米铁粉与水中NO 反应的离子方程式为4Fe+NO
反应的离子方程式为4Fe+NO +10H+=4Fe2++NH
+10H+=4Fe2++NH +3H2O
+3H2O
①研究发现,若pH偏低将会导致NO 的去除率下降,其原因是
的去除率下降,其原因是___ 。
②相同条件下,纳米铁粉去除不同水样中NO 的速率有较大差异,图2中所产生的差异的可能原因是
的速率有较大差异,图2中所产生的差异的可能原因是 ____________ 。(答一条)
(1)Fe2O3与CH4反应可制备“纳米级”金属铁,其反应为:3 CH4(g)+Fe2O3(s)
 Fe(s)+6H2(g)+3CO(g) ΔH
Fe(s)+6H2(g)+3CO(g) ΔH①在容积均为VL的Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中加入足量“纳米级”金属铁,然后分别充入amolCO和2amolH2,三个容器的反应温度分别保持T1、T2、T3,在其它条件相同的情况下,实验测得反应均进行到tmin时CO的体积分数如图1所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定处于化学平衡状态的是

②在T℃时,向某恒容密闭容器中加入3molCH4(g)和2molFe2O3(s),进行上述反应,反应起始时压强为P0,反应进行至10min时达到平衡,测得此时容器的气体压强是起始压强的2倍。T℃下该反应的KP=
(2)纳米铁粉与水中NO
 反应的离子方程式为4Fe+NO
反应的离子方程式为4Fe+NO +10H+=4Fe2++NH
+10H+=4Fe2++NH +3H2O
+3H2O①研究发现,若pH偏低将会导致NO
 的去除率下降,其原因是
的去除率下降,其原因是②相同条件下,纳米铁粉去除不同水样中NO
 的速率有较大差异,图2中所产生的差异的可能原因是
的速率有较大差异,图2中所产生的差异的可能原因是
您最近一年使用:0次
名校
解题方法
6 . 某小组利用H2C2O4溶液与用硫酸酸化的KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时。该小组设计了如下的方案。
(1)a=_______ ,该实验是通过____________________ 来判断反应的快慢。
(2)探究温度对化学反应速率影响的实验编号是_______ 和_______ (填编号,下同),可探究H2C2O4浓度对化学反应速率影响的实验编号是_______ 和_______ 。
(3)该小组发现室温下反应速率走势如右图,其中t1~t2时间内速率变快的主要原因可能是:_______ ,若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是_______ (填序号)

A.硫酸钾 B.硫酸锰 C.稀硫酸 D.氯化锰
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 蒸馏水 体积/ml | 温度/℃ | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | |||
| ① | 0.50 | 6.0 | 0.010 | 4.0 | 0 | 25 |
| ② | 0.50 | 3.0 | 0.010 | 4.0 | a | 25 |
| ③ | 0.50 | 6.0 | 0.010 | 4.0 | 0 | 50 |
(2)探究温度对化学反应速率影响的实验编号是
(3)该小组发现室温下反应速率走势如右图,其中t1~t2时间内速率变快的主要原因可能是:

A.硫酸钾 B.硫酸锰 C.稀硫酸 D.氯化锰
您最近一年使用:0次
7 . 一种利用含硫物质的热化学循环来实现能量的转化与存储的构想如图所示:
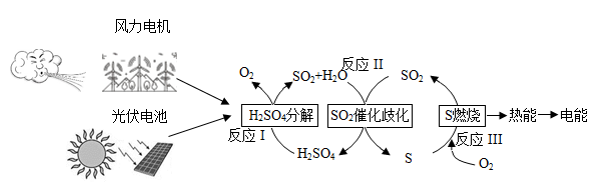
回答下列问题:
(1)举出图中两种形式的能量转化:________ 、________ 。
(2)反应I的化学方程式为_________ 。
(3)研究表明,I-可以作为水溶液中SO2歧化反应的催化剂,催化过程如下:
i.________ (请补充完整);
ii. I2+2H2O+SO2=4H++SO +2I-。
+2I-。
(4)SO2歧化反应速率与i、ii反应速率有一定关系,某同学设计实验如下:分别将18 mL SO2饱和溶液加入到2mL下列试剂中,密闭放置观察现象。
已知:I2易溶解在KI溶液中。
①B是A的对比实验,a=_______ ;A、B对比实验说明________ ;A、C对比实验说明________ 。
②实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:________ 。
(5)已知原子利用率是指目标产物中某原子的总质量与反应物中某原子的总质量之比。反应Ⅱ若目标产物是H2SO4,则硫原子利用率为________ %(结果保留三位有效数字)。

回答下列问题:
(1)举出图中两种形式的能量转化:
(2)反应I的化学方程式为
(3)研究表明,I-可以作为水溶液中SO2歧化反应的催化剂,催化过程如下:
i.
ii. I2+2H2O+SO2=4H++SO
 +2I-。
+2I-。(4)SO2歧化反应速率与i、ii反应速率有一定关系,某同学设计实验如下:分别将18 mL SO2饱和溶液加入到2mL下列试剂中,密闭放置观察现象。
| 序号 | A | B | C | D |
| 试剂组成 | 0.4 mol•L-1的KI | a mol•L-1的KI 0.2 mol•L-1的H2SO4混合物 | 0.2 mol•L-1的H2SO4 | 0.2 mol•L-1的KI和0.0002 mol I2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
①B是A的对比实验,a=
②实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:
(5)已知原子利用率是指目标产物中某原子的总质量与反应物中某原子的总质量之比。反应Ⅱ若目标产物是H2SO4,则硫原子利用率为
您最近一年使用:0次
2020-11-10更新
|
112次组卷
|
2卷引用:湖南河北联考2021届2020-2021学年高三新高考10月质量检测化学试题
名校
解题方法
8 . 某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(1)通过实验A、B,可探究出________ (填外部因素)的改变对化学反应速率的影响,其中V1=________ ;通过实验________ (填实验序号)可探究出温度变化对化学反应速率的影响。
(2)若t1<8,则由此实验可以得出的结论是__________________________ ;
(3)该小组的一位同学通过查阅资料发现,上述实验过程中n(Mn2+)随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对KMnO4与草酸之间的反应有某种特殊作用,则该作用是__________ ,相应的粒子最可能是________ (填粒子符号)。

| 实验序号 | 实验温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
| 酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/ mol·L-1 | V mL | c/ mol·L-1 | V/mL | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(2)若t1<8,则由此实验可以得出的结论是
(3)该小组的一位同学通过查阅资料发现,上述实验过程中n(Mn2+)随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对KMnO4与草酸之间的反应有某种特殊作用,则该作用是

您最近一年使用:0次
解题方法
9 . 为比较Fe3+、Cu2+和MnO2对H2O2分解反应的催化效果,某化学研究小组的同学分别设计了如图甲、乙、丙所示的实验。请回答相关问题:
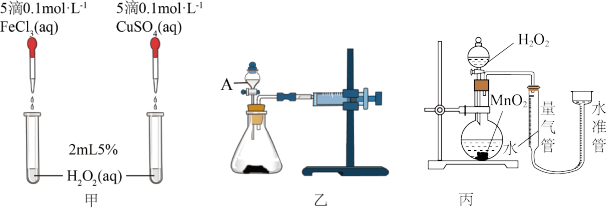
(1)同学X观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果。其结论________ (填“合理”或“不合理”)。理由是_______ 。
(2)同学Y利用乙装置,测定相同时间内产生气体的体积,从而探究Fe3+和Cu2+对H2O2分解的催化效果。试回答下列问题:
① 仪器A的名称是________ 。
② 除了必要的试剂和图乙所示的仪器外,还有一样不能缺少的实验用品是___________ 。
③ 实验时组装好装置乙,关闭A的活塞,将注射器活塞向外拉出一段。这一操作的实验目的是_________ 。
(3)同学Z利用丙装置探究MnO2对H2O2分解的催化效果。将50 mL 双氧水一次性加入盛有0.10 mol MnO2粉末的烧瓶中,测得标准状况下由量气管读出气体的体积[V(量气管)]和时间(t/min)的关系如图所示。
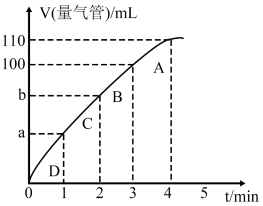
图中 b________ (填“大于”、“小于”或“等于”)90 mL

(1)同学X观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果。其结论
(2)同学Y利用乙装置,测定相同时间内产生气体的体积,从而探究Fe3+和Cu2+对H2O2分解的催化效果。试回答下列问题:
① 仪器A的名称是
② 除了必要的试剂和图乙所示的仪器外,还有一样不能缺少的实验用品是
③ 实验时组装好装置乙,关闭A的活塞,将注射器活塞向外拉出一段。这一操作的实验目的是
(3)同学Z利用丙装置探究MnO2对H2O2分解的催化效果。将50 mL 双氧水一次性加入盛有0.10 mol MnO2粉末的烧瓶中,测得标准状况下由量气管读出气体的体积[V(量气管)]和时间(t/min)的关系如图所示。

图中 b
您最近一年使用:0次
名校
解题方法
10 . 某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
请回答:
(1)根据上表中的实验数据,可以得到的结论是___________________________________ 。
(2)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率v(KMnO4)=_____________________ 。
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图甲所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图乙所示。该小组同学根据图乙所示信息提出了新的假设,并继续进行实验探究。______________________________ 。
②请你帮助该小组同学完成实验方案,并填写表中空白。
③若该小组同学提出的假设成立,应观察到的现象是_____________________________ 。
【实验原理】2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液 颜色褪至无色 所需时间/min | |||
| 0.6 mol · L-1 H2C2O4溶液 | H2O | 0.2 mol · L-1 KMnO4溶液 | 3 mol · L-1 稀硫酸 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
(1)根据上表中的实验数据,可以得到的结论是
(2)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率v(KMnO4)=
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图甲所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图乙所示。该小组同学根据图乙所示信息提出了新的假设,并继续进行实验探究。
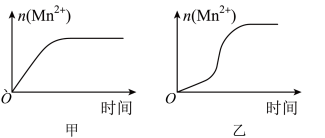
②请你帮助该小组同学完成实验方案,并填写表中空白。
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6mol/LH2C2O4溶液 | H2O | 0.2mol/LKMnO4溶液 | 3mol/L稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | t | |
③若该小组同学提出的假设成立,应观察到的现象是
您最近一年使用:0次
2020-10-12更新
|
154次组卷
|
11卷引用:湖南省醴陵二中、醴陵四中2017-2018学年高二上学期期中联考化学试题
湖南省醴陵二中、醴陵四中2017-2018学年高二上学期期中联考化学试题(已下线)2012-2013学年安徽省宿松县复兴中学高二第一次月考化学试卷【全国百强校】山东省济南外国语学校三箭分校2018-2019学年高二上学期期中考试化学试题河南省郑州市高新区一中2019-2020学年高二上学期期中考试化学试题高一必修第二册(人教2019版)第六章 第二节 化学反应的速率与限度 课时1 化学反应的速率山东省济宁市曲阜市第一中学2020-2021学年高二上学期阶段性检测(9月月考)化学试题安徽省黄山市屯溪第一中学、中科大附中2020-2021学年高一下学期期中联考化学试题黑龙江省哈尔滨市宾县一中2020-2021学年高一下学期第二次月考化学试题(已下线)考点33 物质的定性与定量分析-备战2022年高考化学一轮复习考点帮(浙江专用)福建省福州重点中学2022-2023学年高一下学期期中考试化学试题河南省南阳市邓州市第一高级中学校2023-2024学年高一下学期第一次月考化学试题B卷



