解题方法
1 . 我国在政府工作报告中提出力争于2030年前做到碳达峰,2060年前实现碳中和。因此,研发二氧化碳转化利用技术,成为当下研究热点。
 .
. 与
与 重整是
重整是 再利用的研究热点之一。该重整反应体系主要涉及以下反应:
再利用的研究热点之一。该重整反应体系主要涉及以下反应:
①

②
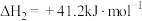
③
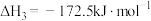
(1)已知反应①低温无法自发进行,只能在高温下自发进行,则
___________ 0(填“>”或“<”)。
(2)某温度下,在体积 的密闭容器中加入
的密闭容器中加入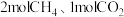 及催化剂仅发生反应①,经过
及催化剂仅发生反应①,经过 达到平衡状态时
达到平衡状态时 的转化率为
的转化率为 。则用
。则用 表示的平均化学反应速率为
表示的平均化学反应速率为___________ ,平衡常数的值为___________ ;达到平衡后,其他条件不变时向容器中充入 与
与 各
各 ,则化学平衡
,则化学平衡___________ 移动(选填“正向”、“逆向”或“不”)。
(3) 下,将
下,将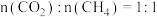 的混合气体置于密闭容器中,不同温度下重整体系中
的混合气体置于密闭容器中,不同温度下重整体系中 和
和 的平衡转化率如图所示。
的平衡转化率如图所示。 时
时 的平衡转化率远大于
的平衡转化率远大于 时
时 的平衡转化率。原因是
的平衡转化率。原因是___________ 。 .
. 在催化剂作用下,通过电催化还原为
在催化剂作用下,通过电催化还原为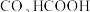 是一种具有前景的利用
是一种具有前景的利用 的方式。在催化剂表面,
的方式。在催化剂表面, 还原生成
还原生成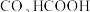 通过两种平行的反应途径进行,各自途径的关键中间体分别为
通过两种平行的反应途径进行,各自途径的关键中间体分别为 。催化剂催化
。催化剂催化 转化为
转化为 和
和 的反应历程如图1(*表示吸附在催化剂表面)。
的反应历程如图1(*表示吸附在催化剂表面)。 催化剂表面更利于生成
催化剂表面更利于生成___________ 。
(5)在m和n两种催化剂作用下,反应①的阿伦尼乌斯经验公式实验数据如图2所示,已知阿伦尼乌斯经验公式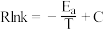 (
( 为活化能,k为速率常数,R和C为常数),m和n两种催化剂中对该反应催化效果较高的是
为活化能,k为速率常数,R和C为常数),m和n两种催化剂中对该反应催化效果较高的是___________ (填“m”或“n”)。
 .
. 与
与 重整是
重整是 再利用的研究热点之一。该重整反应体系主要涉及以下反应:
再利用的研究热点之一。该重整反应体系主要涉及以下反应:①


②

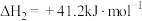
③

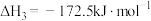
(1)已知反应①低温无法自发进行,只能在高温下自发进行,则

(2)某温度下,在体积
 的密闭容器中加入
的密闭容器中加入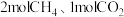 及催化剂仅发生反应①,经过
及催化剂仅发生反应①,经过 达到平衡状态时
达到平衡状态时 的转化率为
的转化率为 。则用
。则用 表示的平均化学反应速率为
表示的平均化学反应速率为 与
与 各
各 ,则化学平衡
,则化学平衡(3)
 下,将
下,将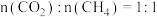 的混合气体置于密闭容器中,不同温度下重整体系中
的混合气体置于密闭容器中,不同温度下重整体系中 和
和 的平衡转化率如图所示。
的平衡转化率如图所示。 时
时 的平衡转化率远大于
的平衡转化率远大于 时
时 的平衡转化率。原因是
的平衡转化率。原因是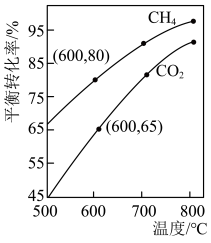
 .
. 在催化剂作用下,通过电催化还原为
在催化剂作用下,通过电催化还原为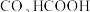 是一种具有前景的利用
是一种具有前景的利用 的方式。在催化剂表面,
的方式。在催化剂表面, 还原生成
还原生成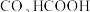 通过两种平行的反应途径进行,各自途径的关键中间体分别为
通过两种平行的反应途径进行,各自途径的关键中间体分别为 。催化剂催化
。催化剂催化 转化为
转化为 和
和 的反应历程如图1(*表示吸附在催化剂表面)。
的反应历程如图1(*表示吸附在催化剂表面)。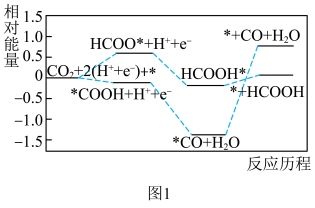
 催化剂表面更利于生成
催化剂表面更利于生成(5)在m和n两种催化剂作用下,反应①的阿伦尼乌斯经验公式实验数据如图2所示,已知阿伦尼乌斯经验公式
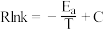 (
( 为活化能,k为速率常数,R和C为常数),m和n两种催化剂中对该反应催化效果较高的是
为活化能,k为速率常数,R和C为常数),m和n两种催化剂中对该反应催化效果较高的是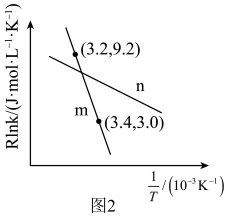
您最近一年使用:0次
2 . 在一定体积下,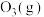 分解时相关物质的相对能量与反应历程关系如图所示[已知
分解时相关物质的相对能量与反应历程关系如图所示[已知 和
和 的相对能量为0]。下列说法错误的是
的相对能量为0]。下列说法错误的是
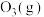 分解时相关物质的相对能量与反应历程关系如图所示[已知
分解时相关物质的相对能量与反应历程关系如图所示[已知 和
和 的相对能量为0]。下列说法错误的是
的相对能量为0]。下列说法错误的是
A.根据图像可知: |
B.形成1molCl―Cl键时释放的能量为 |
C. 的平衡转化率:历程Ⅰ=历程Ⅱ 的平衡转化率:历程Ⅰ=历程Ⅱ |
D.历程Ⅱ中快反应的热化学方程式为 , , |
您最近一年使用:0次
名校
3 .  溶液和
溶液和 溶液可发生反应:
溶液可发生反应: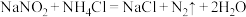 。为探究反应速率v与
。为探究反应速率v与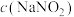 的关系,进行如下实验:常温常压下,向锥形瓶中加入一定体积V的
的关系,进行如下实验:常温常压下,向锥形瓶中加入一定体积V的
 溶液、
溶液、 溶液和水,充分搅拌,无明显现象。控制体系温度,通过分液漏斗向锥形瓶中加入
溶液和水,充分搅拌,无明显现象。控制体系温度,通过分液漏斗向锥形瓶中加入 醋酸。当导管口气泡均匀稳定冒出时,用排水法收集气体。用秒表测量收集1.0mL
醋酸。当导管口气泡均匀稳定冒出时,用排水法收集气体。用秒表测量收集1.0mL 所需时间t。实验数据如下表。下列说法正确的
所需时间t。实验数据如下表。下列说法正确的
 溶液和
溶液和 溶液可发生反应:
溶液可发生反应: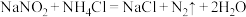 。为探究反应速率v与
。为探究反应速率v与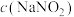 的关系,进行如下实验:常温常压下,向锥形瓶中加入一定体积V的
的关系,进行如下实验:常温常压下,向锥形瓶中加入一定体积V的
 溶液、
溶液、 溶液和水,充分搅拌,无明显现象。控制体系温度,通过分液漏斗向锥形瓶中加入
溶液和水,充分搅拌,无明显现象。控制体系温度,通过分液漏斗向锥形瓶中加入 醋酸。当导管口气泡均匀稳定冒出时,用排水法收集气体。用秒表测量收集1.0mL
醋酸。当导管口气泡均匀稳定冒出时,用排水法收集气体。用秒表测量收集1.0mL 所需时间t。实验数据如下表。下列说法正确的
所需时间t。实验数据如下表。下列说法正确的V/mL | t/s | ||||
|
| 醋酸 | 水 | ||
1 | 4.0 |
| 4.0 | 8.0 | 334 |
2 |
| 4.0 | 4.0 |
| 150 |
3 | 8.0 | 4.0 | 4.0 | 4.0 | 83 |
4 | 12.0 | 4.0 | 4.0 | 0.0 | 38 |
A.实验3中,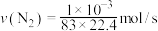 |
B.若实验4反应从开始到结束历时bs,则整个过程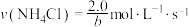 |
C. ;若 ;若 ,则 ,则 |
| D.醋酸可能作该反应的催化剂,且不改变反应历程 |
您最近一年使用:0次
解题方法
4 . 下图为 分子在催化剂作用下发生一系列转化的示意图,下列叙述正确的是
分子在催化剂作用下发生一系列转化的示意图,下列叙述正确的是
 分子在催化剂作用下发生一系列转化的示意图,下列叙述正确的是
分子在催化剂作用下发生一系列转化的示意图,下列叙述正确的是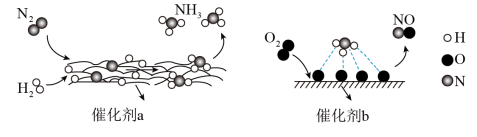
| A.催化剂a、b表面均发生了极性共价键的断裂 |
B. 分子和 分子和 分子的中心原子杂化类型不同 分子的中心原子杂化类型不同 |
C.若 键能是a kJ·mol 键能是a kJ·mol  键能是b kJ·mol 键能是b kJ·mol , , 键能是c kJ·mol 键能是c kJ·mol ,则每生成2 mol ,则每生成2 mol ,放出 ,放出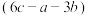 kJ热量 kJ热量 |
| D.在催化剂b作用下发生转化得到的两种生成物,均为直线形分子 |
您最近一年使用:0次
名校
5 . 利用下列实验装置能完成相应实验的是
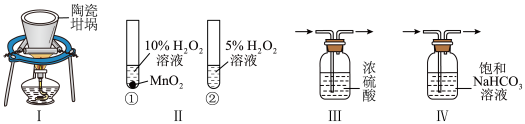
| A.图Ⅰ:熔化NaOH | B.图Ⅱ:探究催化剂对反应速率的影响 |
| C.图Ⅲ:干燥二氧化硫 | D.图Ⅳ:用装置除去Cl2中混有的HCl气体 |
您最近一年使用:0次
解题方法
6 . 采用可再生的生物质原料生产乙醇,再脱水制乙烯的技术是调整能源结构、减少环境污染、促进国民经济的重要途径之一、一定温度下,在某密闭容器中进行乙醇脱水制乙烯的反应: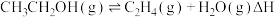 ,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是
,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是
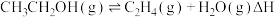 ,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是
,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是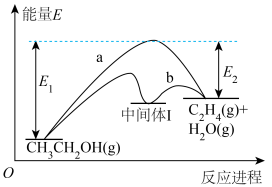
A.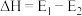 |
B.在 路径中,乙醇 路径中,乙醇 中间体Ⅰ为反应的决速步骤 中间体Ⅰ为反应的决速步骤 |
C.b路径的反应速率大于 路径的 路径的 |
D.反应达到平衡后, 路径中 路径中 的产率比 的产率比 路径的高 路径的高 |
您最近一年使用:0次
名校
解题方法
7 . 氮及其化合物的转化过程如图所示。下列分析不合理的是
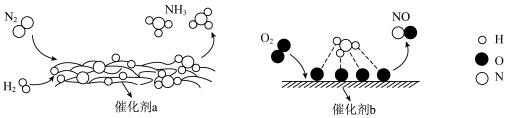
| A.催化剂a表面发生了极性共价键的断裂和形成 |
B. 与 与 反应生成 反应生成 的原子利用率(期望产物的总质量与生成物的总质量之比)为100% 的原子利用率(期望产物的总质量与生成物的总质量之比)为100% |
| C.在催化剂b表面形成氮氧键时,涉及电子转移 |
| D.使用催化剂a、b均可以提高单位时间内生成物的产量 |
您最近一年使用:0次
名校
8 . 图中展示的是乙烯催化氧化的过程(部分相关离子未画出),下列描述正确的是
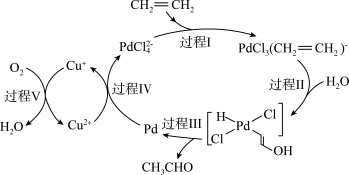
A.乙烯催化氧化反应的化学方程式为 |
B.反应中只有 作催化剂 作催化剂 |
| C.该转化过程中,没有极性键的断裂与形成 |
D.该转化过程中,涉及反应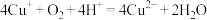 |
您最近一年使用:0次
2024-04-10更新
|
287次组卷
|
2卷引用:四川省巴中中学2023-2024学年高二下学期3月月考化学试题
名校
9 . 下列事实能用勒夏特列原理来解释的是
A.实验室采用排饱和食盐水的方法收集氯气: |
B.500℃温度比室温更有利于合成氨反应:  |
C.H2、I2、HI平衡混合气体加压后颜色加深: |
D.SO2被氧化为SO3,往往需要使用催化剂: |
您最近一年使用:0次
名校
10 . 在2L恒容密闭容器中投入4molA、2molB和催化剂,发生反应:2A(g)+B(g) 4C(g) △H>0,在不同温度下测得A的物质的量与时间t的关系如表所示。
4C(g) △H>0,在不同温度下测得A的物质的量与时间t的关系如表所示。
下列说法不正确的是
 4C(g) △H>0,在不同温度下测得A的物质的量与时间t的关系如表所示。
4C(g) △H>0,在不同温度下测得A的物质的量与时间t的关系如表所示。| t/min T/K | 0 | 4 | 8 | 12 | 16 |
| T1 | 4.0 | 3.3 | 2.8 | 2.5 | 2.4 |
| T2 | 4.0 | 3.2 | 2.6 | 2.6 | 2.6 |
| A.反应的温度:T1>T2 |
| B.T2温度下,催化剂活性更高 |
| C.T1温度下,到16min时,反应已达到平衡状态 |
| D.T2温度下,4~8min内,v(C)=0.15mol•L-1•min-1 |
您最近一年使用:0次
2024-03-10更新
|
56次组卷
|
2卷引用:四川省绵阳中学2023-2024学年高二下学期开学化学试题






