名校
1 . 2020年9月,习近平主席在第75届联合国大会提出我国要实现2030年前碳达峰、2060年前碳中和的目标。因此CO2的捕集、利用与封存成为科学家研究的重要课题。
I.研究表明CO2与CH4在催化剂存在下可发生反应制得合成气:CO2(g)+CH4(g)⇌2CO(g)+2H2(g) ∆H
(1)一定压强下,由最稳定单质生成1mol化合物的焓变为该物质的摩尔生成焓。已知CO2(g)、CH4(g)、CO(g)的摩尔生成焓分别为-395kJ·mol-1、-74.9kJ·mol-1、-110.4kJ·mol-1则上述反应的∆H=_______ kJ·mol-1
(2)此反应的活化能Ea(正)_______ Ea(逆)(填“>”、“=”或“<”),利于反应自发进行的条件是_______ (填“高温”或“低温”)。
(3)一定温度下,向一恒容密闭容器中充入CO2和CH4发生上述反应,初始时CO2和CH4的分压分别为14kPa、16kPa,一段时间达到平衡后,测得体系压强是起始时的1.4倍,则该反应的平衡常数Kp=_______ (kPa)2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
II.CO2和H2合成甲烷也是CO2资源化利用的重要方法。对于反应CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g) ∆H=-165kJ·mol-1,催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如图所示。
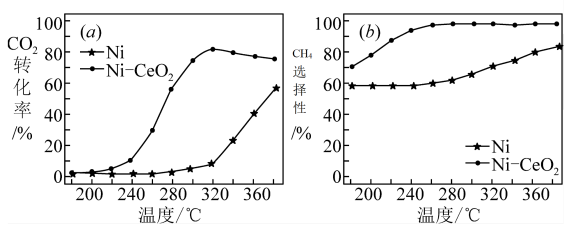
(4)高于320℃后,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是_______ 。
(5)对比上述两种催化剂的催化性能,工业上应选择的催化剂是_______ ,使用的合适温度为_______ 。
I.研究表明CO2与CH4在催化剂存在下可发生反应制得合成气:CO2(g)+CH4(g)⇌2CO(g)+2H2(g) ∆H
(1)一定压强下,由最稳定单质生成1mol化合物的焓变为该物质的摩尔生成焓。已知CO2(g)、CH4(g)、CO(g)的摩尔生成焓分别为-395kJ·mol-1、-74.9kJ·mol-1、-110.4kJ·mol-1则上述反应的∆H=
(2)此反应的活化能Ea(正)
(3)一定温度下,向一恒容密闭容器中充入CO2和CH4发生上述反应,初始时CO2和CH4的分压分别为14kPa、16kPa,一段时间达到平衡后,测得体系压强是起始时的1.4倍,则该反应的平衡常数Kp=
II.CO2和H2合成甲烷也是CO2资源化利用的重要方法。对于反应CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g) ∆H=-165kJ·mol-1,催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如图所示。

(4)高于320℃后,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是
(5)对比上述两种催化剂的催化性能,工业上应选择的催化剂是
您最近一年使用:0次
2021-06-05更新
|
420次组卷
|
3卷引用:河北省秦皇岛市青龙一中2021届高三高考适应性考试化学试题
名校
解题方法
2 . NiSO4·nH2O易溶于水,难溶于乙醇,其水溶液显酸性。从电镀污泥中回收制备NiSO4·nH2O和其它金属的工艺流程如下。
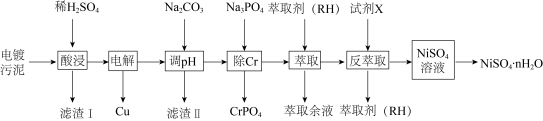
已知:Ⅰ.电镀污泥含有Cu(OH)2、Ni(OH)2、Fe(OH)3、Cr(OH)3和SiO2等。
Ⅱ.萃取剂(RH)萃取Ni2+的原理为Ni2++2RH2 NiR2+2H+。
NiR2+2H+。
回答下列问题:
(1)“酸浸”时,为加快浸出速率,提高生产效益,下列措施不合理的有___________ (填标号)。
A.用机械搅拌器搅拌 B.体积不变增加硫酸的浓度 C.进一步球磨粉碎
(2)“电解”时,铜的电解电压较低,且电解速率很快,铁和铬存在形式随电解电压的变化如下表。为得到纯的NiSO4·nH2O,电解电压的范围应选择___________ V。
(3)萃取余液可在___________ 中循环利用(填操作单元),反萃取剂X为___________ (填化学式)。
(4)“反萃取”得到的NiSO4溶液,可在强碱溶液中被NaClO氧化,得到用作镍镉电池正极材料的NiOOH。该反应的离子方程式为___________ 。NiSO4溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥等多步操作可得NiSO4·nH2O。下列说法正确的是___________ (填标号)。
A.为得到较大NiSO4·nH2O晶体颗粒,宜用冰水快速冷却结晶
B.蒸发浓缩至溶液表面出现晶膜时,停止加热
C.可通过抽滤提高过滤速度,在80℃鼓风干燥,快速得到干燥晶体
D.向冷却结晶后的固液混合物中加入乙醇可提高产率
(5)采用热重分析法测定NiSO4·nH2O样品所含结晶水数。将样品在900℃下进行煅烧,失重率随时间变化如下图,A点时失掉2个结晶水,n的值为___________ ;C点产物的化学式为___________ 。


已知:Ⅰ.电镀污泥含有Cu(OH)2、Ni(OH)2、Fe(OH)3、Cr(OH)3和SiO2等。
Ⅱ.萃取剂(RH)萃取Ni2+的原理为Ni2++2RH2
 NiR2+2H+。
NiR2+2H+。回答下列问题:
(1)“酸浸”时,为加快浸出速率,提高生产效益,下列措施不合理的有
A.用机械搅拌器搅拌 B.体积不变增加硫酸的浓度 C.进一步球磨粉碎
(2)“电解”时,铜的电解电压较低,且电解速率很快,铁和铬存在形式随电解电压的变化如下表。为得到纯的NiSO4·nH2O,电解电压的范围应选择
| 电解电压/V | 1.0 | 1.2 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 |
| Fe2+ | 有 | 有 | 有 | 无 | 无 | 无 | 无 |
| Cr4+ | 无 | 无 | 无 | 无 | 无 | 有 | 有 |
(4)“反萃取”得到的NiSO4溶液,可在强碱溶液中被NaClO氧化,得到用作镍镉电池正极材料的NiOOH。该反应的离子方程式为
A.为得到较大NiSO4·nH2O晶体颗粒,宜用冰水快速冷却结晶
B.蒸发浓缩至溶液表面出现晶膜时,停止加热
C.可通过抽滤提高过滤速度,在80℃鼓风干燥,快速得到干燥晶体
D.向冷却结晶后的固液混合物中加入乙醇可提高产率
(5)采用热重分析法测定NiSO4·nH2O样品所含结晶水数。将样品在900℃下进行煅烧,失重率随时间变化如下图,A点时失掉2个结晶水,n的值为

您最近一年使用:0次
2021-05-14更新
|
539次组卷
|
2卷引用:河北省秦皇岛市青龙一中2021届高三高考适应性考试化学试题



