名校
解题方法
1 . 氯化钡是重要的化工原料,是制备其他钡盐的主要中间原料,以毒重石(主要成分为 ,还含有
,还含有 及含Ca、Mg、Fe、Al的化合物)为原料制备
及含Ca、Mg、Fe、Al的化合物)为原料制备 的工艺流程如下:
的工艺流程如下: 、
、 、
、 、
、 形式存在于溶液中。
形式存在于溶液中。
回答下列问题:
(1)在“浸取”时,除温度、酸的浓度、液固比等因素影响钡的浸出率外,还有___________ 因素。
(2)下表列举了不同温度、盐酸的浓度、液固比下钡的浸出率实验数据,每个实验只改变一个条件:
分析表中数据,温度越高钡的浸出率越低的可能原因是___________ ;判断“浸取”的最佳液固比为___________ 。
(3)常温时,几种金属离子沉淀的pH如图所示,加 时发生反应的离子方程式为
时发生反应的离子方程式为___________ ;“调pH(Ⅰ)”时,调节溶液 ,则“滤渣Ⅱ”的主要成分为
,则“滤渣Ⅱ”的主要成分为___________ (填化学式)。___________ 。
 ,还含有
,还含有 及含Ca、Mg、Fe、Al的化合物)为原料制备
及含Ca、Mg、Fe、Al的化合物)为原料制备 的工艺流程如下:
的工艺流程如下: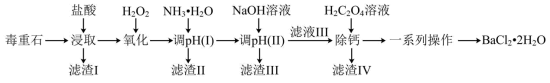
 、
、 、
、 、
、 形式存在于溶液中。
形式存在于溶液中。回答下列问题:
(1)在“浸取”时,除温度、酸的浓度、液固比等因素影响钡的浸出率外,还有
(2)下表列举了不同温度、盐酸的浓度、液固比下钡的浸出率实验数据,每个实验只改变一个条件:
| 改变的条件 | 温度(℃) | 盐酸的浓度(%) | 液固比 | ||||||||
| 30 | 55 | 75 | 10 | 15 | 20 | 25 | 3:1 | 4:1 | 5:1 | 6:1 | |
| 钡的浸出率(%) | 74.31 | 69.60 | 68.42 | 59.21 | 74.31 | 74.15 | 55.32 | 59.84 | 65.12 | 74.31 | 74.35 |
(3)常温时,几种金属离子沉淀的pH如图所示,加
 时发生反应的离子方程式为
时发生反应的离子方程式为 ,则“滤渣Ⅱ”的主要成分为
,则“滤渣Ⅱ”的主要成分为
您最近一年使用:0次
2 . 历史上诺贝尔化学奖曾经3次颁给研究合成氨的化学家。合成氨的原理为  。回答下列问题。
。回答下列问题。
(1)t℃时,向填充有催化剂、体积为2L 的刚性容器中充入一定量的 和N2合成氨,实验中测得 c(NH3)随时间的变化如表所示:
和N2合成氨,实验中测得 c(NH3)随时间的变化如表所示:
5~15min内 N2的平均反应速率  =
=___________ 
下列情况能说明反应达到平衡状态的是________ (填标号)。
A.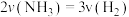 B. 混合气体的相对分子质量不再变化
B. 混合气体的相对分子质量不再变化
C. N2体积分数不再变化 D. 混合气体的密度保持不变
(2)如表列出了在不同温度和压强下,反应达到平衡时) 的百分含量
的百分含量  。
。
①从表中数据得出,最优的条件是___________ 。
②工业上通常选择在400~500℃和10~30MPa条件下合成氨, 原因是___________ 。
 。回答下列问题。
。回答下列问题。(1)t℃时,向填充有催化剂、体积为2L 的刚性容器中充入一定量的
 和N2合成氨,实验中测得 c(NH3)随时间的变化如表所示:
和N2合成氨,实验中测得 c(NH3)随时间的变化如表所示:| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol·L⁻¹ | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
 =
=
下列情况能说明反应达到平衡状态的是
A.
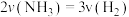 B. 混合气体的相对分子质量不再变化
B. 混合气体的相对分子质量不再变化C. N2体积分数不再变化 D. 混合气体的密度保持不变
(2)如表列出了在不同温度和压强下,反应达到平衡时)
 的百分含量
的百分含量  。
。压强/MPa 温度/℃ | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.5 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
②工业上通常选择在400~500℃和10~30MPa条件下合成氨, 原因是
您最近一年使用:0次
解题方法
3 . 利用图中装置进行实验,能达到实验目的的是
| A | B |
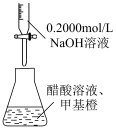 | 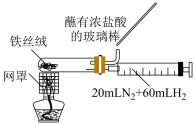 |
| 装置测定醋酸浓度 | 合成氨并检验氨的生成 |
| C | D |
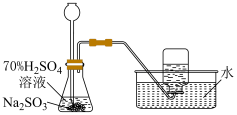 | 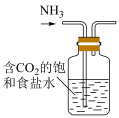 |
制备 | 模拟侯氏制碱法制备 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 在硫酸工业中,通过下列反应: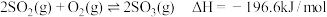 ,下表列出了在不同温度和压强下,反应达到平衡时
,下表列出了在不同温度和压强下,反应达到平衡时 的转化率。下列说法不正确的是
的转化率。下列说法不正确的是
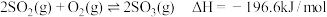 ,下表列出了在不同温度和压强下,反应达到平衡时
,下表列出了在不同温度和压强下,反应达到平衡时 的转化率。下列说法不正确的是
的转化率。下列说法不正确的是| 温度/ | 平衡时 的转化率 的转化率 | ||||
| 0.1MPa | 0.5MPa | 1MPa | 5MPa | 10MPa | |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
| A.工业上通入过量空气的主要目的是加快反应速率 |
B.回收尾气中的 仅为了防止空气污染 仅为了防止空气污染 |
C.采用常压条件是因为常压下 的转化率足够高,增大压强会增加设备成本 的转化率足够高,增大压强会增加设备成本 |
D.选择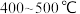 的较高温度既提高反应速率也提高平衡转化率 的较高温度既提高反应速率也提高平衡转化率 |
您最近一年使用:0次
5 . 下图为工业合成氨的流程图。图中为提高原料转化率而采取的措施是
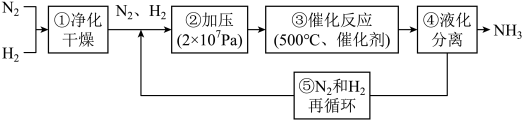
| A.①②③ | B.①③⑤ | C.②④⑤ | D.②③④ |
您最近一年使用:0次
2024-03-23更新
|
63次组卷
|
2卷引用:海南省海桂中学2023-2024学年高二上学期12月教学检测(三)化学试题
解题方法
6 . Ⅰ.习近平总书记十分重视生态环境保护,多次对生态文明建设作出重要指示,其中研究 、
、 、CO等气体的无害化处理对治埋大气污染、建设生态文明具有重要意义。
、CO等气体的无害化处理对治埋大气污染、建设生态文明具有重要意义。
(1)处理含CO、 烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:
烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:
①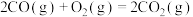
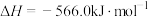
②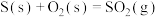

则CO与 反应生成S的热化学方程式是
反应生成S的热化学方程式是_______ 。
(2)在一绝热体系且容积固定的密闭容器中,用 催化还原
催化还原 也可以消除氮氧化物的污染,其中发生化学反应之一为:
也可以消除氮氧化物的污染,其中发生化学反应之一为: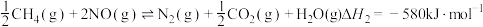 ,能说明上反应达到平衡状态的是
,能说明上反应达到平衡状态的是_______ 。
a.平均摩尔质量不变 b. 和
和 的体积比保持不变
的体积比保持不变
c.体系压强保持不变 d.每生成1mol 同时生成2molNO
同时生成2molNO
Ⅱ.运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
(3)生产氢气:将水蒸气通过红热的炭即产生水煤气;
 ,
,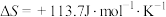 ,该反应在(填“高温”或“低温”或“任何温度”)
,该反应在(填“高温”或“低温”或“任何温度”)_______ 下,才能自发进行。
(4)合成氨工业中的主要反应是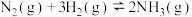
 ,从温度和压强的角度回答:要加快合成氨的反应速率应选择
,从温度和压强的角度回答:要加快合成氨的反应速率应选择_______ ;要提高氨的产率应选择_______ 。
 、
、 、CO等气体的无害化处理对治埋大气污染、建设生态文明具有重要意义。
、CO等气体的无害化处理对治埋大气污染、建设生态文明具有重要意义。(1)处理含CO、
 烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:
烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:①
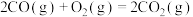
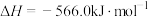
②
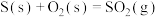

则CO与
 反应生成S的热化学方程式是
反应生成S的热化学方程式是(2)在一绝热体系且容积固定的密闭容器中,用
 催化还原
催化还原 也可以消除氮氧化物的污染,其中发生化学反应之一为:
也可以消除氮氧化物的污染,其中发生化学反应之一为: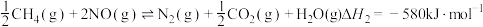 ,能说明上反应达到平衡状态的是
,能说明上反应达到平衡状态的是a.平均摩尔质量不变 b.
 和
和 的体积比保持不变
的体积比保持不变c.体系压强保持不变 d.每生成1mol
 同时生成2molNO
同时生成2molNOⅡ.运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
(3)生产氢气:将水蒸气通过红热的炭即产生水煤气;

 ,
,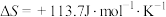 ,该反应在(填“高温”或“低温”或“任何温度”)
,该反应在(填“高温”或“低温”或“任何温度”)(4)合成氨工业中的主要反应是
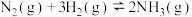
 ,从温度和压强的角度回答:要加快合成氨的反应速率应选择
,从温度和压强的角度回答:要加快合成氨的反应速率应选择
您最近一年使用:0次
解题方法
7 . 氨是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业;合成氨反应N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ/mol。下列有关合成氨反应的说法正确的是
2NH3(g) ΔH=-92.4 kJ/mol。下列有关合成氨反应的说法正确的是
 2NH3(g) ΔH=-92.4 kJ/mol。下列有关合成氨反应的说法正确的是
2NH3(g) ΔH=-92.4 kJ/mol。下列有关合成氨反应的说法正确的是| A.高温条件下该反应可以自发 |
| B.反应的ΔH=E(N-N)+3E(H-H)-6E(N-H) (E表示键能) |
| C.反应中每消耗1 mol H2转移电子的数目约等于2×6.02×1023 |
| D.该反应采用高温高压条件是为了增大H2的平衡转化率 |
您最近一年使用:0次
名校
8 . 某小组同学研究合成氨反应及氨水的性质如下:
(1)已知:N2(g)+3H2(g)=2NH3(g) ΔH =-92.4 kJ/mol
2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ/mol
则氨气完全燃烧生成氮气和水蒸气的热化学方程式________ 。
(2)实验室在固定容积的密闭容器中加入1mol氮气和3mol氢气模拟工业合成氨,反应在一定条件下已达到平衡的标志是________ 。
a.气体的密度不再发生改变 b.容器内的压强保持不变
c.N2、H2、NH3的浓度不再发生变化 d.反应停止,正、逆反应的速率都等于零
(3)工业合成氨的反应温度选择500℃左右的原因是_______ 。
(4)如图是合成氨反应平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是_______ (填“温度”或“压强”),判断L1、L2的大小关系:L1______ L2(填“<”或“>”)。

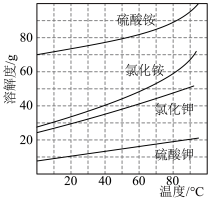
(5)在70℃-80℃时,配制饱和的(NH4)2SO4和KCl溶液后混合。经过________ 、_______ 、干燥就可以得到K2SO4晶体。
(1)已知:N2(g)+3H2(g)=2NH3(g) ΔH =-92.4 kJ/mol
2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ/mol
则氨气完全燃烧生成氮气和水蒸气的热化学方程式
(2)实验室在固定容积的密闭容器中加入1mol氮气和3mol氢气模拟工业合成氨,反应在一定条件下已达到平衡的标志是
a.气体的密度不再发生改变 b.容器内的压强保持不变
c.N2、H2、NH3的浓度不再发生变化 d.反应停止,正、逆反应的速率都等于零
(3)工业合成氨的反应温度选择500℃左右的原因是
(4)如图是合成氨反应平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是

(5)在70℃-80℃时,配制饱和的(NH4)2SO4和KCl溶液后混合。经过

您最近一年使用:0次
名校
9 . 某科研小组探究了 和
和 协同氧化烟道气中
协同氧化烟道气中 的反应状况,
的反应状况, 的除去率与投料比[
的除去率与投料比[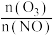 ]和
]和 溶液浓度的关系如图1、2所示。已知:
溶液浓度的关系如图1、2所示。已知: 参与反应时,
参与反应时, 的
的 转化成臭氧的另一种同素异形体;
转化成臭氧的另一种同素异形体; 被氧化成
被氧化成 的最高价态离子,
的最高价态离子, 的还原产物为
的还原产物为 。
。

下列叙述错误的是
 和
和 协同氧化烟道气中
协同氧化烟道气中 的反应状况,
的反应状况, 的除去率与投料比[
的除去率与投料比[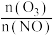 ]和
]和 溶液浓度的关系如图1、2所示。已知:
溶液浓度的关系如图1、2所示。已知: 参与反应时,
参与反应时, 的
的 转化成臭氧的另一种同素异形体;
转化成臭氧的另一种同素异形体; 被氧化成
被氧化成 的最高价态离子,
的最高价态离子, 的还原产物为
的还原产物为 。
。
下列叙述错误的是
A.结合生产成本考虑,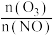 最佳投料比为0.5 最佳投料比为0.5 |
B.其他条件相同,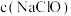 越大, 越大, 除去率越大 除去率越大 |
C.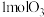 和 和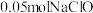 共同作用最多除去 共同作用最多除去 |
D. 溶液吸收 溶液吸收 的离子方程式为 的离子方程式为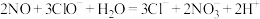 |
您最近一年使用:0次
2024-02-13更新
|
87次组卷
|
2卷引用:河北省沧州市泊头市部分学校2023-2024学年高三上学期12月月考化学试题
名校
10 . 氨对发展农业有着重要意义,也是重要的化工原料。合成氨的生产流程示意如下。

下列说法不正确 的是

下列说法
| A.为防止原料气中混有的杂质使催化剂“中毒”而丧失催化活性,原料气必须经过净化 |
| B.压缩机加压过程,既要考虑平衡移动的问题,又要考虑加压对设备材料的强度设备的制造要求的问题 |
| C.合成氨反应的温度控制在500℃左右,此温度下反应物的平衡转化率最大 |
| D.冷却过程,及时将NH3从平衡混合物中分离除去,促使合成氨反应向生成氨气的方向移动 |
您最近一年使用:0次



