名校
解题方法
1 . 一定温度下,向三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应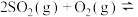
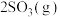 (正反应放热),测得反应的相关数据如下:
(正反应放热),测得反应的相关数据如下:
下列说法正确的是
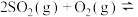
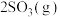 (正反应放热),测得反应的相关数据如下:
(正反应放热),测得反应的相关数据如下:| 容器1 | 容器2 | 容器3 | |
| 反应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2 mol 、1 mol 、1 mol | 4mol | 2 mol 、1 mol 、1 mol |
平衡时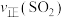 / /(mol·L  ·s ·s ) ) |  |  |  |
平衡时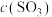 /(mol·L  ) ) |  |  | 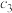 |
| 平衡时体系总压强p/Pa |  |  |  |
物质的平衡转化率 | 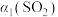 | 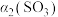 | 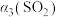 |
| 平衡常数K |  |  |  |
A. , , | B. , ,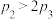 |
C. , ,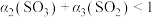 | D. , ,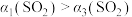 |
您最近一年使用:0次
2024-01-19更新
|
53次组卷
|
2卷引用:河北省沧州市大数据联考2023-2024学年高二上学期10月月考化学试题
名校
2 . 反应X(g)+Y(g) 2Z(g) ΔH<0,在一定条件下,反应情况如图所示。若使曲线a变为曲线b可采取的措施是
2Z(g) ΔH<0,在一定条件下,反应情况如图所示。若使曲线a变为曲线b可采取的措施是
 2Z(g) ΔH<0,在一定条件下,反应情况如图所示。若使曲线a变为曲线b可采取的措施是
2Z(g) ΔH<0,在一定条件下,反应情况如图所示。若使曲线a变为曲线b可采取的措施是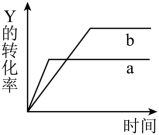
| A.加入催化剂 | B.降低温度 |
| C.减小压强 | D.保持容器体积不变,冲入He气 |
您最近一年使用:0次
2024-01-08更新
|
154次组卷
|
3卷引用:河北省保定市高碑店市崇德实验中学2023-2024学年高二上学期1月考试化学试题
名校
3 . 在一密闭烧瓶中,在25℃时存在如下平衡:2NO2(g)⇌N2O4(g) ∆H<0,将烧瓶置于100℃的水中,则下列几项性质中不会改变的是
①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度
①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度
| A.①和③ | B.②和④ | C.④和⑤ | D.③和⑤ |
您最近一年使用:0次
2023-12-27更新
|
48次组卷
|
2卷引用:河北省保定市高碑店市崇德实验中学2023-2024学年高二上学期1月考试化学试题
名校
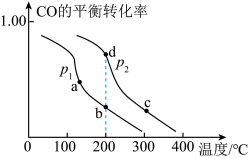
4 . 为实现碳中和目标,可利用CO制甲醇进行有效转化,反应为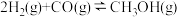 。一定条件下,在容积恒定为VL的密闭容器中充入
。一定条件下,在容积恒定为VL的密闭容器中充入 和
和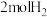 ,在催化剂作用下发生上述反应,CO的平衡转化率与温度、压强的关系如图所示。下列说法正确的是
,在催化剂作用下发生上述反应,CO的平衡转化率与温度、压强的关系如图所示。下列说法正确的是
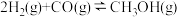 。一定条件下,在容积恒定为VL的密闭容器中充入
。一定条件下,在容积恒定为VL的密闭容器中充入 和
和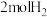 ,在催化剂作用下发生上述反应,CO的平衡转化率与温度、压强的关系如图所示。下列说法正确的是
,在催化剂作用下发生上述反应,CO的平衡转化率与温度、压强的关系如图所示。下列说法正确的是
A.图中b、c、d三点的化学平衡常数分别为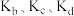 ,它们的大小关系为 ,它们的大小关系为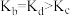 |
B.体系中气体平均摩尔质量: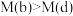 |
| C.不断将甲醇从体系中分离出来能够同时增大正反应速率和提高CO的平衡转化率 |
D.体系中活化分子百分数: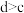 |
您最近一年使用:0次
名校
解题方法
5 . HCOOH是一种重要的化工原料。
(1)已知几种共价键的键能如下表。
根据上述键能估算:

___________  。
。
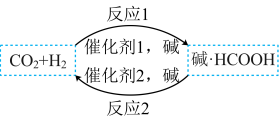
(2)HCOOH是一种储氢材料,其某种制备原理如图所示。反应1断裂的化学键有___________(填标号)。
(3)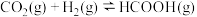 的速率公式为
的速率公式为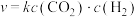 (k为速率常数,只与温度、催化剂有关)。已知经验公式为
(k为速率常数,只与温度、催化剂有关)。已知经验公式为 (其中,
(其中, 、k分别为活化能、速率常数,R、C为常数,T为温度)。在催化剂作用下,测得
、k分别为活化能、速率常数,R、C为常数,T为温度)。在催化剂作用下,测得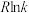 与温度(
与温度( )的关系如图所示。其他条件都相同时,催化效率较高的是
)的关系如图所示。其他条件都相同时,催化效率较高的是___________ (填“Cat1”或“Cat2”)。Cat2催化剂作用下,活化能 为
为___________  。
。

(4)在一定温度下,保持总压强为170kPa。在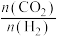 为1:1、1:2、1:3条件下发生反应
为1:1、1:2、1:3条件下发生反应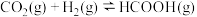 ,测得
,测得 的平衡转化率与
的平衡转化率与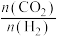 之间的关系如图。曲线c代表的投料比为
之间的关系如图。曲线c代表的投料比为___________ 。M点条件下,平衡常数 为
为___________  。(提示:用分压计算的平衡常数为
。(提示:用分压计算的平衡常数为 ,分压=总压×物质的量分数)
,分压=总压×物质的量分数)

(5)某种含银催化剂可以高效催化甲酸的合成,已知银的晶胞结构如图,其晶胞参数为anm,设 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
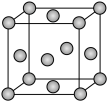
①Ag原子的配位数为___________ 。
②Ag原子的半径为___________ nm。
③该晶体的密度为___________  。
。
(1)已知几种共价键的键能如下表。
| 共价键 | 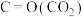 | H-H | H-C | C=O | C-O | O-H |
键能 | 803 | 436 | 413 | 745 | 351 | 463 |


 。
。(2)HCOOH是一种储氢材料,其某种制备原理如图所示。反应1断裂的化学键有___________(填标号)。

| A.极性键 | B.氢键 | C.非极性键 | D.σ键和π键 |
(3)
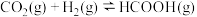 的速率公式为
的速率公式为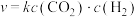 (k为速率常数,只与温度、催化剂有关)。已知经验公式为
(k为速率常数,只与温度、催化剂有关)。已知经验公式为 (其中,
(其中, 、k分别为活化能、速率常数,R、C为常数,T为温度)。在催化剂作用下,测得
、k分别为活化能、速率常数,R、C为常数,T为温度)。在催化剂作用下,测得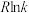 与温度(
与温度( )的关系如图所示。其他条件都相同时,催化效率较高的是
)的关系如图所示。其他条件都相同时,催化效率较高的是 为
为 。
。
(4)在一定温度下,保持总压强为170kPa。在
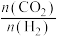 为1:1、1:2、1:3条件下发生反应
为1:1、1:2、1:3条件下发生反应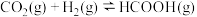 ,测得
,测得 的平衡转化率与
的平衡转化率与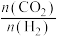 之间的关系如图。曲线c代表的投料比为
之间的关系如图。曲线c代表的投料比为 为
为 。(提示:用分压计算的平衡常数为
。(提示:用分压计算的平衡常数为 ,分压=总压×物质的量分数)
,分压=总压×物质的量分数)
(5)某种含银催化剂可以高效催化甲酸的合成,已知银的晶胞结构如图,其晶胞参数为anm,设
 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
①Ag原子的配位数为
②Ag原子的半径为
③该晶体的密度为
 。
。
您最近一年使用:0次
2023-11-27更新
|
223次组卷
|
3卷引用:河北省邢台市五岳联盟2023-2024学年高三上学期11月月考化学试题
名校
6 . 二氧化碳加氢是对温室气体的有效转化,同时也是生成再生能源与化工原料的重要途径。
(1)由 加氢生成
加氢生成 的反应为
的反应为 。
。
①若 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成 该物质的焓变。则该反应的反应热
该物质的焓变。则该反应的反应热
_______ 。
②若在一定温度下的容积固定的密闭容器中进行该反应,则可以提高 平衡转化率的措施有
平衡转化率的措施有_______ (写出两种)。
③下列说法可以证明该反应已达到平衡状态的是_______ (填字母)。
a. b.容器内气体密度不再改变
b.容器内气体密度不再改变
c. 的物质的量分数不再改变 d.
的物质的量分数不再改变 d. 和
和 的浓度之比为1:2
的浓度之比为1:2
(2) 催化加氢制低碳烯烃的反应历程如图所示,
催化加氢制低碳烯烃的反应历程如图所示, 首先在
首先在 表面解离成2个
表面解离成2个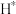 ,随后参与到
,随后参与到 的转化过程。
的转化过程。
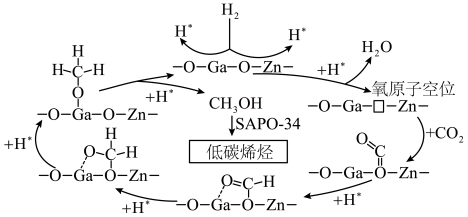
注:“□”表示氧原子空位,“*”表示吸附在催化剂上的微粒。
理论上反应历程中消耗的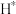 与生成的甲醇的物质的量之比为
与生成的甲醇的物质的量之比为_______ 。
(3)一定条件下 与
与 可生成甲酸
可生成甲酸 ,化学方程式为
,化学方程式为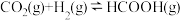 。
。
①在 下,等物质的量的
下,等物质的量的 与
与 的混合气体反应生成甲酸,化学反应速率
的混合气体反应生成甲酸,化学反应速率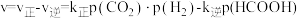 ,
,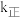 、k逆分别为正反应、逆反应的速率常数,
、k逆分别为正反应、逆反应的速率常数, 为气体的分压(气体分压=气体总压
为气体的分压(气体分压=气体总压 体积分数)。用气体分压表示的平衡常数
体积分数)。用气体分压表示的平衡常数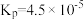 ,则
,则 的转化率为
的转化率为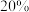 时,
时,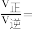
_______ 。
②恒定压强为 时,向密闭容器中充入一定量的
时,向密闭容器中充入一定量的 气体,
气体, 除了能分解成
除了能分解成 和
和 ,还能分解为
,还能分解为 和
和 ,反应为
,反应为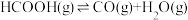 ,则此平衡体系中
,则此平衡体系中 或
或 的选择性和
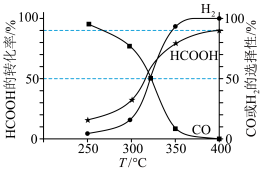
的选择性和 的转化率随温度变化曲线如图所示。图中随着温度升高,
的转化率随温度变化曲线如图所示。图中随着温度升高, 的转化率增大,请解释
的转化率增大,请解释 的选择性下降可能的原因:
的选择性下降可能的原因:_______ 。 时
时 的体积分数为
的体积分数为_______ 。
(1)由
 加氢生成
加氢生成 的反应为
的反应为 。
。①若
 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成 该物质的焓变。则该反应的反应热
该物质的焓变。则该反应的反应热
| 物质 | CO2 | H2 | CH4 | H2O |
 (kJ·mol-1) (kJ·mol-1) | -393.5 | 0 | -74.8 | -241.8 |
 平衡转化率的措施有
平衡转化率的措施有③下列说法可以证明该反应已达到平衡状态的是
a.
 b.容器内气体密度不再改变
b.容器内气体密度不再改变c.
 的物质的量分数不再改变 d.
的物质的量分数不再改变 d. 和
和 的浓度之比为1:2
的浓度之比为1:2(2)
 催化加氢制低碳烯烃的反应历程如图所示,
催化加氢制低碳烯烃的反应历程如图所示, 首先在
首先在 表面解离成2个
表面解离成2个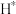 ,随后参与到
,随后参与到 的转化过程。
的转化过程。
注:“□”表示氧原子空位,“*”表示吸附在催化剂上的微粒。
理论上反应历程中消耗的
 与生成的甲醇的物质的量之比为
与生成的甲醇的物质的量之比为(3)一定条件下
 与
与 可生成甲酸
可生成甲酸 ,化学方程式为
,化学方程式为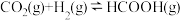 。
。①在
 下,等物质的量的
下,等物质的量的 与
与 的混合气体反应生成甲酸,化学反应速率
的混合气体反应生成甲酸,化学反应速率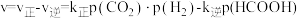 ,
,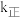 、k逆分别为正反应、逆反应的速率常数,
、k逆分别为正反应、逆反应的速率常数, 为气体的分压(气体分压=气体总压
为气体的分压(气体分压=气体总压 体积分数)。用气体分压表示的平衡常数
体积分数)。用气体分压表示的平衡常数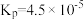 ,则
,则 的转化率为
的转化率为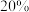 时,
时,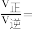
②恒定压强为
 时,向密闭容器中充入一定量的
时,向密闭容器中充入一定量的 气体,
气体, 除了能分解成
除了能分解成 和
和 ,还能分解为
,还能分解为 和
和 ,反应为
,反应为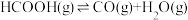 ,则此平衡体系中
,则此平衡体系中 或
或 的选择性和
的选择性和 的转化率随温度变化曲线如图所示。图中随着温度升高,
的转化率随温度变化曲线如图所示。图中随着温度升高, 的转化率增大,请解释
的转化率增大,请解释 的选择性下降可能的原因:
的选择性下降可能的原因: 时
时 的体积分数为
的体积分数为
您最近一年使用:0次
7 . “碳储科学”主要研究方向涉及 的捕获、转化等领域。高浓度的
的捕获、转化等领域。高浓度的 溶液可作为
溶液可作为 的捕获剂,为了更好地捕获
的捕获剂,为了更好地捕获 ,控制压强合理的是
,控制压强合理的是
 的捕获、转化等领域。高浓度的
的捕获、转化等领域。高浓度的 溶液可作为
溶液可作为 的捕获剂,为了更好地捕获
的捕获剂,为了更好地捕获 ,控制压强合理的是
,控制压强合理的是| A.常压 | B.高于常压 | C.低于常压 | D.无法确定 |
您最近一年使用:0次
2023-11-14更新
|
48次组卷
|
3卷引用:河北省保定市高碑店市崇德实验中学2023-2024学年高三上学期1月考试化学试题
名校
8 . 下列叙述中,不能用勒夏特列原理解释的是
A.红棕色的 气体体系加压后颜色先变深后变浅 气体体系加压后颜色先变深后变浅 |
B.向橙色 溶液中加入一定浓度的 溶液中加入一定浓度的 溶液后,溶液变为黄色 溶液后,溶液变为黄色 |
C.对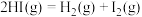 平衡体系增大压强使气体颜色变深 平衡体系增大压强使气体颜色变深 |
| D.新制氯水光照下颜色变浅 |
您最近一年使用:0次
名校
9 . 在密闭容器中,一定量M和N的混合气体发生反应: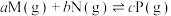 ,达到平衡时,测得M的浓度为
,达到平衡时,测得M的浓度为 ,在温度不变的条件下,仅将容器的体积压缩至原来的一半,反应再次达到平衡时,测得M的浓度为
,在温度不变的条件下,仅将容器的体积压缩至原来的一半,反应再次达到平衡时,测得M的浓度为 ,下列有关判断正确的是
,下列有关判断正确的是
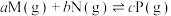 ,达到平衡时,测得M的浓度为
,达到平衡时,测得M的浓度为 ,在温度不变的条件下,仅将容器的体积压缩至原来的一半,反应再次达到平衡时,测得M的浓度为
,在温度不变的条件下,仅将容器的体积压缩至原来的一半,反应再次达到平衡时,测得M的浓度为 ,下列有关判断正确的是
,下列有关判断正确的是A.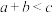 | B.P的平衡体积分数下降 |
| C.N的平衡浓度增大 | D.平衡向逆反应方向移动 |
您最近一年使用:0次
2023-10-05更新
|
61次组卷
|
3卷引用:河北省邢台市四校质检联盟2023-2024学年高二上学期第一次月考化学试题
10 . 下列事实不能用勒夏特列原理解释的是
| A.夏天打开可乐有大量泡沫溢出 |
| B.高炉炼铁时,将焦炭和铁矿石预先粉碎 |
| C.实验室制备乙酸乙酯时,将乙酸乙酯不断蒸出 |
| D.用排饱和食盐水法收集氯气 |
您最近一年使用:0次
2023-10-05更新
|
215次组卷
|
6卷引用:河北省邢台市四校质检联盟2023-2024学年高二上学期第一次月考化学试题



