解题方法
1 . I.甲醇(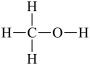 )是重要的化工原料,又可作为燃料。利用合成气(主要成分为
)是重要的化工原料,又可作为燃料。利用合成气(主要成分为 、
、 和
和 )在催化剂的作用下合成甲醇,涉及的反应有:
)在催化剂的作用下合成甲醇,涉及的反应有:
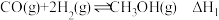
②

③
 与
与 反应生成
反应生成 和
和
已知反应①中的相关的化学键键能数据如下:(
 为
为 )
)| 化学键 |  |  |  |  |  |
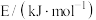 | 436 | 343 | 1076 | 465 | 413 |
(1)

 。
。(2)反应③的热化学方程式为
 用含
用含 和
和 的式子表示)
的式子表示)Ⅱ.亚硝酰氯(
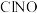 )是有机合成中的重要试剂,可通过反应:
)是有机合成中的重要试剂,可通过反应: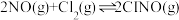 获得。
获得。(3)在恒温恒容的密闭容器中,氮氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
①
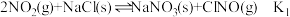
②

③

则

 、
、 的式子表示)。
的式子表示)。下列事实不能说明上述体系中反应③已达平衡状态的是
a.容器内气体的颜色不再变化 b.容器中气体的密度不再变化 c.
 不再发生变化
不再发生变化(4)300℃时,
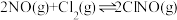 的正反应速率表达式为
的正反应速率表达式为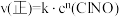 ,测得速率和浓度的关系如表所示:
,测得速率和浓度的关系如表所示:| 序号 | 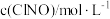 | 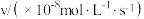 |
| ① | 0.30 | 0.36 |
| ② | 0.60 | 1.44 |
| ③ | 0.90 | 3.24 |
(5)对于反应③按投料比
 把
把 和
和 加入到压强恒为p的密闭容器中发生反应,平衡时
加入到压强恒为p的密闭容器中发生反应,平衡时 的转化率与温度T的关系如图所示:
的转化率与温度T的关系如图所示: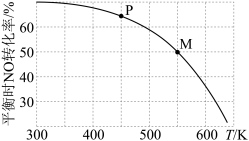
 的体积分数为
的体积分数为②M点的分压平衡常数

(6)一定条件下,在恒温恒容的密闭容器中按一定比例充入
 和
和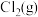 ,平衡时
,平衡时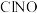 的体积分数随
的体积分数随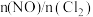 的变化图像如图所示,则A、B、C三状态中,
的变化图像如图所示,则A、B、C三状态中, 的转化率最大的是
的转化率最大的是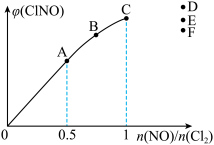
您最近一年使用:0次
名校
解题方法
2 . 化学与生产生活密切相关,下列说法不正确的是
| A.泡沫灭火器的成分是小苏打和硫酸铝溶液 |
| B.采用催化转换技术能提高汽车尾气中有害气体的平衡转化率 |
| C.粗镍精炼时,粗镍作阳极 |
| D.漂白粉和明矾都常用于自来水的处理,二者的作用原理是不相同的 |
您最近一年使用:0次
解题方法
3 . 金属钌在电子制造、化学工业及催化剂生产等行业中有关键作用,六氯钌酸铵[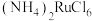 ]是生产金属钌的重要中间产物。一种利用精炼镍阳极泥(主要含金属Ru、Os及Pb等)制备六氯钌酸铵的工业流程如图所示:
]是生产金属钌的重要中间产物。一种利用精炼镍阳极泥(主要含金属Ru、Os及Pb等)制备六氯钌酸铵的工业流程如图所示:
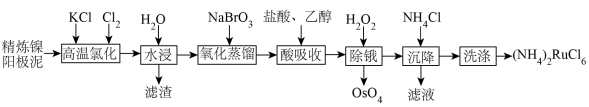
已知:六氯钌酸铵在冷水、乙醇中的溶解度较小。
回答下列问题:
(1)“高温氯化”后得到 、
、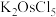 ,
,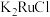 。
。 中Ru元素的化合价为
中Ru元素的化合价为___________ ,生成 的化学方程式为
的化学方程式为___________ 。
(2)“氧化蒸馏”过程中蒸出 、
、 ,生成
,生成 的离子方程式为
的离子方程式为___________ 。
(3)“酸吸收”过程中加入乙醇的作用是___________ 。
(4)“除锇”过程中元素钌化合价不变,溶液的主要成分为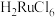 ,溶液中存在
,溶液中存在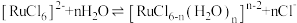
 ,六氯钌酸铵中水含量低,有利于六氯钌酸铵结晶物的粉碎焙烧。为降低六氯钌酸铵中水的含量,可以采用的措施有
,六氯钌酸铵中水含量低,有利于六氯钌酸铵结晶物的粉碎焙烧。为降低六氯钌酸铵中水的含量,可以采用的措施有___________ 。
(5)检验滤液中主要阴离子的实验方法是___________ ,“洗涤”时最合适的试剂为___________ 。
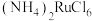 ]是生产金属钌的重要中间产物。一种利用精炼镍阳极泥(主要含金属Ru、Os及Pb等)制备六氯钌酸铵的工业流程如图所示:
]是生产金属钌的重要中间产物。一种利用精炼镍阳极泥(主要含金属Ru、Os及Pb等)制备六氯钌酸铵的工业流程如图所示:
已知:六氯钌酸铵在冷水、乙醇中的溶解度较小。
回答下列问题:
(1)“高温氯化”后得到
 、
、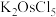 ,
,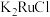 。
。 中Ru元素的化合价为
中Ru元素的化合价为 的化学方程式为
的化学方程式为(2)“氧化蒸馏”过程中蒸出
 、
、 ,生成
,生成 的离子方程式为
的离子方程式为(3)“酸吸收”过程中加入乙醇的作用是
(4)“除锇”过程中元素钌化合价不变,溶液的主要成分为
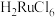 ,溶液中存在
,溶液中存在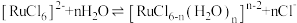
 ,六氯钌酸铵中水含量低,有利于六氯钌酸铵结晶物的粉碎焙烧。为降低六氯钌酸铵中水的含量,可以采用的措施有
,六氯钌酸铵中水含量低,有利于六氯钌酸铵结晶物的粉碎焙烧。为降低六氯钌酸铵中水的含量,可以采用的措施有(5)检验滤液中主要阴离子的实验方法是
您最近一年使用:0次
4 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.18g金刚石中,碳碳共价键数为3NA |
| B.100g质量分数为46%的乙醇水溶液中氧原子数为NA |
C. 与足量的NaOH溶液反应转移的电子数是NA 与足量的NaOH溶液反应转移的电子数是NA |
D.某温度和压强下,将 气体充入密闭容器中,容器中的分子数为NA 气体充入密闭容器中,容器中的分子数为NA |
您最近一年使用:0次
5 . 砷的化合物可用于半导体领域。一种从酸性高浓度含砷废水[砷主要以亚砷酸(H3AsO3)形式存在]中回收As2O3的工艺流程如下:

已知:①As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
②As2S3 (s) +3S2-(aq) 2
2 (aq)
(aq)
③砷酸(H3AsO4)在酸性条件下有强氧化性,能被SO2、HI等还原。
下列说法错误的是

已知:①As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
②As2S3 (s) +3S2-(aq)
 2
2 (aq)
(aq)③砷酸(H3AsO4)在酸性条件下有强氧化性,能被SO2、HI等还原。
下列说法错误的是
| A.“沉砷”过程,用过量的Na2S代替FeS效果更好 |
| B.浸渣的主要成分为FeS |
C.“还原”过程的离子方程式为2SO2+2H3AsO4=As2O3+2 +4H++H2O +4H++H2O |
| D.“还原”后可以用HI、淀粉溶液检验溶液中是否仍存在砷酸 |
您最近一年使用:0次
2023-11-26更新
|
375次组卷
|
2卷引用:山东省德州市第一中学2023-2024学年高三上学期1月月考化学试题
名校
解题方法
6 . 在一定温度下,将 和2moB两种气体相混合于容积为
和2moB两种气体相混合于容积为 的某密闭容器中,发生如下反应:
的某密闭容器中,发生如下反应: ,
, 末反应达到平衡状态,此时测得D的浓度为
末反应达到平衡状态,此时测得D的浓度为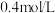 ,用C表示的反应速率为
,用C表示的反应速率为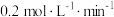 请填写下列空白:
请填写下列空白:
(1)x值等于___________ 。
(2)A的转化率为___________ 。
(3)如果增大反应体系的压强,则平衡体系中C的质量分数___________ (增大、减小或不变)。
(4)在此温度下,该化学反应的平衡常数K=___________ 。
(5)在此条件下,向该容器内加入 、
、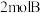 、
、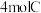 、
、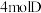 后,
后,
___________ (填“>”“<”或“=”) 。
。
(6)在此条件下, 末再向容器内加入
末再向容器内加入 、
、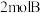 ,则平衡移动的方向
,则平衡移动的方向___________ ,再次达到平衡后A的转化率___________ (增大、减小或不变),C的物质的量分数___________ (增大、减小或不变)。
 和2moB两种气体相混合于容积为
和2moB两种气体相混合于容积为 的某密闭容器中,发生如下反应:
的某密闭容器中,发生如下反应: ,
, 末反应达到平衡状态,此时测得D的浓度为
末反应达到平衡状态,此时测得D的浓度为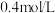 ,用C表示的反应速率为
,用C表示的反应速率为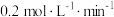 请填写下列空白:
请填写下列空白:(1)x值等于
(2)A的转化率为
(3)如果增大反应体系的压强,则平衡体系中C的质量分数
(4)在此温度下,该化学反应的平衡常数K=
(5)在此条件下,向该容器内加入
 、
、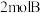 、
、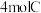 、
、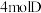 后,
后,
 。
。(6)在此条件下,
 末再向容器内加入
末再向容器内加入 、
、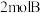 ,则平衡移动的方向
,则平衡移动的方向
您最近一年使用:0次
解题方法
7 . 反应mA(s)+nB(g) eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是
eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是

 eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是
eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是
| A.到平衡后,加入催化剂则C%增大 |
| B.化学方程式中n>e+f |
| C.达到平衡后,若升温,平衡左移 |
| D.达到平衡后,增加A的量有利于平衡向右移动 |
您最近一年使用:0次
8 . 部分含氯物质的分类与相应氯元素的化合价关系如图所示。下列说法错误的是


| A.a的水溶液可以闻到刺激性气味,说明其易挥发 |
| B.c为一种新型自来水消毒剂,c可以代替b,消毒效果比b更好 |
| C.家庭使用84消毒液的时候加入少量醋酸,消毒效果更好 |
| D.e的水溶液中加入硝酸酸化的硝酸银溶液,有白色沉淀生成 |
您最近一年使用:0次
2023-10-13更新
|
184次组卷
|
2卷引用:山东省实验中学2023-2024学年高一上学期10月月考化学试题
名校
9 . 某兴趣小组用图1装置探究压强对反应 的影响,推动或拉伸注射器活塞得到的混合气体透光率变化曲线如图2,整个过程均在恒温体系中进行。气体颜色越深,透光率越低。下列说法正确的是
的影响,推动或拉伸注射器活塞得到的混合气体透光率变化曲线如图2,整个过程均在恒温体系中进行。气体颜色越深,透光率越低。下列说法正确的是
 的影响,推动或拉伸注射器活塞得到的混合气体透光率变化曲线如图2,整个过程均在恒温体系中进行。气体颜色越深,透光率越低。下列说法正确的是
的影响,推动或拉伸注射器活塞得到的混合气体透光率变化曲线如图2,整个过程均在恒温体系中进行。气体颜色越深,透光率越低。下列说法正确的是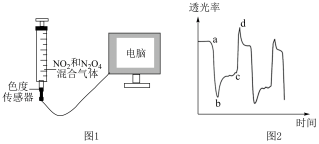
| A.a→b为拉伸活塞的过程 | B.b→c为平衡逆向移动的过程 |
| C.c→d为平衡正向移动的过程 | D.a、b、c、d的平衡常数相同 |
您最近一年使用:0次
2023-10-09更新
|
155次组卷
|
5卷引用:山东省部分学校2023-2024学年高二上学期10月月考化学试题
名校
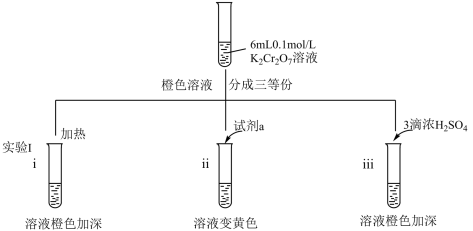
10 . 某兴趣小组以重铬酸钾(K2Cr2O7)溶液为研究对象,结合所学反应原理的知识改变条件使其发生“色彩变幻”。下列关于该实验的说法错误的是
已知:①K2Cr2O7溶液存在平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。
②含铬元素的离子在溶液中的颜色:Cr2O (橙色);CrO
(橙色);CrO (黄色);Cr 3+ (绿色)。
(黄色);Cr 3+ (绿色)。
已知:①K2Cr2O7溶液存在平衡:Cr2O
 +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。 ②含铬元素的离子在溶液中的颜色:Cr2O
 (橙色);CrO
(橙色);CrO (黄色);Cr 3+ (绿色)。
(黄色);Cr 3+ (绿色)。 
A.i 可证明反应 Cr2O +H2O +H2O 2CrO 2CrO +2H+的正反应放热 +2H+的正反应放热 |
| B.ii 是验证“只降低生成物的浓度,该平衡正向移动”,试剂 a 可以是 NaOH |
| C.iii 平衡逆向移动仅仅是因为增大了生成物的浓度 |
| D.向 iii 所得橙色溶液中加入乙醇,溶液将由橙色变为绿色 |
您最近一年使用:0次
2023-08-26更新
|
402次组卷
|
4卷引用:山东省青岛第一中学2023-2024学年高二上学期10月月考化学试题



