解题方法
1 . 合成气(CO+H2)在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品。
(1)煤化工中生产合成气的反应为:C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.5kJ·mol-1
CO(g)+H2(g) ΔH=+131.5kJ·mol-1
①判断该反应的自发性条件___________ ;
②在恒温恒容下,同时放入C(s)、H2O(g)、CO(g)、H2(g)四种物质,下列事实能够说明反应C(s)+H2O(g) CO(g)+H2(g)已达到平衡的是
CO(g)+H2(g)已达到平衡的是___________ 。
A.反应体系中,混合气体的密度不再改变
B.反应体系中,各组分的物质的量相等
C.反应体系中,当有2molH—O键断裂的同时有1molH—H键断裂
D.混合气体的平均相对分子质量保持不变
(2)天然气化工中生产合成气的主要反应为:2CH4(g)+O2(g) 2CO(g)+4H2(g) ΔH=akJ·mol-1,在恒容容器中按物质的量之比1︰2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
2CO(g)+4H2(g) ΔH=akJ·mol-1,在恒容容器中按物质的量之比1︰2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
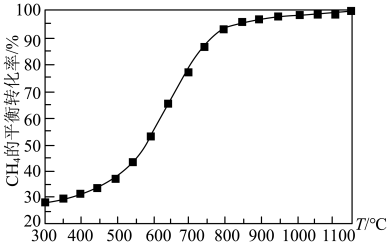
①请在图中画出压强为5.05×105Pa时CH4的平衡转化率随温度的变化曲线________ 。
②现有实验测得反应2CH4(g)+O2(g) 2CO(g)+4H2(g)在750℃下,以不同碳氧比[n(CH4)/n(O2)]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示。(已知:选择性=目标产物的产率/反应原料的转化率)
2CO(g)+4H2(g)在750℃下,以不同碳氧比[n(CH4)/n(O2)]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示。(已知:选择性=目标产物的产率/反应原料的转化率)
最佳碳氧比[n(CH4)/n(O2)]为___________ 。
(1)煤化工中生产合成气的反应为:C(s)+H2O(g)
 CO(g)+H2(g) ΔH=+131.5kJ·mol-1
CO(g)+H2(g) ΔH=+131.5kJ·mol-1①判断该反应的自发性条件
②在恒温恒容下,同时放入C(s)、H2O(g)、CO(g)、H2(g)四种物质,下列事实能够说明反应C(s)+H2O(g)
 CO(g)+H2(g)已达到平衡的是
CO(g)+H2(g)已达到平衡的是A.反应体系中,混合气体的密度不再改变
B.反应体系中,各组分的物质的量相等
C.反应体系中,当有2molH—O键断裂的同时有1molH—H键断裂
D.混合气体的平均相对分子质量保持不变
(2)天然气化工中生产合成气的主要反应为:2CH4(g)+O2(g)
 2CO(g)+4H2(g) ΔH=akJ·mol-1,在恒容容器中按物质的量之比1︰2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
2CO(g)+4H2(g) ΔH=akJ·mol-1,在恒容容器中按物质的量之比1︰2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
①请在图中画出压强为5.05×105Pa时CH4的平衡转化率随温度的变化曲线
②现有实验测得反应2CH4(g)+O2(g)
 2CO(g)+4H2(g)在750℃下,以不同碳氧比[n(CH4)/n(O2)]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示。(已知:选择性=目标产物的产率/反应原料的转化率)
2CO(g)+4H2(g)在750℃下,以不同碳氧比[n(CH4)/n(O2)]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示。(已知:选择性=目标产物的产率/反应原料的转化率)| 碳氧比[n(CH4)/n(O2)] | 1︰0.25 | 1︰0.5 | 1︰1 | 1︰1.25 |
| CH4转化率 | 0.40 | 0.88 | 0.98 | 0.99 |
| H2选择性 | 0.98 | 0.93 | 0.67 | 0.40 |
| CO选择性 | 0.99 | 0.94 | 0.65 | 0.32 |
您最近一年使用:0次
2 . 氮及其化合物的重要转化关系如图所示,下列说法正确的是
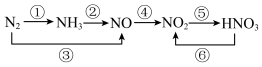

A.反应③④⑤是工业生产 的主要反应 的主要反应 |
| B.反应①②均需要使用催化剂,以提高反应物的平衡转化率 |
C.将 通入 通入 中发生反应⑤,生成 中发生反应⑤,生成 时同时生成 时同时生成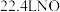 |
D.实验室用浓硝酸与铜通过反应⑥制取 时,得到的气体中可能含有 时,得到的气体中可能含有 和 和 |
您最近一年使用:0次
3 . 在密闭容器中进行反应: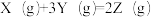 ,有关下列图像的说法错误的是
,有关下列图像的说法错误的是
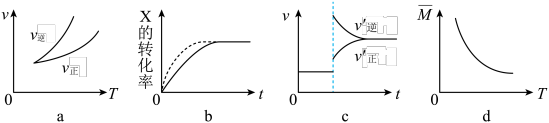
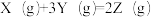 ,有关下列图像的说法错误的是
,有关下列图像的说法错误的是
| A.依据图a可判断正反应为放热反应 |
| B.在图b中,虚线可表示使用了催化剂 |
| C.若正反应的△H<0,图c可表示升高温度使平衡向逆反应方向移动 |
| D.由图d中混合气体的平均相对分子质量随温度的变化情况,可推知正反应的△H>0 |
您最近一年使用:0次
2023-11-06更新
|
228次组卷
|
6卷引用:浙江省海盐第二高级中学2022-2023学年高二上学期10月第一阶段检测化学试题
名校
4 . 在一个体积为 2L 的密闭容器中发生以下反应: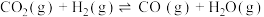 ,其平衡常数(K)和温度(t)的关系如下表所示
,其平衡常数(K)和温度(t)的关系如下表所示
(1)该反应的平衡常数表达式 K= ___________ ;该反应___________ 反应(填“吸热”或“放热”)
(2)600℃时,向容器中充入 1mol H2和 1mol CO2 气体,平衡时 CO 气体有 0.4mol,则 600℃时K=___________
(3)在 830℃向容器中充入 2mol CO 和 2mol H2O,保持温度不变,5 分钟后反应达到平衡后,其平衡常数___________ (填“大于”“小于”或“等于”)1,此时 H2O 的转化率为 ___________ 。
(4)若 1000℃时,某时刻反应混合物中 CO2、H2、CO、H2O 物质的量分别为 2mol 、2mol 、4mol 、4mol ,则此时上述反应的平衡移动方向为___________ (填“正反应方向”“逆反应方向”或“不移动”)
(5)为提高平衡时 H2的转化率,除了适当控制反应温度,还可以采取的措施是___________ 。
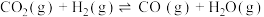 ,其平衡常数(K)和温度(t)的关系如下表所示
,其平衡常数(K)和温度(t)的关系如下表所示| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(2)600℃时,向容器中充入 1mol H2和 1mol CO2 气体,平衡时 CO 气体有 0.4mol,则 600℃时K=
(3)在 830℃向容器中充入 2mol CO 和 2mol H2O,保持温度不变,5 分钟后反应达到平衡后,其平衡常数
(4)若 1000℃时,某时刻反应混合物中 CO2、H2、CO、H2O 物质的量分别为 2mol 、2mol 、4mol 、4mol ,则此时上述反应的平衡移动方向为
(5)为提高平衡时 H2的转化率,除了适当控制反应温度,还可以采取的措施是
您最近一年使用:0次
2023-10-07更新
|
77次组卷
|
3卷引用:浙江省杭州市精诚联盟2023-2024学年高二上学期10月月考化学试题
名校
解题方法
5 . 利用CO2合成乙烯的反应原理为: ,往恒压密闭容器中按n(CO2)∶n(H2)=1∶3充入气体,在常压和催化剂作用下进行反应。测得温度对CO2平衡转化率和催化剂催化效率影响情况如图所示。下列说法不正确的是
,往恒压密闭容器中按n(CO2)∶n(H2)=1∶3充入气体,在常压和催化剂作用下进行反应。测得温度对CO2平衡转化率和催化剂催化效率影响情况如图所示。下列说法不正确的是

 ,往恒压密闭容器中按n(CO2)∶n(H2)=1∶3充入气体,在常压和催化剂作用下进行反应。测得温度对CO2平衡转化率和催化剂催化效率影响情况如图所示。下列说法不正确的是
,往恒压密闭容器中按n(CO2)∶n(H2)=1∶3充入气体,在常压和催化剂作用下进行反应。测得温度对CO2平衡转化率和催化剂催化效率影响情况如图所示。下列说法不正确的是
| A.该反应△H<0,平衡常数:KM>KN |
| B.反应速率有可能是(M)>(N) |
| C.温度越低,反应一定时间后CO2的转化率越高 |
| D.若投料比改为n(CO2)∶n(H2)=1∶4,可提高CO2的平衡转化率 |
您最近一年使用:0次
2023-09-17更新
|
212次组卷
|
2卷引用:浙江省海宁市高级中学2022-2023学年高二上学期10月月考化学试题
名校
解题方法
6 . 利用水煤气合成甲醇的反应原理为: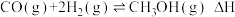 ,一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变温度或压强时,平衡后甲醇的体积分数φ(CH3OH)变化趋势如图所示。下列说法不正确的是
,一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变温度或压强时,平衡后甲醇的体积分数φ(CH3OH)变化趋势如图所示。下列说法不正确的是

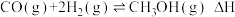 ,一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变温度或压强时,平衡后甲醇的体积分数φ(CH3OH)变化趋势如图所示。下列说法不正确的是
,一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变温度或压强时,平衡后甲醇的体积分数φ(CH3OH)变化趋势如图所示。下列说法不正确的是
| A.该反应△H<0 |
| B.图中压强的大小关系是a<b<c<d |
| C.CH3OH的体积分数越大,平衡常数越大 |
| D.恒温恒压时,往平衡体系中再充入1mol甲醇,重新平衡后甲醇的体积分数不变 |
您最近一年使用:0次
2023-09-17更新
|
411次组卷
|
4卷引用:浙江省海宁市高级中学2022-2023学年高二上学期10月月考化学试题
浙江省海宁市高级中学2022-2023学年高二上学期10月月考化学试题江西省宜春市宜丰中学创新部2023-2024学年高三上学期期中考试化学试题2024届河南省郑州市宇华实验学校高三一模化学试题(已下线)专题06 化学反应速率与化学平衡-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
7 . 化学与日常生活息息相关。下列说法错误的是
| A.使用含氟牙膏能预防龋齿 | B.晶体硅可用于制造光导纤维 |
| C.可用食醋除去水垢中的碳酸钙 | D.食品添加剂不应降低食品本身营养价值 |
您最近一年使用:0次
名校
解题方法
8 . 以 为代表的温室气体大量排放易导致极端天气的出现,减少碳排放,推进碳中和,提升
为代表的温室气体大量排放易导致极端天气的出现,减少碳排放,推进碳中和,提升 的综合利用技术,降低空气中
的综合利用技术,降低空气中 的含量显得刻不容缓。目前
的含量显得刻不容缓。目前 的综合利用技术常用的有如下三种:
的综合利用技术常用的有如下三种:
一、光催化技术
(1)中国广州分析测试中心研究团队在温和条件下用 合成
合成 ,方程式为:
,方程式为: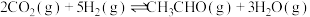
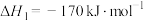
已知生成乙醛的净反应速率为 (
( 、
、 分别表示正、逆反应速率常数)。若在某一温度下
分别表示正、逆反应速率常数)。若在某一温度下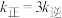 ,则此温度下,上述反应的平衡常数
,则此温度下,上述反应的平衡常数
__________ 。
二、电化学技术
(2)研究证明 也可在熔融碳酸钠中通过电解生成
也可在熔融碳酸钠中通过电解生成 ,收集
,收集 可进行其他有机类合成,化废为宝。则生成
可进行其他有机类合成,化废为宝。则生成 的电极反应式是
的电极反应式是____________________ 。
三、化学催化技术
恒温、体积不变的密闭容器中,加入一定量的 和
和 ,在催化剂下同时发生反应Ⅰ、Ⅱ。
,在催化剂下同时发生反应Ⅰ、Ⅱ。
反应Ⅰ
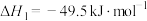
反应Ⅱ
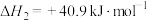
回答下列问题:
(3)下列说法不正确 的是__________。
(4)其他条件相同,仅改变容器体积,实验测得 的平衡产率随着压强的增加而减少,可能原因是
的平衡产率随着压强的增加而减少,可能原因是________________ 。
(5)在一定条件下,选择合适的催化剂只进行反应Ⅱ,调整 和
和 初始投料比,测得在一定投料比和一定温度下,
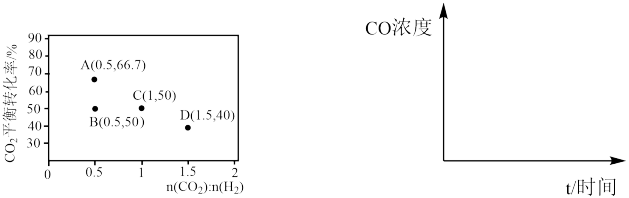
初始投料比,测得在一定投料比和一定温度下, 的平衡转化率如图所示(各点对应的反应温度可能相同,也可能不同)。
的平衡转化率如图所示(各点对应的反应温度可能相同,也可能不同)。
①C、D二点对应的反应温度 、
、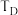 的关系是
的关系是__________ 。
②A、B两点的起始浓度相同,请分别在如图定性画出CO浓度随时间的变化关系,请在曲线上标明 和
和
_______ 。
 为代表的温室气体大量排放易导致极端天气的出现,减少碳排放,推进碳中和,提升
为代表的温室气体大量排放易导致极端天气的出现,减少碳排放,推进碳中和,提升 的综合利用技术,降低空气中
的综合利用技术,降低空气中 的含量显得刻不容缓。目前
的含量显得刻不容缓。目前 的综合利用技术常用的有如下三种:
的综合利用技术常用的有如下三种:一、光催化技术
(1)中国广州分析测试中心研究团队在温和条件下用
 合成
合成 ,方程式为:
,方程式为: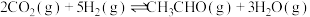
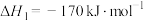
已知生成乙醛的净反应速率为
 (
( 、
、 分别表示正、逆反应速率常数)。若在某一温度下
分别表示正、逆反应速率常数)。若在某一温度下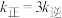 ,则此温度下,上述反应的平衡常数
,则此温度下,上述反应的平衡常数
二、电化学技术
(2)研究证明
 也可在熔融碳酸钠中通过电解生成
也可在熔融碳酸钠中通过电解生成 ,收集
,收集 可进行其他有机类合成,化废为宝。则生成
可进行其他有机类合成,化废为宝。则生成 的电极反应式是
的电极反应式是三、化学催化技术
恒温、体积不变的密闭容器中,加入一定量的
 和
和 ,在催化剂下同时发生反应Ⅰ、Ⅱ。
,在催化剂下同时发生反应Ⅰ、Ⅱ。反应Ⅰ

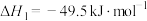
反应Ⅱ

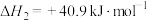
回答下列问题:
(3)下列说法
A.反应Ⅰ的活化能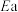 大于反应Ⅱ 大于反应Ⅱ | B.容器内压强不变时可以判断反应达到平衡 |
C.该温度下,反应Ⅱ的 大于零 大于零 | D.使用性能更佳的催化剂可以提高 平衡转化率 平衡转化率 |
 的平衡产率随着压强的增加而减少,可能原因是
的平衡产率随着压强的增加而减少,可能原因是(5)在一定条件下,选择合适的催化剂只进行反应Ⅱ,调整
 和
和 初始投料比,测得在一定投料比和一定温度下,
初始投料比,测得在一定投料比和一定温度下, 的平衡转化率如图所示(各点对应的反应温度可能相同,也可能不同)。
的平衡转化率如图所示(各点对应的反应温度可能相同,也可能不同)。①C、D二点对应的反应温度
 、
、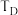 的关系是
的关系是②A、B两点的起始浓度相同,请分别在如图定性画出CO浓度随时间的变化关系,请在曲线上标明
 和
和

您最近一年使用:0次
名校
解题方法
9 . 氢气是一种理想的能源,探索绿色化制氢是化学界一个热门话题。(本题反应中涉及 、
、 、
、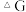 均为298K条件值)。
均为298K条件值)。
(1)传统制备氢气方法之一为水煤气法: ,该反应自发进行的条件是
,该反应自发进行的条件是___________ 。
(2)利用生物质可再生资源乙醇制备氢气具有良好的开发前景。乙醇在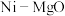 催化下,制取氢气有如下方法:
催化下,制取氢气有如下方法:
方法a:水蒸气催化重整


方法b:部分催化重整

已知:298K时,相关物质的相对能量如图1。

①依据图1数据,计算方法b反应的 =
=___________ 
②已知体系自由能变化: 时反应自发进行。请从
时反应自发进行。请从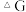 的角度分析方法a、b哪个更有利?
的角度分析方法a、b哪个更有利?___________ 。
③在某恒温和恒压( )体系中,
)体系中, 和
和 以系数比投料进行方法a制氢,若平衡时
以系数比投料进行方法a制氢,若平衡时 的产率为50%,该条件下方法a反应的平衡常数
的产率为50%,该条件下方法a反应的平衡常数 =
=___________ 。[如 的平衡压强
的平衡压强 为平衡系统中
为平衡系统中 的物质的量分数,p为平衡时总压]
的物质的量分数,p为平衡时总压]
(3)有化学工作者提出,在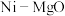 催化剂中添加纳米
催化剂中添加纳米 强化,开展“催化氧化重整”制氢,是一种优化的制氢方法。
强化,开展“催化氧化重整”制氢,是一种优化的制氢方法。
方法c: 下列有关说法正确的是___________。
下列有关说法正确的是___________。
 、
、 、
、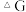 均为298K条件值)。
均为298K条件值)。(1)传统制备氢气方法之一为水煤气法:
 ,该反应自发进行的条件是
,该反应自发进行的条件是(2)利用生物质可再生资源乙醇制备氢气具有良好的开发前景。乙醇在
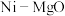 催化下,制取氢气有如下方法:
催化下,制取氢气有如下方法:方法a:水蒸气催化重整



方法b:部分催化重整


已知:298K时,相关物质的相对能量如图1。

①依据图1数据,计算方法b反应的
 =
=
②已知体系自由能变化:
 时反应自发进行。请从
时反应自发进行。请从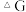 的角度分析方法a、b哪个更有利?
的角度分析方法a、b哪个更有利?③在某恒温和恒压(
 )体系中,
)体系中, 和
和 以系数比投料进行方法a制氢,若平衡时
以系数比投料进行方法a制氢,若平衡时 的产率为50%,该条件下方法a反应的平衡常数
的产率为50%,该条件下方法a反应的平衡常数 =
= 的平衡压强
的平衡压强 为平衡系统中
为平衡系统中 的物质的量分数,p为平衡时总压]
的物质的量分数,p为平衡时总压](3)有化学工作者提出,在
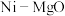 催化剂中添加纳米
催化剂中添加纳米 强化,开展“催化氧化重整”制氢,是一种优化的制氢方法。
强化,开展“催化氧化重整”制氢,是一种优化的制氢方法。方法c:
 下列有关说法正确的是___________。
下列有关说法正确的是___________。A.方法c制氢时,充分提高廉价原料 的浓度,一定能增加氢气产率 的浓度,一定能增加氢气产率 |
| B.方法c与a比,相同条件下方法c能耗更低,制氢速率更快 |
C.乙醇制氢的三种方法中原子利用率(期望产物的总质量与生成物总质量之比)大小关系为: |
D.方法c相当于方法b与水煤气变换 的优化组合。水醇比 的优化组合。水醇比 对乙醇平衡转化率有较大影响 对乙醇平衡转化率有较大影响 |
您最近一年使用:0次
名校
解题方法
10 . 苯乙烯是一种重要的有机化工原料,可广泛用于合成橡胶,工程塑料及制药等。工业上可通过乙苯催化脱氢来制取苯乙烯,反应方程式如下:
___________ 。
(2)下列关于该反应的说法不正确的是___________。
(3)工业上通入过热水蒸气 ,在常压的条件下发生乙苯的催化脱氢反应
,在常压的条件下发生乙苯的催化脱氢反应
①反应中通入水蒸气的作用是___________
②将乙苯和水蒸气通入反应器,其中乙苯的物质的量分数为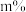 ,在温度t、压强p下进行反应。平衡时,乙苯的转化率为
,在温度t、压强p下进行反应。平衡时,乙苯的转化率为 ,该反应的平衡常数
,该反应的平衡常数
___________ (分压 总压
总压 物质的量分数)
物质的量分数)
(4)保持温度为 ,向体积不等的恒容密闭容器中加入一定量的乙苯发生反应,反应
,向体积不等的恒容密闭容器中加入一定量的乙苯发生反应,反应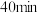 后测得各容器中乙苯的转化率与容器体积的关系如图所示,画出
后测得各容器中乙苯的转化率与容器体积的关系如图所示,画出 之间乙苯的平衡转化率变化曲线
之间乙苯的平衡转化率变化曲线___________ 。

 ;
;

| 物质 | 乙苯 | 苯乙烯 | 氢气 |
燃烧热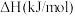 |  |  |  |
| A.高温、低压有利于该反应平衡正向进行 |
| B.高温恒压条件下,乙苯可能会裂解产生积碳覆盖在催化剂的表面,使催化效果下降 |
| C.恒温恒容条件下,反应达到平衡后,向体系中再充入乙苯蒸气,乙苯的转化率将增大 |
| D.选择合适的催化剂可以缩短达到平衡的时间,可使乙苯的平衡转化率变大 |
 ,在常压的条件下发生乙苯的催化脱氢反应
,在常压的条件下发生乙苯的催化脱氢反应①反应中通入水蒸气的作用是
②将乙苯和水蒸气通入反应器,其中乙苯的物质的量分数为
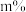 ,在温度t、压强p下进行反应。平衡时,乙苯的转化率为
,在温度t、压强p下进行反应。平衡时,乙苯的转化率为 ,该反应的平衡常数
,该反应的平衡常数
 总压
总压 物质的量分数)
物质的量分数)(4)保持温度为
 ,向体积不等的恒容密闭容器中加入一定量的乙苯发生反应,反应
,向体积不等的恒容密闭容器中加入一定量的乙苯发生反应,反应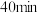 后测得各容器中乙苯的转化率与容器体积的关系如图所示,画出
后测得各容器中乙苯的转化率与容器体积的关系如图所示,画出 之间乙苯的平衡转化率变化曲线
之间乙苯的平衡转化率变化曲线
您最近一年使用:0次
2023-04-27更新
|
165次组卷
|
2卷引用:浙江省海宁市高级中学2023-2024学年高二下学期3月月考化学试题



