名校
解题方法
1 . 在恒压、NO和O2的起始浓度一定的条件下, 催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是
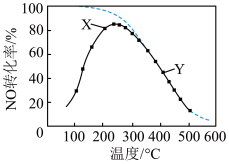
| A.反应2NO(g)+O2(g)=2NO2(g)的 ΔH>0 |
| B.图中X点所示条件下,延长反应时间能提高NO转化率 |
| C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率 |
| D.380℃下,c起始(O2)=5.0 ×10-4 mol·L-1, NO平衡转化率为50%,则平衡常数K<2000 |
您最近一年使用:0次
2021-06-20更新
|
436次组卷
|
11卷引用:河北省石家庄市河北正定中学2024届高三上学期第二次月考化学试题
河北省石家庄市河北正定中学2024届高三上学期第二次月考化学试题江苏省镇江中学2020-2021学年高二上学期期末考试化学试题(已下线)【镇江新东方】高二下期中21高二期中校级联考江苏省扬州市江都区大桥高级中学2020-2021学年高二下学期学情检测(二)化学试题贵州省毕节市金沙县第一中学2021-2022学年高二上学期期中考试化学试题河南省范县第一中学2021-2022学年高二上学期期中检测化学试题内蒙古霍林郭勒市第一中学2021-2022学年高二上学期期中考试化学试题山西省晋中市平遥县第二中学校2021-2022学年高二上学期期中考试化学试题福建省宁德第一中学2022-2023学年高二上学期第二次月考化学试题福建省厦门市第一中学2021-2022学年高二上学期 期中考试化学试卷江苏省南京市第一中学2023-2024学年高一下学期期中考试化学试卷
2 . 一定条件下,当反应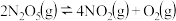 达到平衡时,通入
达到平衡时,通入 一定时间后,下列物质中存在
一定时间后,下列物质中存在 的是
的是
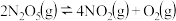 达到平衡时,通入
达到平衡时,通入 一定时间后,下列物质中存在
一定时间后,下列物质中存在 的是
的是A.只有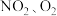 | B.只有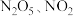 |
C.只有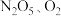 | D.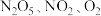 |
您最近一年使用:0次
2021-06-20更新
|
344次组卷
|
6卷引用:【石家庄新东方】河北省沧衡八校联盟2020-2021学年高一下学期期中考试化学试题
3 . 已知: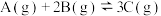
 ,向一恒温恒容的密闭容器中充入
,向一恒温恒容的密闭容器中充入 和
和 发生反应,
发生反应, 时达到平衡状态I,在
时达到平衡状态I,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
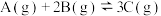
 ,向一恒温恒容的密闭容器中充入
,向一恒温恒容的密闭容器中充入 和
和 发生反应,
发生反应, 时达到平衡状态I,在
时达到平衡状态I,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是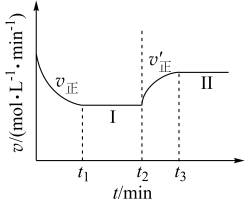
| A.容器内压强不变,表明反应达到平衡 |
B. 时改变的条件:向容器中加入C 时改变的条件:向容器中加入C |
C.平衡时A的体积分数 : :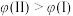 |
D.平衡常数K: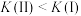 |
您最近一年使用:0次
2021-06-09更新
|
9290次组卷
|
49卷引用:河北省衡水中学2021-2022学年高二上学期8月份线上调研化学试题
河北省衡水中学2021-2022学年高二上学期8月份线上调研化学试题2021年新高考湖南化学高考真题山东省临沂市沂水县第一中学2020-2021学年高二下学期期末检测化学试题(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时38 化学平衡常规图像-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第20讲 化学平衡常数及转化率的计算(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第19讲 化学平衡(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)湖南省常德市第一中学2021-2022学年高二上学期第一次月考化学试题(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)2021年湖南省高考化学试卷变式题11-19(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题12 化学反应速率与化学平衡-2022年高考化学二轮复习重点专题常考点突破练河南省郑州市第四高级中学2021-2022学年高二下学期第二次调研考试化学试题(已下线)秘籍07 化学反应速率及平衡图象剖析-备战2022年高考化学抢分秘籍(全国通用)(已下线)押新高考卷09题 速率和平衡-备战2022年高考化学临考题号押题(新高考通版)(已下线)回归教材重难点06 化学反应速率与化学平衡-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点07 图像数据和结果的分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题09 化学反应速率、化学平衡-三年(2020-2022)高考真题分项汇编广东省揭阳市普宁市华侨中学2021-2022学年高二下学期第三次月考化学试题(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第22讲 化学平衡常数及转化率的计算(练)-2023年高考化学一轮复习讲练测(全国通用)第二章 综合拔高练(已下线)第20讲 化学平衡常数及转化率的计算(讲)-2023年高考化学一轮复习讲练测(新教材新高考)湖南省宁远县第一中学2022-2023学年高二上学期第一次适应性考试化学试题湖南省湘潭凤凰中学2022-2023学年高二上学期10月月考化学试题贵州省黔东南州凯里市第一中学2022-2023学年高二上学期期中考试化学试题湖南省长沙市长郡中学2022-2023学年高二上学期期中考试化学试题湖南省临湘市第五中学2021-2022学年高二上学期第三次月考化学试题安徽省桐城中学2022-2023学年高二上学期月考(1)化学试题湖南省郴州市永兴县童星学校2022-2023学年高二上学期9月月考化学试题河南省郑州市2021-2022学年高二上学期期末考试化学试题湖南省怀化市第三中学2022-2023学年高二上学期期中考试化学试题湖南省株洲市第二中学2022-2023学年高二上学期期中考试化学试题(已下线)专题09 化学反应速率与化学平衡(练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题17 化学平衡图表分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)化学反应速率与化学平衡——进阶学习(已下线)题型124 突破化学反应速率和化学平衡图像题(已下线)专题15 化学平衡图像-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)题型23 平衡常数、平衡转化率图象(已下线)专题08 反应速率与化学平衡-2023年高考化学真题题源解密(新高考专用)(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点3 化学平衡常数及转化率的计算(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)山东省青岛莱西市2022-2023学年高二上学期期中考试化学试题河南省周口恒大中学2023-2024学年高三下学期4月期中考试化学试题
4 . SO2与O2在一定条件下合成SO3的反应,达到平衡时变化关系如图所示,下列说法错误的是

A.反应的方程式为2SO2+O2 2SO3 2SO3 |
| B.达到平衡时SO2与O2的转化率之比为1:1 |
| C.达到平衡时,断开SO2的硫氧键的个数是断开O2的氧氧键个数的4倍 |
| D.达到平衡时,增大SO2的物质的量浓度可提高反应物的转化率 |
您最近一年使用:0次
解题方法
5 . 利用含钴废料(主要成分为Co3O4,还含有少量的铝箔、LiCoO2等杂质)制备碳酸钴的工艺流程如图:

已知:萃取Co2+的反应原理:Co2++2HR(有机磷) CoR2+2H+。下列说法错误的是
CoR2+2H+。下列说法错误的是

已知:萃取Co2+的反应原理:Co2++2HR(有机磷)
 CoR2+2H+。下列说法错误的是
CoR2+2H+。下列说法错误的是| A.“滤液Ⅰ”中溶质的主要成分是Na[Al(OH)4] |
| B.“酸溶”中H2O2的作用是将Co2+氧化为Co3+ |
| C.“反萃取”中可加入H2SO4分离出Co2+ |
| D.“沉钴”时增大Na2CO3溶液的浓度或滴加速率,能够提高产品的纯度 |
您最近一年使用:0次
2021-05-25更新
|
943次组卷
|
2卷引用:河北省部分学校2022-2023学年高三上学期10月期中考试化学试题
20-21高二下·广东广州·阶段练习
名校
6 . 进入实验室后,一切行动听指挥。不听老师指挥或者不听课的同学就容易做错这一题。下列实验设计或实验现象描述正确的是
①水溶液中,K2Cr2O7存在以下平衡:Cr2O +H2O
+H2O CrO
CrO +2H+,加入2-3滴NaOH溶液,溶液变黄
+2H+,加入2-3滴NaOH溶液,溶液变黄
②探究温度对反应速率的影响:在两支试管中分别混合等体积、同浓度的Na2S2O3溶液和稀硫酸,一支放在热水中,另一支放在冰水中,观察出现浑浊的先后
③[Cu(H2O)4]2+(蓝色)+4C1- [CuCl4]2-(黄色)+4H2OΔH>0,升高温度,溶液由蓝色变成黄色
[CuCl4]2-(黄色)+4H2OΔH>0,升高温度,溶液由蓝色变成黄色
④把装有NO2与N2O4混合气体的平衡球一端置于冷水,一端置于热水中,置于冷水中的颜色更深
⑤实验室用足量的Zn和稀硫酸反应制备H2,加入几滴CuSO4溶液,反应速率加快,产生H2的量不变
①水溶液中,K2Cr2O7存在以下平衡:Cr2O
 +H2O
+H2O CrO
CrO +2H+,加入2-3滴NaOH溶液,溶液变黄
+2H+,加入2-3滴NaOH溶液,溶液变黄②探究温度对反应速率的影响:在两支试管中分别混合等体积、同浓度的Na2S2O3溶液和稀硫酸,一支放在热水中,另一支放在冰水中,观察出现浑浊的先后
③[Cu(H2O)4]2+(蓝色)+4C1-
 [CuCl4]2-(黄色)+4H2OΔH>0,升高温度,溶液由蓝色变成黄色
[CuCl4]2-(黄色)+4H2OΔH>0,升高温度,溶液由蓝色变成黄色④把装有NO2与N2O4混合气体的平衡球一端置于冷水,一端置于热水中,置于冷水中的颜色更深
⑤实验室用足量的Zn和稀硫酸反应制备H2,加入几滴CuSO4溶液,反应速率加快,产生H2的量不变
| A.②④⑤ | B.②③⑤ | C.①⑤ | D.①②④ |
您最近一年使用:0次
名校
7 . 相同温度和压强下,研究Cl2在不同溶液中的溶解度(用溶解Cl2的物质的量浓度表示)随溶液浓度的变化。在NaCl溶液和盐酸中Cl2的溶解度以及各种含氯微粒的浓度变化如图。

下列说法不正确的是

下列说法不正确的是
A.由图1可知,Cl2溶于NaCl溶液时还发生了反应Cl2+Cl-=Cl |
| B.随NaCl溶液浓度增大,Cl2+H2O⇌H++Cl-+HClO平衡逆移,Cl2溶解度减小 |
C.随盐酸浓度增加Cl2与H2O的反应被抑制,生成Cl 为主要反应从而促进Cl2溶解 为主要反应从而促进Cl2溶解 |
| D.由上述实验可知,H+浓度增大促进Cl2溶解,由此推知在稀硫酸中,随硫酸浓度增大Cl2的溶解度会增大 |
您最近一年使用:0次
2021-05-20更新
|
2169次组卷
|
15卷引用:河北省武邑中学2021届高考七模化学试题
河北省武邑中学2021届高考七模化学试题北京市西城区2021届高三一模化学试题(已下线)【一飞冲天】7.塘沽一中模拟(已下线)专题11 富集在海水中的元素——氯 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练(已下线)2.3.1 浓度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)辽宁省实验中学2022届高三第一次阶段性考试化学试题(已下线)专题07 常见非金属及其化合物-备战2022年高考化学学霸纠错(全国通用)天津市滨海新区塘沽第一中学2021-2022学年高三上学期期中考试化学试题山东省滕州第一中学2021-2022学年高三上学期第一学段模块考试(期中)化学试题苏州市相城区陆慕高级中学2021-2022学年高二下学期4月线上教学质量检测化学试题辽宁省沈阳市沈阳二中2023届高三上学期8月阶段测试化学试题辽宁省沈阳市东北育才学校高三上学期10月第一次模拟考试化学试题江苏省扬州市宝应县2022-2023学年高二上学期期中检测化学(选修)试题北京市首都师范大学附属中学2023-2024学年高三上学期10月月考化学试题北京市中国人民大学附属中学2023-2024学年高三下学期一模模拟化学试题
名校
8 . 已知重铬酸根和铬酸根离子间存在如下平衡: +H2O
+H2O 2
2 +2H+。向试管中加入4 mL0. lmol·L-1K2Cr2O7溶液。下列说法正确的是
+2H+。向试管中加入4 mL0. lmol·L-1K2Cr2O7溶液。下列说法正确的是
 +H2O
+H2O 2
2 +2H+。向试管中加入4 mL0. lmol·L-1K2Cr2O7溶液。下列说法正确的是
+2H+。向试管中加入4 mL0. lmol·L-1K2Cr2O7溶液。下列说法正确的是| A.向试管中加水,平衡向右移动,c(H+)增大 |
| B.向该试管中滴加数滴1 mol·L-1 NaOH溶液,溶液由橙色变为黄色 |
| C.向K2Cr2O7强酸性溶液中加入FeSO4固体,平衡正向移动 |
D.加入催化剂,可提高平衡时 的浓度 的浓度 |
您最近一年使用:0次
名校
9 . 已知[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:[Co(H2O)6]2++4Cl-⇌[CoCl4]2-+6H2OΔH,用该溶液做实验,溶液的颜色变化如图:

以下结论和解释错误的是

以下结论和解释错误的是
| A.由实验①可推知ΔH>0 |
| B.等物质的量的[Co(H2O)6]2+和[CoCl4]2-中σ键数之比为9∶2 |
| C.实验②是由于c(H2O)增大,导致平衡逆向移动 |
| D.由实验③可知配离子的稳定性:[ZnCl4]2->[CoCl4]2- |
您最近一年使用:0次
2021-04-07更新
|
172次组卷
|
5卷引用:河北省衡水市武强中学2020-2021学年高二下学期第一次月考化学试题
名校
10 .  (g)+
(g)+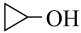 (g)
(g)
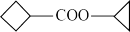 (g)+HCl(g)是制备酯类物质的重要有机反应,下列对相关图象做出的判断正确的是
(g)+HCl(g)是制备酯类物质的重要有机反应,下列对相关图象做出的判断正确的是
 (g)+
(g)+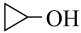 (g)
(g)
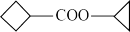 (g)+HCl(g)是制备酯类物质的重要有机反应,下列对相关图象做出的判断正确的是
(g)+HCl(g)是制备酯类物质的重要有机反应,下列对相关图象做出的判断正确的是| A | B | C | D |
 | 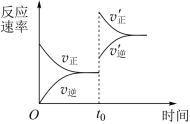 | 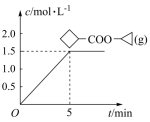 |  |
| 升高温度,平衡向逆反应方向移动 | t1时改变的条件可能为增大 的浓度 的浓度 | 0~5min内,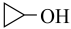 的平均反应速率为0.3mol•L-1•min-1 的平均反应速率为0.3mol•L-1•min-1 | x可能为压强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



