名校
1 . 某温度下,在2 L的密闭容器中,充入4 mol A和2 mol B进行如下反应:3A(g)+2B(g)⇌4C(s)+2D(g),反应一段时间达到平衡,测得生成1.6 mol C,则下列说法正确的是
| A.增大压强,平衡向逆反应方向移动 |
B.达平衡后B的转化率为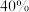 |
| C.增加A,平衡正向移动,化学平衡常数增大 |
| D.若升高温度,A的转化率增大,则该反应∆H<0 |
您最近一年使用:0次
2021-11-18更新
|
692次组卷
|
8卷引用:江西省赣州市2022-2023学年高三上学期期末考试化学试题
江西省赣州市2022-2023学年高三上学期期末考试化学试题黑龙江省大庆市2022届高三上学期第一次教学质量检测化学试题天津市和平区2021~2022学年高三上学期期末考试化学试题(已下线)一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)(已下线)一轮巩固卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)黑龙江省肇东市第四中学2021-2022学年高三12月月考化学试题天津市第一中学2023-2024学年高二上学期10月月考化学试题黑龙江省大庆市2023-2024学年高三上学期第一次模拟考试化学试题
解题方法
2 . 由实验操作和现象,可得出相应正确结论的是
| 实验操作 | 现象 | 结论 | |
| A | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 | 先变橙色,后变蓝色 | 氧化性: Cl2>Br2>I2 |
| B | 将铁锈溶于浓盐酸,再滴加酸性高锰酸钾溶液 | 高锰酸钾溶液的紫色褪去 | 铁锈中含有二价铁 |
| C | 向铬酸钾溶液中缓慢滴加硫酸 | 黄色变为橙红色 |  +H2O +H2O 2 2 +2H+,增大氢离子浓度,平衡向生成 +2H+,增大氢离子浓度,平衡向生成 和的方向移动 和的方向移动 |
| D | 向蔗糖溶液中滴加稀硫酸,水浴加热,再加入新制Cu(OH)2悬浊液 | 无砖红色沉淀 | 蔗糖未发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9-10高二下·浙江金华·期末
名校
3 . 将等物质的量的X、Y气体充入某密闭容器中,一定条件下,发生如下反应并达到平衡: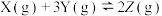
 ,改变某个条件并维持新条件直至达到新的平衡,表中关于新平衡与原平衡的比较正确的是
,改变某个条件并维持新条件直至达到新的平衡,表中关于新平衡与原平衡的比较正确的是
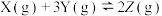
 ,改变某个条件并维持新条件直至达到新的平衡,表中关于新平衡与原平衡的比较正确的是
,改变某个条件并维持新条件直至达到新的平衡,表中关于新平衡与原平衡的比较正确的是| 选项 | 改变的条件 | 新平衡与原平衡比较 |
| A | 升高温度 | X的转化率变小 |
| B | 增大压强(压缩体积) | X的浓度变小 |
| C | 充入一定量Y | Y的转化率增大 |
| D | 使用适当催化剂 | X的体积分数变小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-08-01更新
|
924次组卷
|
23卷引用:2014-2015江西省奉新县第一中学高二上学期期末化学试卷
2014-2015江西省奉新县第一中学高二上学期期末化学试卷2017届江西省九江一中高三上学期月考二化学试卷(已下线)2010年6月浙江金华四校高二期末测试化学试题(已下线)2014届黑龙江省牡丹江一中高二上学期期末考试化学试卷2014-2015黑龙江省桦南培黎学校高二上学期期末考试化学试卷湖南省长沙市第一中学2017-2018学年高二上学期期中考试化学试题广东省惠州市2017-2018学年高二上学期期末教学质量检测(理)化学试题(已下线)2018年9月25日《每日一题》一轮复习-化学平衡的移动河南省洛阳市2018-2019学年高二第一学期期中考试化学试题广东省惠州市2018-2019学年高二上学期期末考试化学(理科)试题人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时3 影响化学平衡的因素宁夏海原第一中学2020-2021学年高二上学期第二次月考化学试题(已下线)专题10 化学平衡(速率、影响因素、图像、标志、平衡压强及常数)-2021年高考化学必做热点专题选择性必修1(SJ)专题2第三单元 化学平衡的移动(已下线)考向22 化学平衡状态 化学平衡的移动-备战2022年高考化学一轮复习考点微专题安徽省六安市第一中学2021-2022学年高二下学期开学考试化学试题湖南省长沙市宁乡市2020-2021学年高二下学期期末调研考试化学试题陕西省西安市雁塔区第二中学2021-2022学年高二上学期第一次月考化学试题福建省泉州市第六中学2021-2022学年高二上学期期中模块测试化学试题(已下线)第七章 化学反应速率与化学平衡 第43练 化学平衡移动原理及应用2.3.2温度 催化剂对化学平衡的影响 课中第3课时 温度、催化剂对化学平衡的影响广东省惠州市2023-2024学年高三上学期第三次调研化学试题
名校
解题方法
4 . 用下列装置不能达到实验目的的是
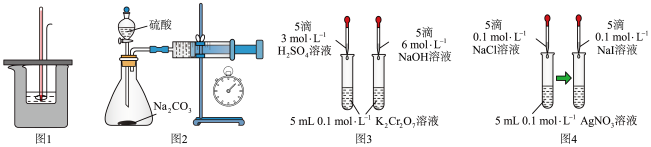

| A.图1:测量强酸强碱中和反应的反应热 |
B.图2:测定 和稀硫酸反应的速率 和稀硫酸反应的速率 |
| C.图3:验证浓度对化学平衡的影响 |
D.图4:证明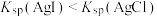 |
您最近一年使用:0次
2023-01-14更新
|
360次组卷
|
3卷引用:江西省丰城市第九中学2022-2023学年高一下学期期末考试化学试题
名校
5 . 某学习小组欲利用 平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
 溶液和20 mL 0.015 mol⋅L
溶液和20 mL 0.015 mol⋅L KSCN溶液混合,得血红色溶液X,进行下列实验:
KSCN溶液混合,得血红色溶液X,进行下列实验:
实验Ⅰ.改变 、
、 、
、 、
、 等离子浓度对平衡的影响
等离子浓度对平衡的影响
(1)取2 mL溶液X,加入5滴0.01 mol⋅L KSCN溶液,溶液红色
KSCN溶液,溶液红色_______ (填“变深”、“变浅”或“不变”,下同);取2 mL溶液X,插入经砂纸打磨过的铁丝,溶液红色_______ 。基于上述两个实验可以得到的结论是_______ 。
(2)取2 mL溶液X,加入5滴0.03 mol⋅L KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是
KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是_______ 或者不直接参与平衡体系的 或
或 对平衡产生了影响。
对平衡产生了影响。
实验Ⅱ.探究KCl对 平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
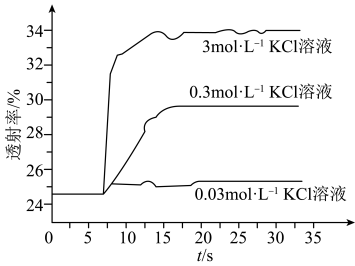
(3)上述实验可以得到以下结论:一是KCl对 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响_______ 。二是_______ 。
(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①: 产生的影响。
产生的影响。
猜想②: 产生的影响。
产生的影响。
猜想③:_______ 。
实验Ⅲ.探究盐对 和
和 平衡体系产生的影响
平衡体系产生的影响
资料信息:
a.溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
b.在 溶液中存在反应
溶液中存在反应 。
。
(5)根据上述信息,学习小组同学各取2 mL溶液X,分别加入5滴①去离子水、②0.3 mol⋅L KCl溶液、③0.3 mol⋅L
KCl溶液、③0.3 mol⋅L NaCl溶液、④0.3 mol⋅L
NaCl溶液、④0.3 mol⋅L
 溶液、⑤3 mol⋅L
溶液、⑤3 mol⋅L HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。

上述实验能证明阳离子盐效应影响 平衡体系的实验组是
平衡体系的实验组是_______ 。盐效应影响较大的阳离子是_______ 。
A.实验①②③ B.实验①②④ C.实验①③④
(6)解释出现实验⑤现象的原因:_______ 。
 平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
平衡体系探究影响平衡的因素,将220 mL 0.005 mol⋅L
 溶液和20 mL 0.015 mol⋅L
溶液和20 mL 0.015 mol⋅L KSCN溶液混合,得血红色溶液X,进行下列实验:
KSCN溶液混合,得血红色溶液X,进行下列实验:实验Ⅰ.改变
 、
、 、
、 、
、 等离子浓度对平衡的影响
等离子浓度对平衡的影响(1)取2 mL溶液X,加入5滴0.01 mol⋅L
 KSCN溶液,溶液红色
KSCN溶液,溶液红色(2)取2 mL溶液X,加入5滴0.03 mol⋅L
 KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是
KCl溶液,观察到溶液红色变浅,产生该现象的原因可能是 或
或 对平衡产生了影响。
对平衡产生了影响。实验Ⅱ.探究KCl对
 平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
平衡体系的影响为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
(3)上述实验可以得到以下结论:一是KCl对
 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①:
 产生的影响。
产生的影响。猜想②:
 产生的影响。
产生的影响。猜想③:
实验Ⅲ.探究盐对
 和
和 平衡体系产生的影响
平衡体系产生的影响资料信息:
a.溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
b.在
 溶液中存在反应
溶液中存在反应 。
。(5)根据上述信息,学习小组同学各取2 mL溶液X,分别加入5滴①去离子水、②0.3 mol⋅L
 KCl溶液、③0.3 mol⋅L
KCl溶液、③0.3 mol⋅L NaCl溶液、④0.3 mol⋅L
NaCl溶液、④0.3 mol⋅L
 溶液、⑤3 mol⋅L
溶液、⑤3 mol⋅L HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
HCl溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
上述实验能证明阳离子盐效应影响
 平衡体系的实验组是
平衡体系的实验组是A.实验①②③ B.实验①②④ C.实验①③④
(6)解释出现实验⑤现象的原因:
您最近一年使用:0次
2023-05-21更新
|
327次组卷
|
2卷引用:江西省萍乡中学、新余市第一中学2023-2024学年高二上学期10月创新班联考化学试题
解题方法
6 . 碘化亚铜(CuI)是重要的有机催化剂。某学习小组用如图装置制备CuI,并设计实验探究其性质。已知:碘化亚铜(CuI)是白色固体,难溶于水,易与KI形成K[CuI2]实验装置如图1所示。
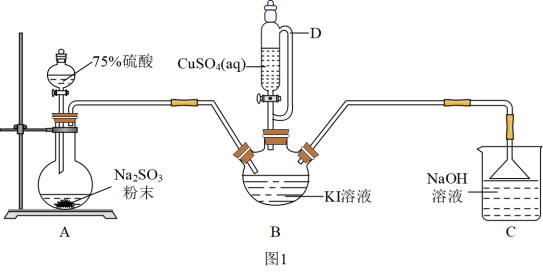
(1)仪器D的名称是________ 。
(2)实验完毕后,用图2所示装置分离CuI的突出优点是_______ 。
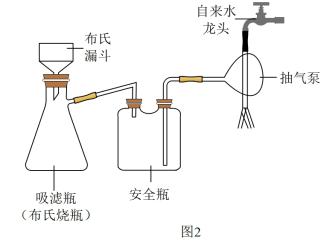
(3)某同学向装置C的烧杯中倾倒NaOH溶液时,不慎将少量溶液溅到皮肤上,处理的方法是:_______ 。
(4)装置B中发生反应的离子方程式是_______ 。
(5)小组同学设计下表方案对CuI的性质进行探究:
①在实验I中“加水,又生成白色沉淀”的原理是_______ 。
②根据实验II,CuI与NaOH溶液反应的化学方程式是_______ 。
(6)测定CuI样品纯度。取a g CuI样品与适量NaOH溶液充分反应后,过滤;在滤液中加入足量的酸化的双氧水,滴几滴淀粉溶液,用b mol/LNa2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液体积为V mL(已知:滴定反应为I2+2 =
= (无色)+2I-)。该样品纯度为
(无色)+2I-)。该样品纯度为_______ (用含a、b、V的代数式表示)。如果其他操作均正确,仅滴定前盛标准液的滴定管用蒸馏水洗净后没有用标准液润洗,测得结果_______ (填“偏高”“偏低”或“无影响”)。

(1)仪器D的名称是
(2)实验完毕后,用图2所示装置分离CuI的突出优点是

(3)某同学向装置C的烧杯中倾倒NaOH溶液时,不慎将少量溶液溅到皮肤上,处理的方法是:
(4)装置B中发生反应的离子方程式是
(5)小组同学设计下表方案对CuI的性质进行探究:
| 实验 | 实验操作及现象 |
| Ⅰ | 取少量CuI放入试管中,加入KI溶液,白色固体溶解得到无色溶液;加水,又生成白色沉淀 |
| Ⅱ | 取少量CuI放入试管中,加入NaOH溶液,振荡,产生砖红色沉淀。过滤,向所得上层清液中滴加淀粉溶液,无明显变化;将砖红色沉淀溶于稀硫酸,产生红色固体和蓝色溶液 |
②根据实验II,CuI与NaOH溶液反应的化学方程式是
(6)测定CuI样品纯度。取a g CuI样品与适量NaOH溶液充分反应后,过滤;在滤液中加入足量的酸化的双氧水,滴几滴淀粉溶液,用b mol/LNa2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液体积为V mL(已知:滴定反应为I2+2
 =
= (无色)+2I-)。该样品纯度为
(无色)+2I-)。该样品纯度为
您最近一年使用:0次
名校
7 . 一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g) 2CO2(g)+S(l) ΔH<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是
2CO2(g)+S(l) ΔH<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是
 2CO2(g)+S(l) ΔH<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是
2CO2(g)+S(l) ΔH<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是| A.平衡前,随着反应的进行,容器内压强始终不变 |
| B.平衡时,其他条件不变,分离出硫,正反应速率加快 |
| C.平衡时,其他条件不变,加入催化剂可提高SO2的转化率 |
| D.平衡后,充入CO和CO2气体,使CO和CO2气体浓度均变为原来的两倍,平衡不移动 |
您最近一年使用:0次
2023-05-16更新
|
308次组卷
|
2卷引用:江西省丰城中学、新建二中2022-2023学年高二下学期期末联考化学试题
名校
8 . 恒容密闭容器中进行反应FeO(s)+CO(g) Fe(s)+CO2(g)
Fe(s)+CO2(g)  H<0。下列说法正确的是
H<0。下列说法正确的是
 Fe(s)+CO2(g)
Fe(s)+CO2(g)  H<0。下列说法正确的是
H<0。下列说法正确的是| A.当混合气体的密度不再变化时,反应达到平衡状态 |
| B.增大CO浓度,因为增大了活化分子百分数,导致反应速率增大 |
| C.该反应在高温下为自发反应 |
| D.平衡时,向容器中加入FeO可促使平衡正向移动 |
您最近一年使用:0次
2023-11-14更新
|
242次组卷
|
3卷引用:江西省上饶市广信二中2023-2024学年高二上学期期中考试化学试卷
名校
9 . 下列事实不能用勒夏特列原理解释的是
A.对于反应2NO2(g) N2O4(g),增大压强(缩小体积),混合气体颜色先变深后变浅 N2O4(g),增大压强(缩小体积),混合气体颜色先变深后变浅 |
| B.H2、I2、HI三者的平衡,混合气体加压(缩小体积),平衡后颜色变深 |
| C.开启汽水瓶后,瓶中马上泛起大量泡沫 |
D.利用反应Na(l)+KCl(l) NaCl(l)+K(g)制取金属钾,选取适宜的温度 NaCl(l)+K(g)制取金属钾,选取适宜的温度 |
您最近一年使用:0次
2023-10-17更新
|
257次组卷
|
3卷引用:江西省广丰中学2023-2024学年高二上学期10月月考化学试题
名校
10 . 甲醇是重要的化工原料,发展前景广阔。研究表明, 加氢可以合成甲醇,反应如下:
加氢可以合成甲醇,反应如下: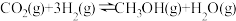
(1)反应的平衡常数表达式为K=___________ 。
(2)有利于提高平衡时 转化率的措施有
转化率的措施有___________ (填字母)。
a.使用催化剂
b.加压
c.增大 和H2的初始投料比
和H2的初始投料比
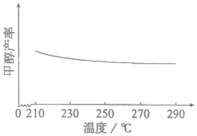
(3)研究温度对甲醇产率的影响时发现,在210~290℃,保持原料气中 和H2的投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的
和H2的投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的
___________ 0(填“>”“=”或“<”),依据是___________ 。
 加氢可以合成甲醇,反应如下:
加氢可以合成甲醇,反应如下: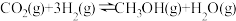
(1)反应的平衡常数表达式为K=
(2)有利于提高平衡时
 转化率的措施有
转化率的措施有a.使用催化剂
b.加压
c.增大
 和H2的初始投料比
和H2的初始投料比(3)研究温度对甲醇产率的影响时发现,在210~290℃,保持原料气中
 和H2的投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的
和H2的投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的

您最近一年使用:0次
2021-12-02更新
|
801次组卷
|
4卷引用:江西省兴国县将军中学有限公司2023-2024学年高二上学期期中考试化学试题(普高部)



