解题方法
1 . 将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如表2组数据:
CO2(g)+H2(g),得到如表2组数据:
(1)实验1中以v(CO2)表示的反应速率为__________ 。
(2)900℃时,反应CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数
CO2(g)+H2(g)的平衡常数_________ 。向实验2的平衡混合物中再加入0.4molH2O(g)和0.4molCO,平衡_________ (选填“正反应方向”、“逆反应方向”或“不”)移动。
 CO2(g)+H2(g),得到如表2组数据:
CO2(g)+H2(g),得到如表2组数据:| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 1 | 2 | 0.8 | 1.2 | 5 |
| 2 | 900 | 0.5 | 1 | 0.2 | 0.8 | 3 |
(2)900℃时,反应CO(g)+H2O(g)
 CO2(g)+H2(g)的平衡常数
CO2(g)+H2(g)的平衡常数
您最近半年使用:0次
2 . 下列事实中,不能用勒夏特列原理解释的是
A.使用催化剂有利于合成氨反应:N2(g)+3H2(g) 2NH3 2NH3 |
B.采用高压有利于合成氨反应:N2(g)+3H2(g) 2NH3 2NH3 |
C.反应CO+NO2 CO2+NO(△H<0),升高温度平衡向逆反应方向移动 CO2+NO(△H<0),升高温度平衡向逆反应方向移动 |
D.氯水中有下列平衡:Cl2+H2O HCl+HClO,当加入AgNO3溶液后溶液颜色变浅 HCl+HClO,当加入AgNO3溶液后溶液颜色变浅 |
您最近半年使用:0次
21-22高二下·宁夏银川·阶段练习
名校
3 . 往 溶液中滴加少量
溶液中滴加少量 溶液,溶液呈红色,发生如下反应:
溶液,溶液呈红色,发生如下反应: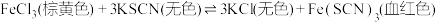 ,下列说法中正确的是
,下列说法中正确的是
 溶液中滴加少量
溶液中滴加少量 溶液,溶液呈红色,发生如下反应:
溶液,溶液呈红色,发生如下反应: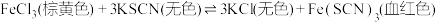 ,下列说法中正确的是
,下列说法中正确的是A.往上述溶液中滴入 溶液,溶液红色变浅 溶液,溶液红色变浅 |
B.往上述溶液中滴入 溶液,溶液红色变浅 溶液,溶液红色变浅 |
| C.往上述溶液中加入铁粉,溶液红色加深 |
D.往上述溶液中滴入 溶液,溶液红色不变 溶液,溶液红色不变 |
您最近半年使用:0次
2023-08-09更新
|
238次组卷
|
4卷引用:6.2.2 化学平衡(第2课时 化学平衡移动)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)
(已下线)6.2.2 化学平衡(第2课时 化学平衡移动)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)宁夏银川市第二中学2021-2022学年高二下学期第一次月考化学试题浙江省台州市台州八校联盟2022-2023学年高二上学期11月期中联考化学试题天津市北辰区2023-2024学年高二上学期期中考试化学试题
名校
4 . 某温度下,向密闭容器中充入等物质的量的 和
和 ,发生反应
,发生反应 。达到平衡后,下列说法正确的是
。达到平衡后,下列说法正确的是
 和
和 ,发生反应
,发生反应 。达到平衡后,下列说法正确的是
。达到平衡后,下列说法正确的是A.增大压强,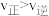 ,平衡常数增大 ,平衡常数增大 |
B.加入催化剂,平衡时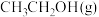 的浓度增大 的浓度增大 |
C.恒温下,移走一定量的 , , 变大, 变大, 变小 变小 |
D.恒容下,充入一定量的 ,平衡时 ,平衡时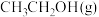 的体积分数一定降低 的体积分数一定降低 |
您最近半年使用:0次
2022-12-16更新
|
687次组卷
|
3卷引用:上海市虹口区2022-2023学年高三上学期一模统考化学试题
名校
5 . 认识化学反应的快慢和限度规律及影响因素,通过调控更好地满足工农业生产和日常生活的实际需要。
Ⅰ.根据所学知识,完成下列各题:
(1)决定化学反应速率的内在因素是_______。
(2)下列过程中,需要加快反应速率的是_______。
Ⅱ.用相同质量的锌片和铜粉跟相同浓度的足量的稀盐酸反应,得到的实验数据如下表所示:
(3)实验①和②表明_______ ,化学反应速率越快。
(4)能表明固体的表面积对反应速率有影响的实验编号是_______ 。
(5)该实验的目的是探究_______ 等因素对锌和稀盐酸反应速率的影响。
(6)请设计一个实验方案探究盐酸的浓度对反应速率的影响。_______
(7)对于2HBr(g) H2(g)+Br2(g)反应,下列四个图中可以表示该反应在一定条件下为可逆反应的是_______。
H2(g)+Br2(g)反应,下列四个图中可以表示该反应在一定条件下为可逆反应的是_______。
(8)对于平衡体系:FeCl3+3KSCN Fe(SCN)3+3KCl,下列描述正确的是_______。(多选)
Fe(SCN)3+3KCl,下列描述正确的是_______。(多选)
Ⅲ.牙齿表面被一层坚硬的名叫羟基磷酸钙的物质保护着,该物质的组成为Ca5(PO4)3OH,它在唾液中存在下列平衡:Ca5(PO4)3OH(s) 5Ca2+(aq)+3
5Ca2+(aq)+3 (aq)+OH-(aq)
(aq)+OH-(aq)
(9)口腔中的细菌和酶在消化分解食物时,会产生有机酸,从而使羟基磷酸钙溶解。若不及时处理,最终会使牙齿产生蛀洞。适用化学平衡知识解释酸使羟基磷酸钙溶解的原因。_______
Ⅰ.根据所学知识,完成下列各题:
(1)决定化学反应速率的内在因素是_______。
| A.温度和压强 | B.反应物的浓度 |
| C.反应物自身的性质 | D.催化剂 |
| A.钢铁腐蚀 | B.食物腐败 | C.炼钢 | D.塑料老化 |
Ⅱ.用相同质量的锌片和铜粉跟相同浓度的足量的稀盐酸反应,得到的实验数据如下表所示:
| 实验编号 | 锌的状态 | 反应温度/℃ | 收集100mL氢气所需时间/s |
| ① | 薄片 | 15 | 200 |
| ② | 薄片 | 25 | 90 |
| ③ | 粉末 | 25 | 10 |
(4)能表明固体的表面积对反应速率有影响的实验编号是
(5)该实验的目的是探究
(6)请设计一个实验方案探究盐酸的浓度对反应速率的影响。
(7)对于2HBr(g)
 H2(g)+Br2(g)反应,下列四个图中可以表示该反应在一定条件下为可逆反应的是_______。
H2(g)+Br2(g)反应,下列四个图中可以表示该反应在一定条件下为可逆反应的是_______。A. | B. | C. | D. |
 Fe(SCN)3+3KCl,下列描述正确的是_______。(多选)
Fe(SCN)3+3KCl,下列描述正确的是_______。(多选)| A.其他条件不变,增大FeCl3溶液浓度,溶液的血红色加深 |
| B.其他条件不变,增大KSCN溶液的浓度,平衡正向移动 |
| C.其他条件不变,加入一定量的KCl固体,平衡逆向移动,溶液颜色变浅 |
| D.其他条件不变,加入少量的铁粉,振荡,溶液颜色变浅 |
Ⅲ.牙齿表面被一层坚硬的名叫羟基磷酸钙的物质保护着,该物质的组成为Ca5(PO4)3OH,它在唾液中存在下列平衡:Ca5(PO4)3OH(s)
 5Ca2+(aq)+3
5Ca2+(aq)+3 (aq)+OH-(aq)
(aq)+OH-(aq)(9)口腔中的细菌和酶在消化分解食物时,会产生有机酸,从而使羟基磷酸钙溶解。若不及时处理,最终会使牙齿产生蛀洞。适用化学平衡知识解释酸使羟基磷酸钙溶解的原因。
您最近半年使用:0次
名校
6 . 实验室配制碘水时,通常将 溶于KI溶液:
溶于KI溶液: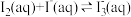 。关于该溶液,下列说法正确的是
。关于该溶液,下列说法正确的是
 溶于KI溶液:
溶于KI溶液: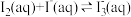 。关于该溶液,下列说法正确的是
。关于该溶液,下列说法正确的是A.KI的电子式: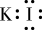 | B.滴入淀粉溶液,不变蓝 |
| C.加水稀释,平衡逆向移动 | D.加少量 固体平衡正向移动 固体平衡正向移动 |
您最近半年使用:0次
2022-11-30更新
|
128次组卷
|
3卷引用:上海市格致中学2022-2023学年高三上学期期中考试化学试题
名校
7 . 反应
 ,在一定条件下的密闭容器中达到平衡。下列措施不能提高乙烷平衡转化率的是
,在一定条件下的密闭容器中达到平衡。下列措施不能提高乙烷平衡转化率的是

 ,在一定条件下的密闭容器中达到平衡。下列措施不能提高乙烷平衡转化率的是
,在一定条件下的密闭容器中达到平衡。下列措施不能提高乙烷平衡转化率的是| A.增大容器容积 | B.升高温度 | C.分离出 | D.再充入 |
您最近半年使用:0次
名校
解题方法
8 . 氯气溶于水达到平衡后,若只改变某一条件,下列叙述正确的是
| A.通入少量SO2,溶液漂白性增强 |
| B.加入少量NaHCO3固体,c(ClO-)减小 |
| C.加入少量水,水的电离平衡向逆方向移动 |
| D.加入NaOH固体至恰好完全反应,一定有c(Na+)=c(Cl-)+c(ClO-)+c(HClO) |
您最近半年使用:0次
名校
解题方法
9 . 元素周期表中ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子,原子核外有_______ 种不同能量的电子,写出其最外层电子的轨道表示式_______ ;碘元素在元素周期表中的位置是_______ ;液溴的保存通常采取的方法是_______ 。
(2)能作为氯、溴、碘元素非金属性递变规律的判断依据是_______(填序号)。
(3) 与
与 反应生成
反应生成 和一种黑色固体。在25℃、101kPa下,已知该反应消耗
和一种黑色固体。在25℃、101kPa下,已知该反应消耗 ,放热44.5kJ,该反应的热化学方程式是
,放热44.5kJ,该反应的热化学方程式是_______ 。
(4)已知: 的熔点为1040℃,
的熔点为1040℃, 在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:
在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:_______
(5)HClO有很好的杀菌消毒效果。为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:_______
(6)下列从海洋中提取或提纯物质的生产或实验流程中,不合理的是_______ (填字母)。
a.海盐提纯:

b.海水提镁:
c.海带提碘: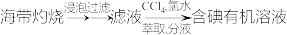

d.海水提溴:
(1)与氯元素同族的短周期元素的原子,原子核外有
(2)能作为氯、溴、碘元素非金属性递变规律的判断依据是_______(填序号)。
A. 、 、 、 、 的氧化性 的氧化性 | B. 、 、 、 、 的熔点 的熔点 |
| C.HCl、HBr、HI的热稳定性 | D.HCl、HBr、HI的酸性 |
 与
与 反应生成
反应生成 和一种黑色固体。在25℃、101kPa下,已知该反应消耗
和一种黑色固体。在25℃、101kPa下,已知该反应消耗 ,放热44.5kJ,该反应的热化学方程式是
,放热44.5kJ,该反应的热化学方程式是(4)已知:
 的熔点为1040℃,
的熔点为1040℃, 在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:
在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:(5)HClO有很好的杀菌消毒效果。为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:
(6)下列从海洋中提取或提纯物质的生产或实验流程中,不合理的是
a.海盐提纯:


b.海水提镁:

c.海带提碘:
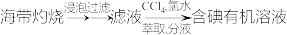

d.海水提溴:

您最近半年使用:0次
2022-11-11更新
|
167次组卷
|
2卷引用:上海市宝山区行知中学2022-2023学年高三上学期期中测试化学试题
名校
10 . 回答下列问题
(1)工业生产氢气时,常将水蒸气通过红热的炭即产生水煤气。
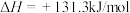 ,
,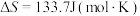 ,该反应在温度在
,该反应在温度在_______ 时能自发进行(“低温”或“高温”)。
(2)已知在400℃时,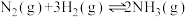 的
的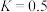
①在400℃时,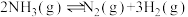 的
的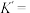
_______ (填数值)。
②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得 、
、 、
、 的物质的量分别为2mol、1mol、2mol,则此时反应
的物质的量分别为2mol、1mol、2mol,则此时反应
_______  (填“>”、“<”、“=”或“不能确定”)。
(填“>”、“<”、“=”或“不能确定”)。
③一定温度下,在恒容的密闭容器中发生上述反应,下列表示反应达到平衡状态的有_______ (填字母)。
A.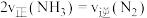
B.气体压强不再变化
C.气体的平均相对分子质量不再变化
D.单位时间每生成 3mol,同时消耗
3mol,同时消耗 2mol
2mol
(3)在某密闭容器中通入2mol 和2mol
和2mol ,在不同条件下发生反应
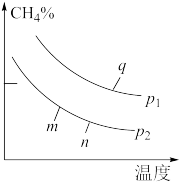
,在不同条件下发生反应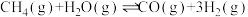 ,测得平衡时
,测得平衡时 的体积分数与温度、压强的关系如图所示。
的体积分数与温度、压强的关系如图所示。
①
_______  (填“<”、“>”或“=”),该反应为
(填“<”、“>”或“=”),该反应为_______ (填“吸”或“放”)热反应。
②m、n、q三点的化学平衡常数大小关系为_______ 。
③若q点对应的纵坐标为30,此时甲烷的转化率为_______ 。
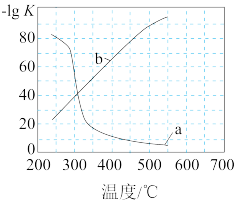
(4)实验测定该反应的化学平衡常数K随温度变化的曲线是如图中的_______ (填“a”、“b”),理由是_______ 。
(1)工业生产氢气时,常将水蒸气通过红热的炭即产生水煤气。

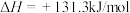 ,
,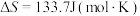 ,该反应在温度在
,该反应在温度在(2)已知在400℃时,
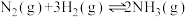 的
的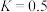
①在400℃时,
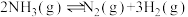 的
的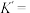
②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得
 、
、 、
、 的物质的量分别为2mol、1mol、2mol,则此时反应
的物质的量分别为2mol、1mol、2mol,则此时反应
 (填“>”、“<”、“=”或“不能确定”)。
(填“>”、“<”、“=”或“不能确定”)。③一定温度下,在恒容的密闭容器中发生上述反应,下列表示反应达到平衡状态的有
A.
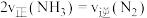
B.气体压强不再变化
C.气体的平均相对分子质量不再变化
D.单位时间每生成
 3mol,同时消耗
3mol,同时消耗 2mol
2mol(3)在某密闭容器中通入2mol
 和2mol
和2mol ,在不同条件下发生反应
,在不同条件下发生反应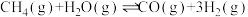 ,测得平衡时
,测得平衡时 的体积分数与温度、压强的关系如图所示。
的体积分数与温度、压强的关系如图所示。
①

 (填“<”、“>”或“=”),该反应为
(填“<”、“>”或“=”),该反应为②m、n、q三点的化学平衡常数大小关系为
③若q点对应的纵坐标为30,此时甲烷的转化率为
(4)实验测定该反应的化学平衡常数K随温度变化的曲线是如图中的

您最近半年使用:0次



