解题方法
1 . 利用反应2NO(g)+2CO(g) 2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比
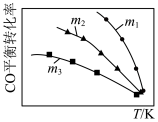
2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比
2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
| A.若m=2,反应达平衡时,NO的转化率为40%,则N2的体积分数为15.4% |
B.该反应的 |
C.投料比: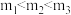 |
| D.汽车排气管中的催化剂可提高NO的平衡转化率 |
您最近一年使用:0次
解题方法
2 . 回答下列问题。
(1)工业合成氨的反应: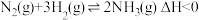 ,分别在
,分别在 、
、 温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图所示:
温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图所示:
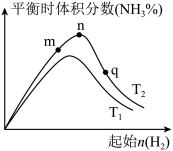
①比较在m、n、q三点所处的平衡状态中,反应物 的转化率最高的是
的转化率最高的是___________ 点。
② 条件下,在
条件下,在 的密闭容器中,充入
的密闭容器中,充入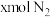 和
和 时,
时, 达平衡,此时反应物的转化率均为a,写出下列仅含a、x的表达式(不必化简):
达平衡,此时反应物的转化率均为a,写出下列仅含a、x的表达式(不必化简):
___________ ;该反应的平衡常数的值
___________ 。
③图像中
___________  (填“高于”、“低于”、“等于”或“无法确定”)。
(填“高于”、“低于”、“等于”或“无法确定”)。
(2)一定温度下,在密闭容器中将等物质的量的 和
和 混合,采用适当的催化剂进行反应
混合,采用适当的催化剂进行反应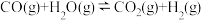 ,已知此温度下,该反应的平衡常数
,已知此温度下,该反应的平衡常数 ,则平衡时体系中
,则平衡时体系中 的物质的量分数为
的物质的量分数为___________  。
。
(1)工业合成氨的反应:
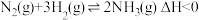 ,分别在
,分别在 、
、 温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图所示:
温度下,改变起始氢气物质的量,测得平衡时氨的体积分数如图所示:
①比较在m、n、q三点所处的平衡状态中,反应物
 的转化率最高的是
的转化率最高的是②
 条件下,在
条件下,在 的密闭容器中,充入
的密闭容器中,充入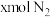 和
和 时,
时, 达平衡,此时反应物的转化率均为a,写出下列仅含a、x的表达式(不必化简):
达平衡,此时反应物的转化率均为a,写出下列仅含a、x的表达式(不必化简):

③图像中

 (填“高于”、“低于”、“等于”或“无法确定”)。
(填“高于”、“低于”、“等于”或“无法确定”)。(2)一定温度下,在密闭容器中将等物质的量的
 和
和 混合,采用适当的催化剂进行反应
混合,采用适当的催化剂进行反应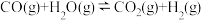 ,已知此温度下,该反应的平衡常数
,已知此温度下,该反应的平衡常数 ,则平衡时体系中
,则平衡时体系中 的物质的量分数为
的物质的量分数为 。
。
您最近一年使用:0次
3 . 下列事实不能 用勒夏特列原理来解释的是
| A.实验室中常用排饱和食盐水的方法收集Cl2 |
| B.鼓入过量空气有利于SO2转化为SO3 |
| C.开启啤酒瓶后,压强变小,瓶中立刻泛起大量泡沫 |
| D.煅烧硫铁矿时先将矿石粉碎 |
您最近一年使用:0次
解题方法
4 . 某学习小组欲利用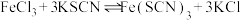 平衡体系探究影响平衡的因素,将
平衡体系探究影响平衡的因素,将
 溶液和
溶液和 溶液混合,得血红色溶液X,进行下列实验:
溶液混合,得血红色溶液X,进行下列实验:
实验Ⅰ.改变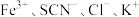 等离子浓度对平衡的影响
等离子浓度对平衡的影响
(1)取 溶液X,加入5滴
溶液X,加入5滴 溶液,得到溶液A;另取
溶液,得到溶液A;另取 溶液X,插入经砂纸打磨过的铁丝得到溶液B,A、B两溶液颜更深的是
溶液X,插入经砂纸打磨过的铁丝得到溶液B,A、B两溶液颜更深的是___________ (填A或B)。原因是:___________ 。
(2)取 溶液X,加入5滴
溶液X,加入5滴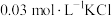 溶液,观察到溶液红色变浅,产生该现象的原因可能是:①
溶液,观察到溶液红色变浅,产生该现象的原因可能是:①___________ 对平衡产生了影响;②不直接参与平衡体系的 或
或 对平衡产生了影响。
对平衡产生了影响。
实验Ⅱ.为了探究KCl对 平衡体系的影响某学习小组同学进行如下探究:各取
平衡体系的影响某学习小组同学进行如下探究:各取 溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
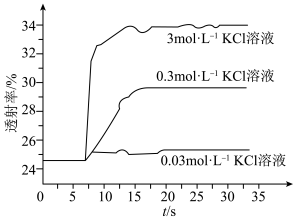
(3)上述实验可以得到以下结论:一是KCl对 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响___________ 移动(填“正向、逆向或不”)。
(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①: 产生的影响。
产生的影响。
猜想②: 产生的影响。
产生的影响。
猜想③:___________ 。
实验Ⅲ.探究盐对 和
和 平衡体系产生的影响资料信息:
平衡体系产生的影响资料信息:
a.溶液中的 离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
b.在 溶液中存在反应
溶液中存在反应 。
。
(5)根据上述信息,学习小组同学各取 溶液X,分别加入5滴①去离子水、②
溶液X,分别加入5滴①去离子水、②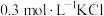 溶液、③
溶液、③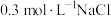 溶液、④
溶液、④ 溶液、⑤
溶液、⑤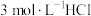 溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
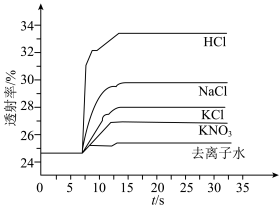
上述实验能证明阳离子盐效应影响 平衡体系的实验组是
平衡体系的实验组是___________ 。盐效应影响较大的阳离子是___________ 。
A.实验①②③ B.实验①②④ C.实验①③④
(6)已知 对平衡没有明显的影响,解释出现实验⑤现象的原因:
对平衡没有明显的影响,解释出现实验⑤现象的原因:___________ 。
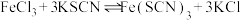 平衡体系探究影响平衡的因素,将
平衡体系探究影响平衡的因素,将
 溶液和
溶液和 溶液混合,得血红色溶液X,进行下列实验:
溶液混合,得血红色溶液X,进行下列实验:实验Ⅰ.改变
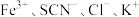 等离子浓度对平衡的影响
等离子浓度对平衡的影响(1)取
 溶液X,加入5滴
溶液X,加入5滴 溶液,得到溶液A;另取
溶液,得到溶液A;另取 溶液X,插入经砂纸打磨过的铁丝得到溶液B,A、B两溶液颜更深的是
溶液X,插入经砂纸打磨过的铁丝得到溶液B,A、B两溶液颜更深的是(2)取
 溶液X,加入5滴
溶液X,加入5滴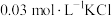 溶液,观察到溶液红色变浅,产生该现象的原因可能是:①
溶液,观察到溶液红色变浅,产生该现象的原因可能是:① 或
或 对平衡产生了影响。
对平衡产生了影响。实验Ⅱ.为了探究KCl对
 平衡体系的影响某学习小组同学进行如下探究:各取
平衡体系的影响某学习小组同学进行如下探究:各取 溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
(3)上述实验可以得到以下结论:一是KCl对
 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①:
 产生的影响。
产生的影响。 猜想②:
 产生的影响。
产生的影响。 猜想③:
实验Ⅲ.探究盐对
 和
和 平衡体系产生的影响资料信息:
平衡体系产生的影响资料信息:a.溶液中的
 离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。b.在
 溶液中存在反应
溶液中存在反应 。
。(5)根据上述信息,学习小组同学各取
 溶液X,分别加入5滴①去离子水、②
溶液X,分别加入5滴①去离子水、②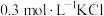 溶液、③
溶液、③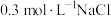 溶液、④
溶液、④ 溶液、⑤
溶液、⑤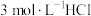 溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
上述实验能证明阳离子盐效应影响
 平衡体系的实验组是
平衡体系的实验组是A.实验①②③ B.实验①②④ C.实验①③④
(6)已知
 对平衡没有明显的影响,解释出现实验⑤现象的原因:
对平衡没有明显的影响,解释出现实验⑤现象的原因:
您最近一年使用:0次
5 . 已知: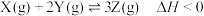 ,向一恒温恒容的密闭容器中充入1molX和3molY发生反应,t1时达到平衡状态I,在t2时改变某一条件,t3时重新达到平衡状态II,正反应速率随时间的变化如图所示。下列说法正确的是
,向一恒温恒容的密闭容器中充入1molX和3molY发生反应,t1时达到平衡状态I,在t2时改变某一条件,t3时重新达到平衡状态II,正反应速率随时间的变化如图所示。下列说法正确的是
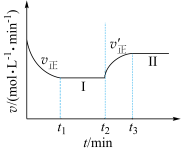
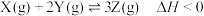 ,向一恒温恒容的密闭容器中充入1molX和3molY发生反应,t1时达到平衡状态I,在t2时改变某一条件,t3时重新达到平衡状态II,正反应速率随时间的变化如图所示。下列说法正确的是
,向一恒温恒容的密闭容器中充入1molX和3molY发生反应,t1时达到平衡状态I,在t2时改变某一条件,t3时重新达到平衡状态II,正反应速率随时间的变化如图所示。下列说法正确的是
| A.容器内压强不变,表明反应达到平衡 |
| B.t2时改变的条件:向容器中加入Z |
| C.平衡时X的体积分数φ:φ(II)<φ(I) |
| D.平衡常数K:K(II)<K(I) |
您最近一年使用:0次
名校
6 . 下列事实不能用平衡移动原理解释的是
| A | B | C | D |
 |  |  |  |
| 向H2(g)、I2(g)、HI(g)的平衡体系加压后颜色变深 | 开启啤酒瓶后,瓶中马上泛起大量泡沫 | 实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出 | 石灰岩受地下水长期溶蚀形成溶洞 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 工业上用软锰矿(主要成分是MnO2,含有Al2O3、SiO2等杂质),制备KMnO4的流程如下:
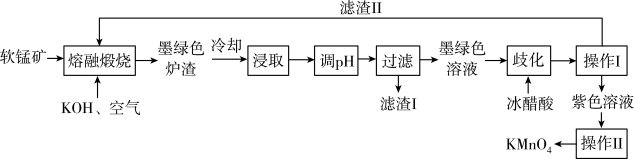
已知:K2MnO4固体和溶液均为墨绿色,溶液呈碱性,能发生可逆的歧化反应。下列说法正确的是

已知:K2MnO4固体和溶液均为墨绿色,溶液呈碱性,能发生可逆的歧化反应。下列说法正确的是
| A.向“浸取”后的溶液中通入CO2,调节其pH,经“过滤”得滤渣I,滤渣I的成分只有硅酸 |
B.“歧化”时,加入冰醋酸是为了调节溶液pH,使3MnO +2H2O +2H2O 2MnO 2MnO +MnO2+4OH-平衡正向移动,促进KMnO4的生成,提高KMnO4的产率 +MnO2+4OH-平衡正向移动,促进KMnO4的生成,提高KMnO4的产率 |
| C.“歧化”步骤中调节溶液pH时,可以用浓盐酸来代替冰醋酸 |
| D.“操作Ⅱ”时,当有大量晶体析出时,利用余热蒸干,即得紫黑色KMnO4晶体 |
您最近一年使用:0次
2023-11-11更新
|
626次组卷
|
5卷引用:福建省“德化一中、永安一中、漳平一中”三校协作2023-2024学年高三上学期12月联考化学试题
福建省“德化一中、永安一中、漳平一中”三校协作2023-2024学年高三上学期12月联考化学试题福建省福州市八县一中2023-2024学年高三上学期11月期中化学试题(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)选择题11-14湖北省黄冈市蕲春县实验高级中学2024届高三一轮复习10月月考化学试题
名校
解题方法
8 . 图Ⅰ、Ⅱ分别是将反应“ ”设计成的原电池装置,其中
”设计成的原电池装置,其中 、
、 均为碳棒。下列叙述中正确的是
均为碳棒。下列叙述中正确的是

 ”设计成的原电池装置,其中
”设计成的原电池装置,其中 、
、 均为碳棒。下列叙述中正确的是
均为碳棒。下列叙述中正确的是
| A.向图Ⅰ烧杯中逐滴加入适量浓盐酸,电流计(G)指针发生偏转,溶液颜色变深 |
B.向图ⅡB烧杯中逐滴加入适量40%NaOH溶液, 作正极 作正极 |
C.向图ⅡB烧杯中逐滴加入适量40%NaOH溶液, 电极: 电极: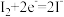 |
D.图Ⅱ中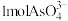 参加反应,溶液中转移2mol电子 参加反应,溶液中转移2mol电子 |
您最近一年使用:0次
2023-09-04更新
|
132次组卷
|
2卷引用:福建省南安市华侨中学2023-2024学年高二上学期8月月考化学试题
名校
9 . 钒的用途十分广泛,有金属“维生素”之称。以含钒石煤(主要成分是 、
、 ,含有的杂质有
,含有的杂质有 、
、 及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
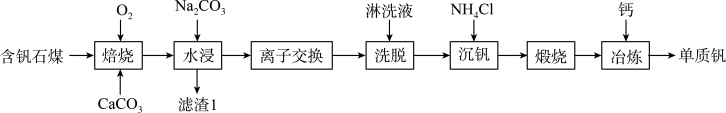
已知:
①该工艺条件下,溶液中金属离子开始沉淀时和完全沉淀时的pH如下表所示:
② ,
, ,
, 远大于
远大于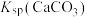 。
。
回答下列问题:
(1)为了提高“焙烧”效率,可采取的措施有___________ 、___________ 。
(2)“焙烧”时, 、
、 都转化为
都转化为 ,写出
,写出 转化为
转化为 的化学方程式:
的化学方程式:___________ 。
(3)“水浸”加入 调节溶液的pH为8.5,可完全除去的金属离子有
调节溶液的pH为8.5,可完全除去的金属离子有___________ ,部分除去的金属离子有___________ 。“水浸”加入过量 不能使
不能使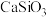 完全转化为
完全转化为 ,原因是
,原因是___________ 。
(4)“离子交换”与“洗脱”可表示为 (
( 为强碱性阴离子交换树脂,
为强碱性阴离子交换树脂, 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用___________ 。
(5)“沉钒”过程析出 晶体,需要加入过量
晶体,需要加入过量 ,目的是
,目的是___________ 。
(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是___________(填字母)。
 、
、 ,含有的杂质有
,含有的杂质有 、
、 及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
已知:
①该工艺条件下,溶液中金属离子开始沉淀时和完全沉淀时的pH如下表所示:
| 金属离子 |  |  |  |  |
| 开始沉淀时的pH | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀时的pH | 3.2 | 9.0 | 4.7 | 10.1 |
 ,
, ,
, 远大于
远大于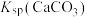 。
。回答下列问题:
(1)为了提高“焙烧”效率,可采取的措施有
(2)“焙烧”时,
 、
、 都转化为
都转化为 ,写出
,写出 转化为
转化为 的化学方程式:
的化学方程式:(3)“水浸”加入
 调节溶液的pH为8.5,可完全除去的金属离子有
调节溶液的pH为8.5,可完全除去的金属离子有 不能使
不能使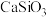 完全转化为
完全转化为 ,原因是
,原因是(4)“离子交换”与“洗脱”可表示为
 (
( 为强碱性阴离子交换树脂,
为强碱性阴离子交换树脂, 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用(5)“沉钒”过程析出
 晶体,需要加入过量
晶体,需要加入过量 ,目的是
,目的是(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是___________(填字母)。
| A.高炉炼铁 | B.电解熔融氯化钠制钠 |
| C.铝热反应制锰 | D.氧化汞分解制汞 |
您最近一年使用:0次
名校
10 . 采用高压氢还原法可以从溶液中直接提取金属粉末。以黄铜矿(含 、
、 ,少量的
,少量的 等)为原料制备铜粉的流程如图:
等)为原料制备铜粉的流程如图:

以下说法错误的是
 、
、 ,少量的
,少量的 等)为原料制备铜粉的流程如图:
等)为原料制备铜粉的流程如图:
以下说法错误的是
A.“废气”成分中含 |
| B.“沉铁”时加入CuO的目的是调节pH |
| C.“滤液”中含有硫酸,可循环使用提高原料的利用率 |
| D.“还原”时,增大溶液酸度有利于Cu的生成 |
您最近一年使用:0次
2023-05-07更新
|
203次组卷
|
3卷引用:福建省泉州第五中学2023-2024学年高三上学期10月月考化学试题



