名校
解题方法
1 . 以CO2、H2为原料合成CH3OH涉及的主要反应如下:
①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H1=-49.5 kJ/mol
②CO(g)+2H2(g)⇌CH3OH(g) ∆H2=-90.4 kJ/mol
③CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H3
不同压强下,按照n(CO2):n(H2)=1:3投料,CO2平衡转化率随温度变化关系如图。下列说法正确的是
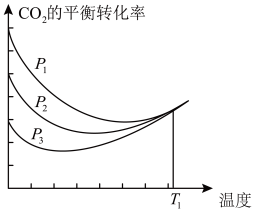
①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H1=-49.5 kJ/mol
②CO(g)+2H2(g)⇌CH3OH(g) ∆H2=-90.4 kJ/mol
③CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H3
不同压强下,按照n(CO2):n(H2)=1:3投料,CO2平衡转化率随温度变化关系如图。下列说法正确的是

| A.∆H3=-40.9 kJ/mol |
| B.p1 < p2 < p3 |
| C.为同时提高CO2的平衡转化率和CH3OH的平衡产率,反应条件应选择高温、高压 |
| D.T1温度时,三条曲线几乎交于一点的原因是:该温度下,主要发生反应③ |
您最近一年使用:0次
2021-04-04更新
|
1237次组卷
|
10卷引用:湖南省武冈市第一中学2021-2022学年高三下学期5月月考化学试题
湖南省武冈市第一中学2021-2022学年高三下学期5月月考化学试题湖南省邵阳市第二中学2021-2022学年高一下学期期末考试化学试题北京市丰台区2021届高三一模化学试题(已下线)押山东卷第14题 化学反应速率和平衡-备战2021年高考化学临考题号押题(山东卷)河北省武邑中学2021届高考七模化学试题黑龙江省大庆铁人中学2021-2022学年高二上学期开学考试化学试题北京市顺义牛栏山第一中学2022-2023学年高二上学期期中考试化学试题北京市第一七一中学2023-2024学年高二上学期期中考试化学试题山东省烟台市龙口市2023-2024学年高二上学期10月统考化学试题云南省保山市腾冲市第八中学2020-2021学年高二下学期期中考试化学试卷
名校
解题方法
2 . 下列实验装置或操作能达到实验目的的是
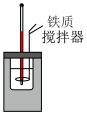 | 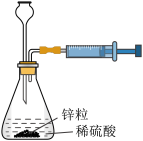 |
| A.测定中和反应的反应热 | B.测定锌与稀硫酸反应的反应速率 |
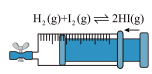 | 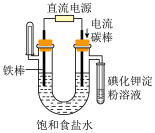 |
| C.探究压强对平衡的影响 | D.验证NaCl溶液(含酚酞)电解产物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-11更新
|
330次组卷
|
3卷引用:湖南省衡阳市第八中学2024届高三模拟预测信息卷(一)化学试题
3 . 在恒容密闭容器中通入 与
与 ,使其物质的量浓度均为
,使其物质的量浓度均为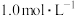 ,在一定条件下发生反应:
,在一定条件下发生反应: 。测得平衡时
。测得平衡时 的体积分数与温度及压强的关系如图所示。
的体积分数与温度及压强的关系如图所示。
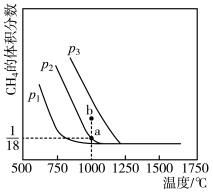
下列说法一定正确的是
 与
与 ,使其物质的量浓度均为
,使其物质的量浓度均为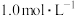 ,在一定条件下发生反应:
,在一定条件下发生反应: 。测得平衡时
。测得平衡时 的体积分数与温度及压强的关系如图所示。
的体积分数与温度及压强的关系如图所示。
下列说法一定正确的是
A.该反应的 | B.压强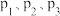 由小到大的顺序为 由小到大的顺序为 |
C.压强为 时,b点处 时,b点处 | D.a点时 的转化率为70% 的转化率为70% |
您最近一年使用:0次
2022-05-14更新
|
377次组卷
|
2卷引用:湖南省怀化市雅礼实验学校2022-2023学年高二上学期第一次月考化学试题
名校
4 . COCl2(g) CO(g) +Cl2(g) △H>0,当反应达到平衡时,下列措施:①升温;②恒容通入惰性气体;③增加CO浓度;④减压;⑤加催化剂;⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g) +Cl2(g) △H>0,当反应达到平衡时,下列措施:①升温;②恒容通入惰性气体;③增加CO浓度;④减压;⑤加催化剂;⑥恒压通入惰性气体,能提高COCl2转化率的是
 CO(g) +Cl2(g) △H>0,当反应达到平衡时,下列措施:①升温;②恒容通入惰性气体;③增加CO浓度;④减压;⑤加催化剂;⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g) +Cl2(g) △H>0,当反应达到平衡时,下列措施:①升温;②恒容通入惰性气体;③增加CO浓度;④减压;⑤加催化剂;⑥恒压通入惰性气体,能提高COCl2转化率的是| A.①②④ | B.①④⑥ | C.②③⑤ | D.③⑤⑥ |
您最近一年使用:0次
2020-12-11更新
|
1390次组卷
|
39卷引用:湖南省湘潭市第一中学2020-2021学年高二下学期期中考试(水平测试)化学试卷
湖南省湘潭市第一中学2020-2021学年高二下学期期中考试(水平测试)化学试卷(已下线)2011-2012年江苏淮安市范集中学高二下学期期中考试化学试卷(已下线)2011-2012年湖北宜昌金东方学校高二上学期期末考试化学试卷(已下线)2013-2014学年江苏省泰州市姜堰区高二上学期期中考试化学试卷2019年秋高三化学复习强化练习—— 化学反应速率及化学平衡(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP409】【化学】广东省江门市第二中学2020-2021学年高二上学期第二次考试(期中)化学试题(已下线)【浙江新东方】99甘肃省白银市第十中学2019-2020学年高二上学期期中考试化学试题湖北省宜昌市人文艺术高中2020-2021学年高二上学期期中考试化学试题河北省衡水市第十四中学2020-2021学年高二下学期摸底考试化学试题广东省广州市荔湾区广州市西关外国语学校2020—2021学年高二培优选拔测试化学试题天津市实验中学滨海学校黄南民族班2020-2021学年高二下学期期中化学试题浙江省宁波市六校2020-2021学年高二上学期期中联考化学试题江西省南昌市八一中学、洪都中学等4校2021-2022学年高二上学期期中联考化学试题陕西省西安市第一中学2021-2022学年高二上学期期中考试化学试题甘肃省永昌县第一高级中学2020-2021学年高二上学期期末考试化学试题(已下线)2.3.2 温度变化对化学平衡的影响(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)宁夏银川市第二中学2021-2022学年高二下学期第一次月考化学试题江西省抚州市崇仁县第二中学2021-2022学年高二上学期第二次月考化学试题江苏省如皋中学2022-2023学年高二上学期8月综合测试化学试题天津市第二南开学校2022-2023学年高二上学期9月阶段性线上练习化学试题 (已下线)2.2.1 化学平衡状态——同步学习必备知识黑龙江省鹤岗市第一中学2022-2023学年高二10月月考化学试题黑龙江省哈尔滨市第二十四中学2022-2023学年高二10月月考化学试题山东省滨州市沾化区实验高级中学2022-2023学年高二10月月考化学试题广东省开平市忠源纪念中学2021-2022学年高二上学期第二次月考化学试题湖北省竹溪县第二高级中学2021-2022学年高二上学期12月月考化学试题新疆吐鲁番市高昌区第二中学2021-2022学年高二上学期期末考试化学试题云南省玉溪市华宁县第二中学2021-2022年高二下学期开学考试化学试题重庆市为明学校2022-2023学年高二上学期期末检测化学试题天津市实验中学2022-2023学年高二上学期末考试化学试题江苏省海安高级中学2023-2024学年高二上学期第一次考试化学试题陕西省西安中学2023-2024学年高二上学期第一次综合评价化学试题吉林省长春市东北师范大学附属中学2023-2024学年高二上学期10月期中化学试题(已下线)BBWYhjhx1105.pdf山东省德州市第一中学2023-2024学年高二10月月考化学试题四川省自贡市第一中学校2023-2024学年高二上学期10月月考化学试题辽宁省大连经济技术开发区第一中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
5 . 我国政府承诺二氧化碳排放在2030年前达到峰值,2060年前实现碳中和,彰显作为大国的担当和责任。 催化重整对温室气体的减排具有重要意义,其反应为
催化重整对温室气体的减排具有重要意义,其反应为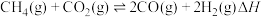 。回答下列问题:
。回答下列问题:
(1)已知:①
②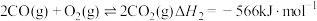
③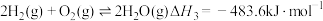
则
___________  。
。
(2)恒容密闭容器中可逆反应 达到平衡状态的标志是___________(填序号)。
达到平衡状态的标志是___________(填序号)。
(3)容器容积为1L,控制 和
和 初始投料量分别为2mol和3mol,发生反应:
初始投料量分别为2mol和3mol,发生反应: ,甲烷的平衡转化率与温度、压强的关系如图甲所示。
,甲烷的平衡转化率与温度、压强的关系如图甲所示。
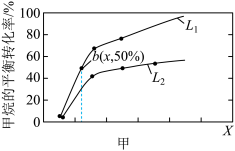
则 代表
代表___________ (填“温度”或“压强”):
___________  (填“大于”或“小于”),并请说出理由:
(填“大于”或“小于”),并请说出理由:___________ ;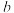 点反应的平衡常数为
点反应的平衡常数为___________ 。
(4)500℃下,将 和
和 的混合气体(投料比为1:1)按一定流速通过盛有炭催化剂的反应器,测得
的混合气体(投料比为1:1)按一定流速通过盛有炭催化剂的反应器,测得 的转化率受炭催化剂颗粒大小的影响如图乙所示(注:目数越大,表示炭催化剂颗粒越小)。
的转化率受炭催化剂颗粒大小的影响如图乙所示(注:目数越大,表示炭催化剂颗粒越小)。
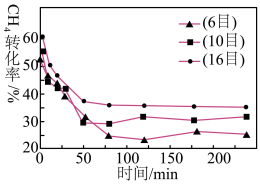
由图乙可知,75min后 转化率与炭催化剂目数的关系为
转化率与炭催化剂目数的关系为___________ ,原因是___________ 。
(5)①温度为 时,
时,
实验测得: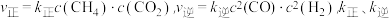 为速率常数。
为速率常数。 时,
时, =
=___________ (以 表示)。
表示)。
②当温度改变为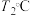 时,
时,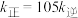 ,则
,则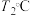 时平衡压强
时平衡压强___________  时平衡压强(填“>”“<”或“=”),理由是
时平衡压强(填“>”“<”或“=”),理由是___________ 。
 催化重整对温室气体的减排具有重要意义,其反应为
催化重整对温室气体的减排具有重要意义,其反应为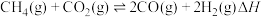 。回答下列问题:
。回答下列问题:(1)已知:①

②
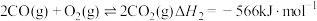
③
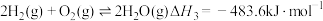
则

 。
。(2)恒容密闭容器中可逆反应
 达到平衡状态的标志是___________(填序号)。
达到平衡状态的标志是___________(填序号)。A.单位时间内生成1mol 的同时消耗2molCO 的同时消耗2molCO |
| B.混合气体的密度不再改变 |
C.反应速率 |
| D.混合气体的平均相对分子质量不再改变 |
 和
和 初始投料量分别为2mol和3mol,发生反应:
初始投料量分别为2mol和3mol,发生反应: ,甲烷的平衡转化率与温度、压强的关系如图甲所示。
,甲烷的平衡转化率与温度、压强的关系如图甲所示。
则
 代表
代表
 (填“大于”或“小于”),并请说出理由:
(填“大于”或“小于”),并请说出理由: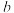 点反应的平衡常数为
点反应的平衡常数为(4)500℃下,将
 和
和 的混合气体(投料比为1:1)按一定流速通过盛有炭催化剂的反应器,测得
的混合气体(投料比为1:1)按一定流速通过盛有炭催化剂的反应器,测得 的转化率受炭催化剂颗粒大小的影响如图乙所示(注:目数越大,表示炭催化剂颗粒越小)。
的转化率受炭催化剂颗粒大小的影响如图乙所示(注:目数越大,表示炭催化剂颗粒越小)。
由图乙可知,75min后
 转化率与炭催化剂目数的关系为
转化率与炭催化剂目数的关系为(5)①温度为
 时,
时,
实验测得:
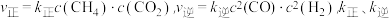 为速率常数。
为速率常数。 时,
时, =
= 表示)。
表示)。②当温度改变为
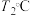 时,
时,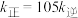 ,则
,则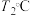 时平衡压强
时平衡压强 时平衡压强(填“>”“<”或“=”),理由是
时平衡压强(填“>”“<”或“=”),理由是
您最近一年使用:0次
2023-02-07更新
|
351次组卷
|
3卷引用:湖南省醴陵市第一中学2023届高三第六次月考化学试题
名校
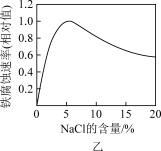
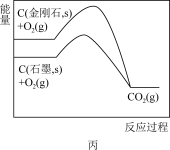
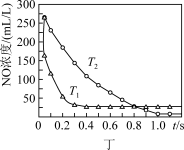
6 . 根据下列图示所得出的结论不正确的是
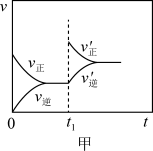




A.图甲表示2SO2(g)+O2(g) 2SO3(g) △H<0,t1时改变的条件是增大体系的压强 2SO3(g) △H<0,t1时改变的条件是增大体系的压强 |
| B.图乙NaCl溶液浓度过高铁腐蚀速率降低,说明NaCl浓度越大溶液中O2的浓度越小 |
| C.图丙说明石墨转化为金刚石的反应的△H<0 |
D.图丁是一定条件下发生反应:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g)此过程△H<0 4N2(g)+6H2O(g)此过程△H<0 |
您最近一年使用:0次
2022-05-10更新
|
367次组卷
|
8卷引用:湖南省岳阳市2019-2020学年高二下学期期末考试化学试题
湖南省岳阳市2019-2020学年高二下学期期末考试化学试题湖南省岳阳市平江县2022届高三下学期教学质量监测(三)化学试题湖南省邵阳市武冈市2022-2023学年高三上学期期中考试化学试题北京市通州区2020届高三第一次模拟考试化学试题河北省武邑中学2021届高三二模化学试题(已下线)第七章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测重庆市第七中学校2022届高三第二次月考化学试题(已下线)微专题38 新情景下的综合图象与突破-备战2023年高考化学一轮复习考点微专题
名校
7 . 在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
[已知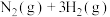

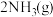
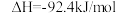 ]。
]。
下列说法正确的是
[已知
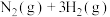

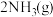
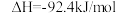 ]。
]。| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol  、3mol 、3mol  | 2 mol  | 4 mol  |
 的浓度(mol/L) 的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 |  |  | 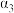 |
| A.2c1>c3 | B.a+b>92.4 | C.2 p2< p3 | D. + +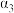 <1 <1 |
您最近一年使用:0次
2022-10-21更新
|
334次组卷
|
16卷引用:湖南省衡阳市第一中学2019-2020学年高二上学期第一次月考化学试题
湖南省衡阳市第一中学2019-2020学年高二上学期第一次月考化学试题(已下线)2013-2014学年湖北省荆州中学高二上学期期中考试化学试卷2015-2016学年安徽省六安一中高二下开学考试化学试卷河南省南阳市第一中学2016-2017学年高二下学期第三次月考化学试题四川省南充高级中学2017-2018学年高二12月月考化学试题(已下线)黄金30题系列 高二化学(选修4) 小题好拿分【提升版】(已下线)解密10 化学反应速率与化学平衡(教师版)——备战2018年高考化学之高频考点解密2017-2018学年鲁科版高二下学期化学选修4-2.2等效平衡练习题四川省宁南中学2018-2019学年高二下学期第一次月考化学试题云南省玉溪市玉溪一中2019-2020学年高二上学期第一次月考化学试题河南省郑州市郑州中学2020-2021学年高二上学期期中考试化学试题河南省鹤壁市高级中学2020-2021学年高二上学期尖子生联赛调研化学试题四川省汉源县第二中学2019-2020学年高二下学期第二次月考化学试题河南省南阳市第一中学校2021-2022学年高二上学期第二次月考化学试题黑龙江省牡丹江市海林市朝鲜族中学2022-2023学年高二上学期第一次月考化学试题山东省枣庄市第三中学(实验班)2022-2023学年高二11月线上测试化学试题
名校
解题方法
8 . 研究含氮、硫物质之间的转化,对资源的综合利用具有重要意义。
(1)硫酸生产中, 催化氧化生成
催化氧化生成 :
: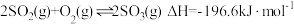
①在恒容密闭容器中达到平衡后,能使平衡正向移动并提高 转化率的是
转化率的是_______
A.向容器中通入 B.向容器中通入
B.向容器中通入 C.使用催化剂 D.降低温度
C.使用催化剂 D.降低温度
②如图表示 催化氧化生成
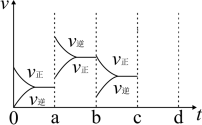
催化氧化生成 在密闭容器中达到平衡时,由于条件改变而引起反应速率的变化情况,a时刻改变的条件可能是
在密闭容器中达到平衡时,由于条件改变而引起反应速率的变化情况,a时刻改变的条件可能是____ ;若c时刻增大压强,把反应速率变化情况画在c~d处____ 。
(2)合成氨反应 是人工固氮的主要手段,对人类生存和经济发展都有着重大意义。合成氨反应中正反应速率
是人工固氮的主要手段,对人类生存和经济发展都有着重大意义。合成氨反应中正反应速率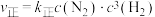 ,逆反应速率
,逆反应速率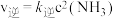 。
。 、
、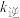 为速率常数。平衡常数K与温度的关系如图。
为速率常数。平衡常数K与温度的关系如图。
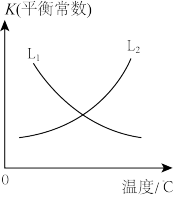
①表示正反应的平衡常数K与温度变化的曲线为_______ (填 或
或 )
)
②平衡时,合成氨反应的平衡常数
_______ (用 ,
,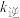 表示)
表示)
(3)将一定量 气体充入恒容的密闭容器中,控制反应温度为T1,发生的反应为:
气体充入恒容的密闭容器中,控制反应温度为T1,发生的反应为: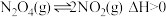 。
。
①下列可作为反应达到平衡的判据是_______
A.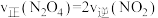 B.气体的压强不变 C.
B.气体的压强不变 C. 不变 D.容器内颜色不变
不变 D.容器内颜色不变
②t1时刻反应达到平衡,混合气体平衡总压强为P, 的平衡转化率为
的平衡转化率为 ,则反应
,则反应 的平衡常数
的平衡常数
_______ (用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
(1)硫酸生产中,
 催化氧化生成
催化氧化生成 :
: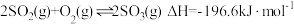
①在恒容密闭容器中达到平衡后,能使平衡正向移动并提高
 转化率的是
转化率的是A.向容器中通入
 B.向容器中通入
B.向容器中通入 C.使用催化剂 D.降低温度
C.使用催化剂 D.降低温度②如图表示
 催化氧化生成
催化氧化生成 在密闭容器中达到平衡时,由于条件改变而引起反应速率的变化情况,a时刻改变的条件可能是
在密闭容器中达到平衡时,由于条件改变而引起反应速率的变化情况,a时刻改变的条件可能是
(2)合成氨反应
 是人工固氮的主要手段,对人类生存和经济发展都有着重大意义。合成氨反应中正反应速率
是人工固氮的主要手段,对人类生存和经济发展都有着重大意义。合成氨反应中正反应速率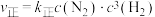 ,逆反应速率
,逆反应速率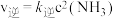 。
。 、
、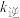 为速率常数。平衡常数K与温度的关系如图。
为速率常数。平衡常数K与温度的关系如图。
①表示正反应的平衡常数K与温度变化的曲线为
 或
或 )
)②平衡时,合成氨反应的平衡常数

 ,
,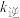 表示)
表示)(3)将一定量
 气体充入恒容的密闭容器中,控制反应温度为T1,发生的反应为:
气体充入恒容的密闭容器中,控制反应温度为T1,发生的反应为: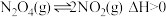 。
。①下列可作为反应达到平衡的判据是
A.
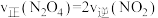 B.气体的压强不变 C.
B.气体的压强不变 C. 不变 D.容器内颜色不变
不变 D.容器内颜色不变②t1时刻反应达到平衡,混合气体平衡总压强为P,
 的平衡转化率为
的平衡转化率为 ,则反应
,则反应 的平衡常数
的平衡常数
您最近一年使用:0次
2022-09-02更新
|
377次组卷
|
3卷引用: 湖南省株洲市第八中学2022-2023学年高三上学期第三次月考化学试题
名校
解题方法
9 . 用下列实验方案和装置能达到相应实验目的的是
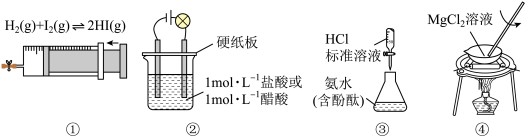

| A.实验①探究压强对平衡的影响 | B.实验②证明醋酸是弱电解质 |
| C.实验③用于测定氨水的浓度 | D.实验④制备无水 |
您最近一年使用:0次
2023-02-11更新
|
322次组卷
|
4卷引用:湖南省衡阳市第八中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
10 . 随着我国“碳达峰”、“碳中和”目标的确定,二氧化碳资源化利用倍受关注。
Ⅰ.以 和
和 为原料合成尿素:
为原料合成尿素: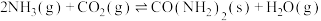
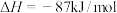 。
。
(1)有利于提高 平衡转化率的措施是_______(填标号)。
平衡转化率的措施是_______(填标号)。
(2)研究发现,合成尿素反应分两步完成,其能量变化如图甲所示。
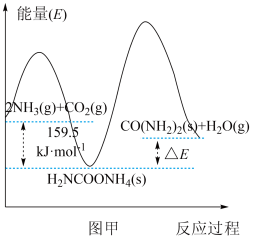
第一步: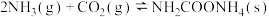

第二步: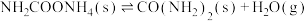

反应速率较快的是反应_______ (填“第一步”或“第二步”)。
Ⅱ.以和催化重整制备合成气: 。
。
(3)在密闭容器中通入物质的量均为0.2mol的 和
和 ,在一定条件下发生反应
,在一定条件下发生反应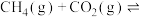
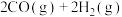 ,
, 的平衡转化率随温度、压强的变化关系如图乙所示:
的平衡转化率随温度、压强的变化关系如图乙所示:
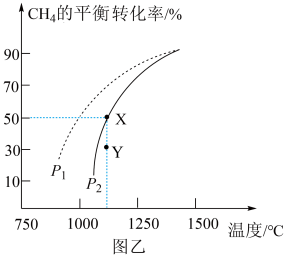
①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是_______ (填标号)。
A.容器中混合气体的密度保持不变 B.容器内混合气体的压强保持不变
C.反应速率: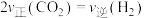 D.同时断裂2mol C—H和1mol H—H
D.同时断裂2mol C—H和1mol H—H
②由图乙可知,压强
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ,则X点对应温度下的
,则X点对应温度下的
_______ (用含 的代数式表示)。
的代数式表示)。
Ⅲ.电化学法还原二氧化碳制乙烯。
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图丙所示:

(4)阴极电极反应为_______ ;该装置中使用的是_______ (填“阳”或“阴”)离子交换膜。
Ⅰ.以
 和
和 为原料合成尿素:
为原料合成尿素: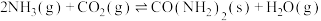
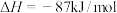 。
。(1)有利于提高
 平衡转化率的措施是_______(填标号)。
平衡转化率的措施是_______(填标号)。| A.高温低压 | B.低温高压 | C.高温高压 | D.低温低压 |

第一步:
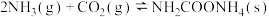

第二步:
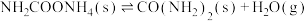

反应速率较快的是反应
Ⅱ.以和催化重整制备合成气:
 。
。(3)在密闭容器中通入物质的量均为0.2mol的
 和
和 ,在一定条件下发生反应
,在一定条件下发生反应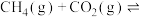
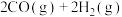 ,
, 的平衡转化率随温度、压强的变化关系如图乙所示:
的平衡转化率随温度、压强的变化关系如图乙所示:
①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是
A.容器中混合气体的密度保持不变 B.容器内混合气体的压强保持不变
C.反应速率:
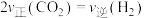 D.同时断裂2mol C—H和1mol H—H
D.同时断裂2mol C—H和1mol H—H②由图乙可知,压强

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
 ,则X点对应温度下的
,则X点对应温度下的
 的代数式表示)。
的代数式表示)。Ⅲ.电化学法还原二氧化碳制乙烯。
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图丙所示:

(4)阴极电极反应为
您最近一年使用:0次
2023-02-06更新
|
342次组卷
|
2卷引用:湖南省长沙市雅礼中学2022-2023学年高三下学期月考卷(六)化学试题



