名校
解题方法
1 . 工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理实现绿色环保、废物利用。
Ⅰ.脱硝:已知:H2的燃烧热为285.8 kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133 kJ·mol-1
H2O(g)=H2O(l) ΔH=-44 kJ·mol-1
(1)催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为___________ 。
Ⅱ.脱碳:
(2)向2 L密闭容器中加入1mol CO2和3 mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g) CH3OH(l)+H2O(l) ΔH<0
CH3OH(l)+H2O(l) ΔH<0
①该反应自发进行的条件是___________ (填“低温”“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是___________ (填字母)。
a.混合气体的平均相对分子质量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1 mol CO2生成的同时有3 mol H-H键断裂
f. CO2和H2的物质的量之比保持不变 g. v正(CO2) = 3v逆(H2)
(3)工业上使用水煤气(CO与H2的混合气体)转化成甲醇,反应为CO(g)+2H2(g) CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
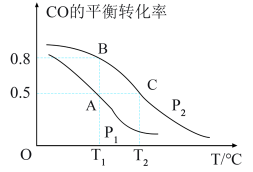
①p1、p2的大小关系是p1___________ p2(填“>”“<"或"=”)。
②A、B、C三点的平衡常数KA、KB、Kc的大小关系是___________ 。
(4)在T2℃、p2压强时,往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。
①平衡时H2的体积分数是___________ ;平衡后再加入1.0molCO后重新到达平衡,则CO的转化率___________ (填“增大""不变”成“减小”),CO与CH3OH的浓度比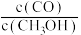
___________ (填"增大”“不变"或“减小")。
②若以不同比例投料,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)___________ v(逆)(填“”“<"或“=”)。
③若p2压强恒定为p,则平衡常数Kp=___________ (Kp用气体平衡分压代替气体平衡浓度计算,分压=总压×气体的物质的量分数,整理出含p的最简表达式)。
Ⅰ.脱硝:已知:H2的燃烧热为285.8 kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133 kJ·mol-1
H2O(g)=H2O(l) ΔH=-44 kJ·mol-1
(1)催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为
Ⅱ.脱碳:
(2)向2 L密闭容器中加入1mol CO2和3 mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)
 CH3OH(l)+H2O(l) ΔH<0
CH3OH(l)+H2O(l) ΔH<0①该反应自发进行的条件是
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均相对分子质量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1 mol CO2生成的同时有3 mol H-H键断裂
f. CO2和H2的物质的量之比保持不变 g. v正(CO2) = 3v逆(H2)
(3)工业上使用水煤气(CO与H2的混合气体)转化成甲醇,反应为CO(g)+2H2(g)
 CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
①p1、p2的大小关系是p1
②A、B、C三点的平衡常数KA、KB、Kc的大小关系是
(4)在T2℃、p2压强时,往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。
①平衡时H2的体积分数是
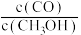
②若以不同比例投料,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)
③若p2压强恒定为p,则平衡常数Kp=
您最近一年使用:0次
名校
2 . 下列对图象的叙述正确的是( )

A.图1对于反应: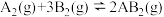 ,图①中的横轴x可以表示压强 ,图①中的横轴x可以表示压强 |
| B.图2表示其他条件相同时,甲、乙两份等浓度等体积的双氧水分解,乙中加入少量氯化铁 |
| C.图3可表示乙酸溶液中通入氨气至过量时溶液导电性的变化 |
D.图4若除去0.1mol∙L-1CuSO4溶液中的 ,可向溶液中加入适量NaOH至pH约为7 ,可向溶液中加入适量NaOH至pH约为7 |
您最近一年使用:0次
名校
3 . 甲、乙、丙三个容器中最初存在的物质及其数量如图所示,三个容器最初的容积相等、温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡。下列说法正确的是
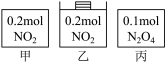
| A.平衡时各容器内c(NO2)的大小顺序为乙>甲>丙 |
| B.平衡时N2O4的百分含量:乙>甲=丙 |
| C.平衡时甲中NO2与丙中N2O4的转化率不可能相同 |
| D.平衡时混合物的平均相对分子质量:甲>乙>丙 |
您最近一年使用:0次
2019-11-06更新
|
2230次组卷
|
28卷引用:天津市第一中学2021届高三上学期第二次月考化学试题
天津市第一中学2021届高三上学期第二次月考化学试题辽宁省辽阳市集美中学2020届高二12月月考化学试题江西省万载中学2019-2020学年高二12月月考(创新班)化学试题山西省寿阳县第一中学2020—2021学年高二上学期第二次月考化学试题河南省林州市第一中学2020-2021学年高二下学期第二次月考化学试题山东省临沂市平邑县第一中学实验部2021-2022学年高二上学期第二次月考化学试题湖北省武汉市长虹中学2021-2022学年高二上学期10月月考化学试卷天津市外国语大学附属外国语学校2021-2022学年高二上学期期中阶段性检测化学试题云南省凤庆县第一中学2021-2022学年高二下学期3月份考试化学试题四川省广安市华蓥中学校2021-2022学年高二上学期11月月考化学试题山西省山西大学附属中学2022-2023学年高二上学期10月考化学试题山东省青岛第十七中学2023-2024学年高二上学期12月月考化学试题山西省朔州市怀仁一中2019-2020学年高二上学期期中考试化学试题山东省新泰市第二中学2019-2020学年高二上学期期中考试化学试题步步为赢 高二化学寒假作业:作业六 化学平衡中的模型构建与等效平衡鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第2节综合训练高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 第二节综合训练黑龙江省哈尔滨三中2021届高三上学期期中考试化学试题(已下线)练习4 化学平衡-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)黑龙江省龙东南六校2020-2021学年高二上学期期末联考化学试题选择性必修1 专题2 第三单元综合训练黑龙江省哈尔滨师范大学附属中学2021-2022学年高二上学期开学考试化学试题(已下线)选择性必修1 期中检测(能力提升卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)河南省洛阳市2021-2022学年高二上期期中考试化学试题江西省新余市2021-2022学年高二上学期期末检测化学试题2.3.1浓度 压强变化对化学平衡的影响 课后安徽省安庆市第二中学2023-2024学年高二上学期期中考试化学试卷福建师范大学附属中学2023-2024学年高二上学期期中考试化学试题
名校
4 . 用活性炭还原法可以处理氮氧化物。某研究小组向2L密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g) 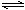 N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度(mol/L)如表所示,则下列说法不正确的是
N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度(mol/L)如表所示,则下列说法不正确的是
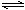 N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度(mol/L)如表所示,则下列说法不正确的是
N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度(mol/L)如表所示,则下列说法不正确的是| 时间/t(min) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| A.10~20 min内,NO的平均反应速率为0.018mol/(L∙min) |
| B.T1℃时,该反应的平衡常数K=0.25 |
| C.保持与前30min的反应条件相同,再向容器中加入2molN2和2molNO,则平衡向左移动 |
| D.30min后,只改变了一个条件,根据上述表格判断,该条件可能为缩小容器体积 |
您最近一年使用:0次
2019-03-07更新
|
471次组卷
|
4卷引用:天津汇文中学2022-2023学年高二上学期第一次阶段性测试化学试题
天津汇文中学2022-2023学年高二上学期第一次阶段性测试化学试题【全国百强校】福建省厦门双十中学2018-2019学年高二下学期第二次月考化学试题【校级联考】江西省南康中学、于都中学2019届高三下学期第二次联考化学试题(已下线)课时35 化学反应速率及影响因素-2022年高考化学一轮复习小题多维练(全国通用)



