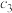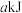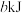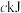1 . 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
I.制取氢气
(1)甲醇和水蒸气制取氢气的过程中有下列反应:
CH3OH(g) CO(g)+2H2(g) △H=+91 kJ·mol-1
CO(g)+2H2(g) △H=+91 kJ·mol-1
CO(g)+H2O(g) CO2(g)+H2 (g) △H=-4lkJ·mol-1
CO2(g)+H2 (g) △H=-4lkJ·mol-1
写出以甲醇为原料制取氢气的热化学方程式___________ 。
(2)理论上,能提高H2平衡产率的措施有___________ (写出一条即可)。
II.储存氢气
硼氢化钠(NaBH4) 是研究最广泛的储氢材料之一;
已知: i.B的电负性为2.0 H的电负性为2.1
ii.25℃下NaBH4 在水中的溶解度为55g,NaBO2在水中的溶解度为0.28g
(3)向NaBH4 水溶液中加入催化剂Ru/NGR后,能够迅速反应,生成偏硼酸钠(NaBO2) 和氢气。写出该反应的化学方程式___________ 。
(4)在研究浓度对催化剂Ru/NGR 活性的影响时,发现B 点后(见下图)增加NaBH4的浓度,制氢速率反而下降,推断可能的原因是___________ 。

(5)用惰性电极电解NaBO2 溶液可制得NaBH4, 实现物质的循环使用,制备装置如图所示。
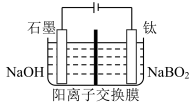
①钛电极的电极反应式是___________ ;
②电解过程中,阴极区溶液pH___________ 。(填“增大”“减小”或“不变”)
I.制取氢气
(1)甲醇和水蒸气制取氢气的过程中有下列反应:
CH3OH(g)
 CO(g)+2H2(g) △H=+91 kJ·mol-1
CO(g)+2H2(g) △H=+91 kJ·mol-1CO(g)+H2O(g)
 CO2(g)+H2 (g) △H=-4lkJ·mol-1
CO2(g)+H2 (g) △H=-4lkJ·mol-1写出以甲醇为原料制取氢气的热化学方程式
(2)理论上,能提高H2平衡产率的措施有
II.储存氢气
硼氢化钠(NaBH4) 是研究最广泛的储氢材料之一;
已知: i.B的电负性为2.0 H的电负性为2.1
ii.25℃下NaBH4 在水中的溶解度为55g,NaBO2在水中的溶解度为0.28g
(3)向NaBH4 水溶液中加入催化剂Ru/NGR后,能够迅速反应,生成偏硼酸钠(NaBO2) 和氢气。写出该反应的化学方程式
(4)在研究浓度对催化剂Ru/NGR 活性的影响时,发现B 点后(见下图)增加NaBH4的浓度,制氢速率反而下降,推断可能的原因是

(5)用惰性电极电解NaBO2 溶液可制得NaBH4, 实现物质的循环使用,制备装置如图所示。

①钛电极的电极反应式是
②电解过程中,阴极区溶液pH
您最近一年使用:0次
名校
2 . 下列说法正确的是
A. 其他条件不变,增大反应容器体积,正逆反应速率不变 其他条件不变,增大反应容器体积,正逆反应速率不变 |
B. ,碳的质量不再改变说明反应已达平衡 ,碳的质量不再改变说明反应已达平衡 |
C.若平均相对分子质量不再随时间变化能说明反应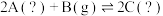 已达平衡,则A、C不能同时是气体 已达平衡,则A、C不能同时是气体 |
D.4mol 分解为 分解为 和 和 的转化率为10%时,吸收热量 的转化率为10%时,吸收热量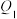 ;在相同温度和压强下,当2mol ;在相同温度和压强下,当2mol 和6mol 和6mol 反应达到平衡时 反应达到平衡时 转化率为10%,放出热量 转化率为10%,放出热量 , , 不等于 不等于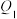 |
您最近一年使用:0次
2023-11-23更新
|
147次组卷
|
2卷引用:北京师范大学附属中学2022-2023学年高二上学期10月月考化学试题
名校
3 . 温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容条件,已知
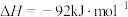 ,测得反应达到平衡时的有关数据如表:
,测得反应达到平衡时的有关数据如表:
下列说法正确的是

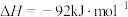 ,测得反应达到平衡时的有关数据如表:
,测得反应达到平衡时的有关数据如表:容器1 | 容器2 | 容器3 | |
| 反应物投入量 |
|
|
|
|
|
|
|
反应的能量变化 | 放出 | 吸收 | 吸收 |
体系的压强 |
|
|
|
反应物的转化率 |
|
|
|
A.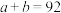 | B. | C. | D.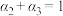 |
您最近一年使用:0次
2023-10-15更新
|
494次组卷
|
2卷引用:北京大学附属中学2023-2024学年高二上学期10月月考化学试题
名校
解题方法
4 . 二硫化碳 是一种重要的溶剂,对
是一种重要的溶剂,对 在内的许多物质具有特殊的溶解能力。在工业生产中用硫
在内的许多物质具有特殊的溶解能力。在工业生产中用硫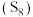 与
与 为原料制备
为原料制备 ,发生以下两个连续反应:反应Ⅰ:
,发生以下两个连续反应:反应Ⅰ: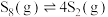 ;反应Ⅱ:
;反应Ⅱ: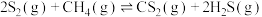 。一定条件下,
。一定条件下, 分解产生
分解产生 的体积分数、
的体积分数、 与
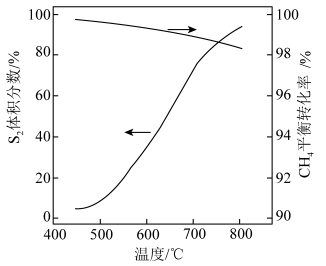
与 反应中
反应中 的平衡转化率与温度的关系如图所示。下列说法不正确的是
的平衡转化率与温度的关系如图所示。下列说法不正确的是
 是一种重要的溶剂,对
是一种重要的溶剂,对 在内的许多物质具有特殊的溶解能力。在工业生产中用硫
在内的许多物质具有特殊的溶解能力。在工业生产中用硫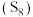 与
与 为原料制备
为原料制备 ,发生以下两个连续反应:反应Ⅰ:
,发生以下两个连续反应:反应Ⅰ: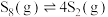 ;反应Ⅱ:
;反应Ⅱ: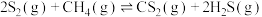 。一定条件下,
。一定条件下, 分解产生
分解产生 的体积分数、
的体积分数、 与
与 反应中
反应中 的平衡转化率与温度的关系如图所示。下列说法不正确的是
的平衡转化率与温度的关系如图所示。下列说法不正确的是
| A.反应Ⅱ的正反应为放热反应 |
B.通过增大 的浓度可以提高 的浓度可以提高 的转化率 的转化率 |
C.增加压强既能提高 的反应速率,又能提高 的反应速率,又能提高 的转化率 的转化率 |
D.制备 时温度需高于600℃的原因是:此温度 时温度需高于600℃的原因是:此温度 平衡转化率已很高,低于此温度, 平衡转化率已很高,低于此温度, 浓度小,反应速率慢 浓度小,反应速率慢 |
您最近一年使用:0次
2023-10-15更新
|
270次组卷
|
2卷引用:北京大学附属中学2023-2024学年高二上学期10月月考化学试题
名校
解题方法
5 . CH4和CO2联合重整能减少温室气体的排放。其主要反应为:
①CH4(g)+CO2(g) 2H2(g)+2CO(g)
2H2(g)+2CO(g)
②H2(g)+CO2(g) H2O(g)+CO(g)
H2O(g)+CO(g)
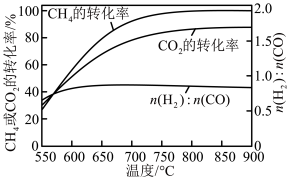
其他条件相同时,投料比n(CH4):n(CO2)为1∶1.3,不同温度下反应的结果如图。
下列说法不正确 的是
①CH4(g)+CO2(g)
 2H2(g)+2CO(g)
2H2(g)+2CO(g)②H2(g)+CO2(g)
 H2O(g)+CO(g)
H2O(g)+CO(g)其他条件相同时,投料比n(CH4):n(CO2)为1∶1.3,不同温度下反应的结果如图。

下列说法
| A.550~600℃,升温更有利于反应①,反应①先达到平衡 |
| B.n(H2)∶n(CO)始终低于1.0,与反应②有关 |
| C.加压有利于增大CH4和CO2反应的速率但不利于提高二者的平衡转化率 |
| D.若不考虑其他副反应,体系中存在:4[c(CH4)+c(CO)+c(CO2)]=2.3[4c(CH4)+2c(H2)+2c(H2O)] |
您最近一年使用:0次
2023-03-31更新
|
1524次组卷
|
12卷引用:北京市第一○一中学2023-2024学年高三上学期10月月考化学试题
北京市第一○一中学2023-2024学年高三上学期10月月考化学试题北京市清华大学附属中学2023-2024学年高三上学期12月统练(六)化学试题北京市第八中学2023-2024学年高三上学期12月月考化学试题北京市西城区2023届一模考试化学试题(已下线)专题15 化学反应速率和化学平衡北京市十一学校2022-2023学年高二下学期期末考试化学试题北京市第六十六中学2023-2024学年高二上学期期中质量检测化学试题北京师范大学附属中学2023-2024学年高三上学期期中考试化学试题陕西省咸阳市实验中学2023-2024学年高二上学期段性检测(二)化学试题安徽省淮北市第一中学2023-2024学年高二上学期第三次月考化学试题(已下线)化学-2023年高考押题预测卷03(江苏卷)(含考试版、全解全析、参考答案、答题卡)江苏省南京师范大学附属中学2023届高三下学期5月模拟考试化学试题
名校
解题方法
6 . 下列实验中,对现象的解释不正确 的是
| 选项 | A | B | C | D |
| 装置及操作 |  向右轻轻推动活塞压缩体积 | 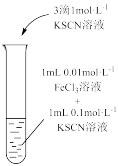 | 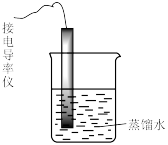 分别测定20℃和80℃蒸馏水的电导率 | 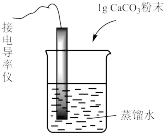 |
| 现象 | 气体红棕色先变深再变浅 | 溶液血红色加深 | 80℃蒸馏水的电导率大于20℃的 | 加入 粉末后电导率增大 粉末后电导率增大 |
| 解释 | 压强增大, 平衡先逆向移动,再正向移动 平衡先逆向移动,再正向移动 | 增大反应物浓度,  平衡正向移动 平衡正向移动 | 温度升高,水的电离平衡正向移动 |  在水中存在 在水中存在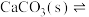  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-06更新
|
929次组卷
|
13卷引用:北京市顺义牛栏山第一中学2022-2023学年高二下学期3月月考化学试题
北京市顺义牛栏山第一中学2022-2023学年高二下学期3月月考化学试题北京市第五十中学2023-2024学年高二上学期12月月考化学试题北京交通大学附属中学第二分校2023-2024学年高二上学期12月月考化学试题北京海淀区2022-2023学年高二上学期期末考试化学试题北京一零一中学2022-2023高二上学期期末考试化学试题北京市首都师范大学附属中学2022-2023学年高二上学期期末考试化学试题北京市顺义牛栏山第一中学2023-2024学年高二上学期期中考试化学试题北京市第三十五中学2023-2024学年高二上学期期中考试化学试题 北京市第十三中学2023-2024学年高二上学期期中考试化学试题北京师范大学附属中学2023-2024学年高二上学期期中考试化学试卷河南省濮阳市第一高级中学2022-2023学年高二下学期期中质量检测化学试题四川省德阳市什邡中学2023-2024学年高二上学期11月期中考试化学试题天津市部分区2023-2024学年高二上学期期末练习化学试题
名校
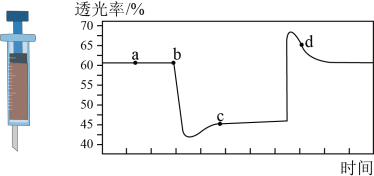
7 . 已知反应:2NO2(红棕色)  N2O4(无色) △H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
N2O4(无色) △H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
 N2O4(无色) △H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
N2O4(无色) △H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
| A.b点的操作是压缩注射器 |
| B.d 点:v正>v逆 |
| C.c点与a点相比,c(NO2)增大,c(N2O4)减小 |
| D.若不忽略体系温度变化,且没有能量损失,则Tb>Tc |
您最近一年使用:0次
2020-04-30更新
|
764次组卷
|
15卷引用:2015届北京市海淀区高三年级3月适应性训练理综化学试卷
2015届北京市海淀区高三年级3月适应性训练理综化学试卷2015届福建省漳州市高三5月适应性考试化学试卷安徽省涡阳县第一中学2019-2020学年高二12月月考化学试题内蒙古自治区赤峰二中2020-2021学年高二上学期第一次月考化学试题北京师范大学第二附属中学未来科技城学校2021-2022学年高二上学期期中考试化学试题重庆市大足中学2022-2023学年高二上学期学期第一次月考化学试题四川省华蓥中学2023-2024学年高二上学期9月月考化学试题北京市第一七一中学2023-2024学年高二上学期期中考试化学试题北京市大兴区兴华中学2023-2024学年高二上学期期中考试化学试题2016-2017学年安徽省师大附中高二上期中化学试卷河北省唐山遵化市2019-2020学年高二上学期期中考试化学试题甘肃省兰州市第一中学2019-2020学年高二上学期期末考试化学试题江西省崇义中学2020-2021学年高一上学期期中考试(A卷)化学试题湖南师范大学附属中学2022-2023学年高一下学期期末考试化学试题江西省宜春市宜丰中学2023-2024学年高二上学期开学考试化学试题

 、
、