名校
1 . 甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、 和
和 )在催化剂作用下可合成甲醇,发生的主要反应如下:
)在催化剂作用下可合成甲醇,发生的主要反应如下:
I.
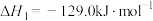
II.

III.

回答下列问题:
(1)
_______ 。
(2)将2.0mol 和3.0mol
和3.0mol  通入容积为3L的恒容密闭容器中,在一定条件下发生反应II,测得
通入容积为3L的恒容密闭容器中,在一定条件下发生反应II,测得 的平衡转化率与温度的关系如图所示。
的平衡转化率与温度的关系如图所示。
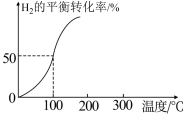
①100℃时反应达到平衡所需的时间为5min,则反应从起始至5min内,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为_______ 。
②100℃时,反应II的平衡常数K=_______ 。
③下列可用来判断该反应已达到平衡状态的有_______ (填标号)。
A.CO的含量保持不变 B.容器中
C.容器中混合气体的密度保持不变 D.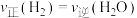
(3)利用天然气制取合成气的原理 ,在密闭容器中通入物质的量浓度均为1
,在密闭容器中通入物质的量浓度均为1 的
的 与
与 ,在一定条件下发生反应,测得
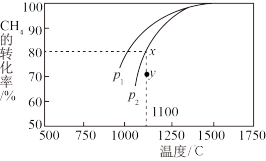
,在一定条件下发生反应,测得 的平衡转化率与温度及压强的关系如图所示,则压强
的平衡转化率与温度及压强的关系如图所示,则压强
_______  (填“大于”或“小于”);压强为
(填“大于”或“小于”);压强为 时,在Y点:
时,在Y点:
_______ 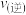 (填“大于”“小于”或“等于”)。为了提高该反应中
(填“大于”“小于”或“等于”)。为了提高该反应中 的转化率,除温度、压强外还可以采取的措施是
的转化率,除温度、压强外还可以采取的措施是_______ 。
 和
和 )在催化剂作用下可合成甲醇,发生的主要反应如下:
)在催化剂作用下可合成甲醇,发生的主要反应如下:I.

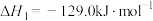
II.


III.


回答下列问题:
(1)

(2)将2.0mol
 和3.0mol
和3.0mol  通入容积为3L的恒容密闭容器中,在一定条件下发生反应II,测得
通入容积为3L的恒容密闭容器中,在一定条件下发生反应II,测得 的平衡转化率与温度的关系如图所示。
的平衡转化率与温度的关系如图所示。
①100℃时反应达到平衡所需的时间为5min,则反应从起始至5min内,用
 表示该反应的平均反应速率为
表示该反应的平均反应速率为②100℃时,反应II的平衡常数K=
③下列可用来判断该反应已达到平衡状态的有
A.CO的含量保持不变 B.容器中

C.容器中混合气体的密度保持不变 D.
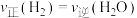
(3)利用天然气制取合成气的原理
 ,在密闭容器中通入物质的量浓度均为1
,在密闭容器中通入物质的量浓度均为1 的
的 与
与 ,在一定条件下发生反应,测得
,在一定条件下发生反应,测得 的平衡转化率与温度及压强的关系如图所示,则压强
的平衡转化率与温度及压强的关系如图所示,则压强
 (填“大于”或“小于”);压强为
(填“大于”或“小于”);压强为 时,在Y点:
时,在Y点:
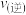 (填“大于”“小于”或“等于”)。为了提高该反应中
(填“大于”“小于”或“等于”)。为了提高该反应中 的转化率,除温度、压强外还可以采取的措施是
的转化率,除温度、压强外还可以采取的措施是
您最近一年使用:0次
2022-11-19更新
|
118次组卷
|
2卷引用:江西省抚州市金溪一中等三校2022-2023年高二上学期第二次联考化学试题
名校
2 . 某温度下,密闭容器中发生反应aX(g) bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积扩大到原来容积的两倍,当达到新平衡时,物质Y和Z的浓度均是原来的0.6倍。则下列叙述正确的是
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积扩大到原来容积的两倍,当达到新平衡时,物质Y和Z的浓度均是原来的0.6倍。则下列叙述正确的是
 bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积扩大到原来容积的两倍,当达到新平衡时,物质Y和Z的浓度均是原来的0.6倍。则下列叙述正确的是
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积扩大到原来容积的两倍,当达到新平衡时,物质Y和Z的浓度均是原来的0.6倍。则下列叙述正确的是| A.可逆反应的化学方程式的化学计量数:a<b+c |
| B.扩大容器的容积时,v正增大,v逆减小 |
| C.达到新平衡时,物质X的转化率减小 |
| D.达到新平衡时,混合物中Z的质量分数减小 |
您最近一年使用:0次
名校
3 . 在一密闭容器中,反应aA(g) bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的60%,则
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的60%,则
 bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的60%,则
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的60%,则| A.平衡向逆反应方向移动了 | B.物质A的转化率减小了 |
| C.物质B的质量分数增加了 | D.a<b |
您最近一年使用:0次
2020-11-12更新
|
102次组卷
|
2卷引用:河北省石家庄市辛集市育才中学2023-2024学年高三上学期12月月考化学试题
名校
解题方法
4 . 将2mol  和1mol
和1mol  分别置于相同温度下相同体积的甲乙两密闭容器中发生反应:
分别置于相同温度下相同体积的甲乙两密闭容器中发生反应: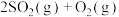
 并达到平衡,甲容器始终保持恒温恒容,乙容器始终保持恒温恒压,达到平衡时,下述说法不正确的是
并达到平衡,甲容器始终保持恒温恒容,乙容器始终保持恒温恒压,达到平衡时,下述说法不正确的是
 和1mol
和1mol  分别置于相同温度下相同体积的甲乙两密闭容器中发生反应:
分别置于相同温度下相同体积的甲乙两密闭容器中发生反应: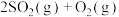
 并达到平衡,甲容器始终保持恒温恒容,乙容器始终保持恒温恒压,达到平衡时,下述说法不正确的是
并达到平衡,甲容器始终保持恒温恒容,乙容器始终保持恒温恒压,达到平衡时,下述说法不正确的是A.平衡时 的百分含量:乙<甲 的百分含量:乙<甲 | B. 的转化率:乙>甲 的转化率:乙>甲 |
| C.反应速率:乙>甲 | D.平衡时容器的压强:乙>甲 |
您最近一年使用:0次
2022-11-18更新
|
394次组卷
|
4卷引用:四川省双流棠湖中学2023-2024学年高二上学期9月月考化学试题
名校
5 . 氨在国民经济中占有重要地位。
(1)合成氨工业中,合成塔中每产生2mol ,放出92.2kJ热量。写出合成氨反应的热化学方程式
,放出92.2kJ热量。写出合成氨反应的热化学方程式_______ ;该可逆反应,若起始时向容器内放入2mol  和6mol
和6mol  ,达平衡后放出的热量为Q,则Q(填“>”、“<”或“=”)
,达平衡后放出的热量为Q,则Q(填“>”、“<”或“=”)_______ 184.4kJ。
(2)反应 的化学平衡常数表达式为
的化学平衡常数表达式为_______ 。请结合下列数据分析,工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是_______ 。
(3)在一定条件下氨的平衡含量如下表。
其他条件不变时,温度升高氨的平衡含量改变的原因是_______ (填字母序号)。
a.温度升高,正反应速率减小,逆反应速率增大,平衡逆向移动
b.温度升高,浓度商(Q)变大,Q>K,平衡逆向移动
c.温度升高,活化分子数增多,反应速率加快
d.温度升高,K变小,平衡逆向移动
哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是_______ 。
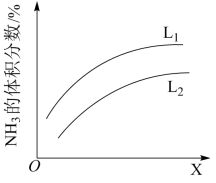
(4)如图是合成氨反应平衡混合气中 的体积分数随温度或压强变化的曲线,图中L(
的体积分数随温度或压强变化的曲线,图中L( 、
、 )、X分别代表温度或压强。其中X代表的是
)、X分别代表温度或压强。其中X代表的是_______ (填“温度”或“压强”);判断小 、
、 的大小关系并说明理由
的大小关系并说明理由_______ 。
(1)合成氨工业中,合成塔中每产生2mol
 ,放出92.2kJ热量。写出合成氨反应的热化学方程式
,放出92.2kJ热量。写出合成氨反应的热化学方程式 和6mol
和6mol  ,达平衡后放出的热量为Q,则Q(填“>”、“<”或“=”)
,达平衡后放出的热量为Q,则Q(填“>”、“<”或“=”)(2)反应
 的化学平衡常数表达式为
的化学平衡常数表达式为| 序号 | 化学反应 | K(298K)的数值 |
| ① |  |  |
| ② |  | 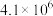 |
| 温度/℃ | 压强/Mpa | 氨的平衡含量 |
| 200 | 10 | 81.5% |
| 550 | 10 | 8.25% |
a.温度升高,正反应速率减小,逆反应速率增大,平衡逆向移动
b.温度升高,浓度商(Q)变大,Q>K,平衡逆向移动
c.温度升高,活化分子数增多,反应速率加快
d.温度升高,K变小,平衡逆向移动
哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是
(4)如图是合成氨反应平衡混合气中
 的体积分数随温度或压强变化的曲线,图中L(
的体积分数随温度或压强变化的曲线,图中L( 、
、 )、X分别代表温度或压强。其中X代表的是
)、X分别代表温度或压强。其中X代表的是 、
、 的大小关系并说明理由
的大小关系并说明理由
您最近一年使用:0次
2022-11-06更新
|
109次组卷
|
3卷引用:新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二上学期第三次月考化学试卷
名校
解题方法
6 . 根据图示,下列得出的结论错误的是
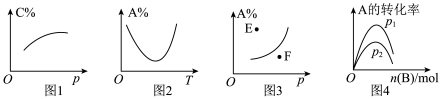

A.图1是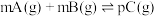 中平衡时C的百分含量与压强的关系,说明m+n>p 中平衡时C的百分含量与压强的关系,说明m+n>p |
B.图2是A+B C中A的百分含量随温度变化的曲线,说明该反应是放热反应 C中A的百分含量随温度变化的曲线,说明该反应是放热反应 |
C.图3是对于反应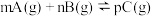 ,当其他条件一定时A的百分含量随压强变化的图像,其中E点v正>v逆 ,当其他条件一定时A的百分含量随压强变化的图像,其中E点v正>v逆 |
D.图4是对于反应 在一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强p1>p2 在一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强p1>p2 |
您最近一年使用:0次
名校
解题方法
7 . 现有反应

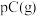 ,达到平衡后,升高温度,B的转化率变大;减小压强,混合物体系中C的质量分数减小,则:
,达到平衡后,升高温度,B的转化率变大;减小压强,混合物体系中C的质量分数减小,则:
(1)该反应的逆反应为________ (填“放热”或“吸热”)反应,且
________ (填“>”“=”或“<”)p。
(2)在恒容条件下加入B,则A的转化率________ (填“增大”“减小”或“不变”,下同),B的转化率________ 。
(3)若升高温度,则平衡时B、C的浓度之比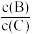 将
将________ (填“增大”“减小”或“不变”)。
(4)若B是有色物质,A、C均无色,则加入C(容器容积不变)时混合物的颜色________ (填“变深”“变浅”或“不变”,下同);而维持容器内压强不变,充入氖气时,混合物的颜色________ 。


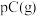 ,达到平衡后,升高温度,B的转化率变大;减小压强,混合物体系中C的质量分数减小,则:
,达到平衡后,升高温度,B的转化率变大;减小压强,混合物体系中C的质量分数减小,则:(1)该反应的逆反应为

(2)在恒容条件下加入B,则A的转化率
(3)若升高温度,则平衡时B、C的浓度之比
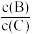 将
将(4)若B是有色物质,A、C均无色,则加入C(容器容积不变)时混合物的颜色
您最近一年使用:0次
2020-10-06更新
|
445次组卷
|
5卷引用:黑龙江嫩江市高级中学等八校2021-2022学年高二上学期9月联合考试化学试题
黑龙江嫩江市高级中学等八校2021-2022学年高二上学期9月联合考试化学试题辽宁师范大学附属中学2021-2022学年高二上学期10月月考化学试题步步为赢 高二化学寒假作业:作业四 化学平衡移动原理人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第二节 化学平衡(已下线)选择性必修1 期中检测(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)
名校
8 . 某温度下,密闭容器中发生反应aX(g)+bY(g) cZ(s)+dW(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y的浓度是原来的1.8倍。则正确的是
cZ(s)+dW(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y的浓度是原来的1.8倍。则正确的是
 cZ(s)+dW(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y的浓度是原来的1.8倍。则正确的是
cZ(s)+dW(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y的浓度是原来的1.8倍。则正确的是| A.可逆反应的系数:a+b>c+d | B.压缩容器的容积时,v(正)=v(逆) |
| C.达到新平衡时,物质X的转化率减小 | D.达到新平衡时,混合物中W的质量分数增大 |
您最近一年使用:0次
2021-06-28更新
|
540次组卷
|
8卷引用:安徽省淮北市树人高级中学2020-2021学年高二下学期第二次月考化学试题
安徽省淮北市树人高级中学2020-2021学年高二下学期第二次月考化学试题黑龙江省佳木斯学校(佳木斯市实验中学)2021-2022学年高二上学期第二次月考化学试题江西省兴国县将军中学2021-2022学年高二上学期10月月考化学试题辽宁省新民市第一高级中学2021-2022学年高二上学期10月月考化学试题山东省东明县第一中学2023-2024学年高二上学期10月月考化学试题(已下线)第二章 第三节 化学平衡(第1课时 化学平衡状态)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)2.3.2 压强变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)山东省枣庄市第三中学2022-2023学年高二上学期期中考试化学试题
9 . 反应Ⅰ、Ⅱ、Ⅲ均会在工业生产硝酸过程中发生,其中反应Ⅰ、Ⅱ发生在氧化炉中,反应Ⅲ发生在氧化塔中,不同温度下各反应的化学平衡常数如下表所示。下列说法正确的是
| 温度/K | 化学平衡常数 | |||
| 反应Ⅰ:4NH3+5O2=4NO+6H2O | 反应Ⅱ:4NH3+3O2=2N2+6H2O | 反应Ⅲ:2NO+O2=2NO2 | ||
| 500 | 1.1×1026 | 7.1×1034 | 1.3×102 | |
| 700 | 2.1×1019 | 2.6×1025 | 1.0 | |
| A.使用选择性催化反应Ⅰ的催化剂不能增大氧化炉中NO的含量 |
| B.通过改变氧化炉的温度可促进反应Ⅰ而抑制反应Ⅱ |
| C.通过改变氧化炉的压强可促进反应Ⅰ而抑制反应Ⅱ |
| D.氧化炉出气在进入氧化塔前应进一步降低温度 |
您最近一年使用:0次
2022-10-11更新
|
114次组卷
|
2卷引用:山东省莱州一中2022-2023学年高二上学期第一次月考化学试题
名校
10 . 某温度下,密闭容器中发生反应aX(g) bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y的浓度是原来的1.8倍。则下列叙述正确的是
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y的浓度是原来的1.8倍。则下列叙述正确的是
 bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y的浓度是原来的1.8倍。则下列叙述正确的是
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y的浓度是原来的1.8倍。则下列叙述正确的是 | A.可逆反应的系数:a>b +c |
| B.压缩容器的容积时,v(正)=v(逆) |
| C.达到新平衡时,混合物中Z的质量分数增大 |
| D.达到新平衡时,物质X的转化率减小 |
您最近一年使用:0次
2020-12-27更新
|
113次组卷
|
2卷引用:辽宁省葫芦岛市第八高级中学2021-2022学年高二上学期实验班第一次月考化学试题



