名校
解题方法
1 . 工业上可通过甲醇羰基化法制取甲酸甲酯( ):
):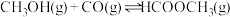 ,在容积固定的密闭容器中,投入等物质的量
,在容积固定的密闭容器中,投入等物质的量 和CO,测得相同时间内CO的转化率随温度变化如下图所示。下列说法
和CO,测得相同时间内CO的转化率随温度变化如下图所示。下列说法不正确 的是

 ):
):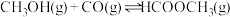 ,在容积固定的密闭容器中,投入等物质的量
,在容积固定的密闭容器中,投入等物质的量 和CO,测得相同时间内CO的转化率随温度变化如下图所示。下列说法
和CO,测得相同时间内CO的转化率随温度变化如下图所示。下列说法
| A.增大压强甲醇转化率增大 |
B.b点反应速率 |
C.平衡常数 ,反应速率 ,反应速率 |
| D.生产时反应温度控制在80~85℃为宜 |
您最近一年使用:0次
2022-05-10更新
|
889次组卷
|
29卷引用:北京市八十中2020-2021学年高二下学期开学考试化学试题
北京市八十中2020-2021学年高二下学期开学考试化学试题北京市大兴区2020-2021学年高二上学期期末考试化学试题辽宁省营口市第二高级中学2021-2022学年高二上学期第一次月考化学试题北京市回民学校2021-2022学年高二上学期期中考试化学试题(已下线)综合复习与测试(2)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)福建省三明第一中学2021-2022学年高二上学期第二次月考化学试题北京市师范大学亚太实验学校2021-2022学年高二上学期期中考试化学试题北京市第四十四中学2021-2022学年高二上学期期中考试化学试题北京市第四中学顺义分校2021-2022学年高二上学期期中考试化学试题陕西省西安市雁塔区第二中学2021-2022学年高二上学期第一次月考化学试题北京市第四十三中学2021-2022学年高二上学期12月月考化学试题北京市西城区2019-2020学年度高二上学期期末考试化学试题北京市中央民族大学附属中学2019-2020学年高二下学期期末考试化学试题人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第二节 化学平衡北京市第四十三中学2020-2021学年高二上学期12月月考化学试题江苏省海安高级中学2020-2021学年度高二上学期第二次合格性考试化学(选修)试题福建省莆田第一中学2021-2022学年高二下学期期中考试化学试题北京市北京师范大学附属实验中学2021-2022学年高一下学期练习卷化学试题(已下线)第11练 以化学平衡图像突破化学平衡移动原理-2022年【暑假分层作业】高二化学(2023届一轮复习通用)河北省石家庄新乐市第一中学2022-2023学年高二上学期第一次月考化学试题北京市第七中学2022-2023学年高二上学期期中化学试题北京师范大学附属中学2022-2023学年上学期高二化学期末试题云南省昌宁县第一中学2022-2023学年高二下学期期末考试化学试题北京市育才学校2023-2024学年高二上学期10月月考化学试题北京市西城区2022-2023学年育才学校高二上学期化学期中考试北京市第二十二中学2023-2024学年高二上学期期中考试化学试题北京市2023-2024学年第二十二中学高二上学期化学期中试题北京市第一六六中学2022-2023学年高二上学期期中考试化学试卷北京市第十一中学2022-2023学年高二上学期期中考试化学试卷
名校
解题方法
2 . 通过反应Ⅰ: 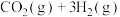

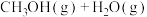
 ,可以实现温室气体资源化利用。该反应通过如下步骤实现:
,可以实现温室气体资源化利用。该反应通过如下步骤实现:
反应Ⅱ:
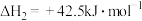
反应Ⅲ:
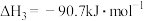
密闭容器中,反应物起始物质的量比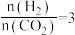 时,在不同条件下(分别在温度为250℃下压强变化和在压强为
时,在不同条件下(分别在温度为250℃下压强变化和在压强为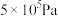 下温度变化)达到平衡时
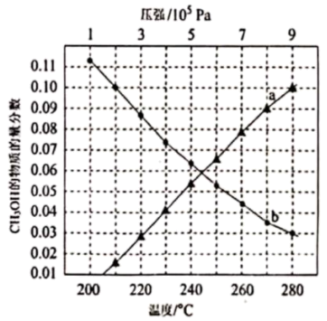
下温度变化)达到平衡时 物质的量分数变化如图所示。下列有关说法正确的是
物质的量分数变化如图所示。下列有关说法正确的是
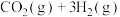

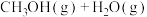
 ,可以实现温室气体资源化利用。该反应通过如下步骤实现:
,可以实现温室气体资源化利用。该反应通过如下步骤实现:反应Ⅱ:

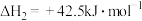
反应Ⅲ:

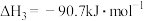
密闭容器中,反应物起始物质的量比
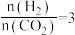 时,在不同条件下(分别在温度为250℃下压强变化和在压强为
时,在不同条件下(分别在温度为250℃下压强变化和在压强为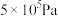 下温度变化)达到平衡时
下温度变化)达到平衡时 物质的量分数变化如图所示。下列有关说法正确的是
物质的量分数变化如图所示。下列有关说法正确的是
A.反应Ⅰ的平衡常数可表示为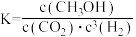 |
B.曲线 表示CH3OH的物质的量分数随温度变化 表示CH3OH的物质的量分数随温度变化 |
| C.提高CO2转化为CH3OH的转化率,需要研发在低温区高效的催化剂 |
D.在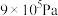 、280℃条件下,平衡时CH3OH的物质的量分数为0.10 、280℃条件下,平衡时CH3OH的物质的量分数为0.10 |
您最近一年使用:0次
2021-09-11更新
|
386次组卷
|
3卷引用:江苏省苏州市2021-2022学年高三上学期期初调研考试化学试题
3 . 一定压强下,向 10 L 密闭容器中充入 1 mol S2Cl2和 1 mol Cl2,发生反应 S2Cl2(g)+Cl2(g) 2SCl2(g)。Cl2与 SCl2的消耗速率(v)与温度(T)的关系如图所示,以下说法中不正确的是
2SCl2(g)。Cl2与 SCl2的消耗速率(v)与温度(T)的关系如图所示,以下说法中不正确的是
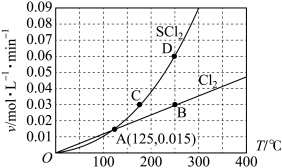
 2SCl2(g)。Cl2与 SCl2的消耗速率(v)与温度(T)的关系如图所示,以下说法中不正确的是
2SCl2(g)。Cl2与 SCl2的消耗速率(v)与温度(T)的关系如图所示,以下说法中不正确的是
| A.正反应的活化能大于逆反应的活化能 |
| B.达到平衡后再加热,平衡向逆反应方向移动 |
| C.A、B、C、D 四点对应状态下,达到平衡状态的为 B、D |
| D.一定温度下,在恒容密闭容器中,达到平衡后缩小容器体积,重新达到平衡后,Cl2的平衡转化率不变 |
您最近一年使用:0次
2021-03-26更新
|
158次组卷
|
4卷引用:浙江省湖州市德清县第三中学2020-2021学年高二下学期返校考试化学试题
2021·江苏南京·模拟预测
名校
4 . 工业上利用炭和水蒸气反应:C(s)+H2O(g)  CO(g)+H2(g)、CO(g)+H2O(g)
CO(g)+H2(g)、CO(g)+H2O(g)  CO2(g)+H2(g)生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO
CO2(g)+H2(g)生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO 能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。下列有关说法正确的是
能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。下列有关说法正确的是
 CO(g)+H2(g)、CO(g)+H2O(g)
CO(g)+H2(g)、CO(g)+H2O(g)  CO2(g)+H2(g)生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO
CO2(g)+H2(g)生成的H2为原料合成氨。在饱和食盐水中先通NH3,后通CO2,由于HCO 能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。下列有关说法正确的是
能形成多聚体,所以容易析出NaHCO3,过滤后热分解得纯碱。下列有关说法正确的是| A.增大压强有利于提高上述反应中焦炭的利用率 |
B.NaHCO3溶液中,HCO 能形成多聚体是因为氢键的作用 能形成多聚体是因为氢键的作用 |
| C.若反应体系中,c(CO)=a mol·L-1,c(CO2)=b mol·L-1,则c(H2)=(a+b) mol·L-1 |
| D.析出NaHCO3的反应属于氧化还原反应 |
您最近一年使用:0次
名校
解题方法
5 . 在容积恒为1 L的密闭容器中通入一定量N2O4,发生反应 △H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是
△H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是
 △H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是
△H>0。假设温度不变,体系中各组分浓度随时间(t)的变化如下表。下列说法错误的是| t/s | 0 | 20 | 40 | 60 | 80 |
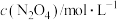 | 0.100 | 0.062 | 0.048 | 0.040 | 0.040 |
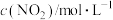 | 0 | 0.076 | 0.104 | 0.120 | 0.120 |
A.0~40 s,N2O4的平均反应速率为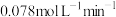 |
| B.80 s时,再充入N2O4、NO2各0.12 mol,平衡移动 |
| C.升高温度,反应的化学平衡常数值增大 |
| D.若压缩容器,达新平衡后,混合气颜色比原平衡时深 |
您最近一年使用:0次
2021-09-12更新
|
402次组卷
|
2卷引用:山东省济南市历城第二中学2021-2022学年(2022届)高三上学期开学考试(B)化学试题
名校
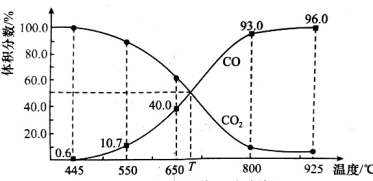
6 . 一定量的 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应: 。平衡时,体系中气体体积分数与温度的关系如图所示,已知:气体分压
。平衡时,体系中气体体积分数与温度的关系如图所示,已知:气体分压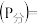 气体总压
气体总压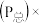 体积分数。下列说法不正确的是
体积分数。下列说法不正确的是
 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应: 。平衡时,体系中气体体积分数与温度的关系如图所示,已知:气体分压
。平衡时,体系中气体体积分数与温度的关系如图所示,已知:气体分压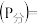 气体总压
气体总压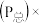 体积分数。下列说法不正确的是
体积分数。下列说法不正确的是
A.该反应 , , |
B.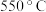 时,若充入惰性气体, 时,若充入惰性气体, , , 均减小,平衡向正反应方向移动 均减小,平衡向正反应方向移动 |
C. 时,若充入等体积的 时,若充入等体积的 和 和 ,平衡向逆反应方向移动 ,平衡向逆反应方向移动 |
D.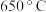 时,反应达平衡后 时,反应达平衡后 的转化率为 的转化率为 |
您最近一年使用:0次
2021-09-10更新
|
261次组卷
|
3卷引用:山西省运城市2022届高三上学期入学摸底测试化学试题
7 . 下列有关化学平衡的说法正确的是
A.对于恒温密闭容器中进行的反应N2(g)+3H2(g) 2NH3(g),若N2的体积分数保持不变,则一定说明反应已达到平衡状态 2NH3(g),若N2的体积分数保持不变,则一定说明反应已达到平衡状态 |
| B.一定温度下,将2.0g CaCO3固体置于1L恒容密闭容器中充分反应后,c(CO2)=0.0125mol/L,若保持温度不变,将容器体积扩大至2L,达到新平衡后c(CO2)=0.01mol/L |
C.反应:CH4(g)+H2O(g) CO(g)+3H2(g) ∆H>0,在其它条件不变的情况下,升高温度、减小容器体积、增大水蒸气的浓度均能提高CH4的平衡转化率 CO(g)+3H2(g) ∆H>0,在其它条件不变的情况下,升高温度、减小容器体积、增大水蒸气的浓度均能提高CH4的平衡转化率 |
D.一定温度下,恒容密闭容器中充入一定量NO2发生反应:2NO2 N2O4达到平衡后,再向容器中充入一定量的NO2并达到新的平衡,则NO2体积分数先增大后减小,但比原平衡小 N2O4达到平衡后,再向容器中充入一定量的NO2并达到新的平衡,则NO2体积分数先增大后减小,但比原平衡小 |
您最近一年使用:0次
名校
解题方法
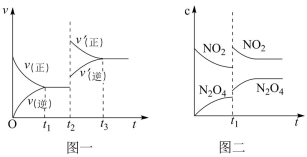
8 . 已知图一表示的是可逆反应C(s)+H2O(g) CO(g)+H2(g)△H<0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应N2O4(g)
CO(g)+H2(g)△H<0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应N2O4(g) 2NO2(g)△H>0的浓度(c)随时间(t)的变化情况。下列说法中正确的是
2NO2(g)△H>0的浓度(c)随时间(t)的变化情况。下列说法中正确的是
 CO(g)+H2(g)△H<0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应N2O4(g)
CO(g)+H2(g)△H<0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应N2O4(g) 2NO2(g)△H>0的浓度(c)随时间(t)的变化情况。下列说法中正确的是
2NO2(g)△H>0的浓度(c)随时间(t)的变化情况。下列说法中正确的是
| A.图一t2时改变的条件可能是升高了温度或增大了压强 |
| B.图一t2时改变的条件是增大压强,则反应的△H增大 |
| C.图二t1时改变的条件可能是升高了温度 |
| D.若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将增大 |
您最近一年使用:0次
2021-03-04更新
|
899次组卷
|
8卷引用:新疆乌苏市第一中学2020-2021学年高二下学期入学检测化学(4-21班)试题
新疆乌苏市第一中学2020-2021学年高二下学期入学检测化学(4-21班)试题(已下线)周末培优1 化学反应速率与化学平衡图像问题-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第2章 化学反应速率和化学平衡(选拔卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)四川省成都市简阳市阳安中学2021-2022学年高二上学期9月月考化学试卷广东省佛山市南海区桂城中学2021-2022学年高二上学期第一次月考化学试题(已下线)2.4 化学反应的调控(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)广东省徐闻县徐闻中学2022-2023学年高二上学期开学测试化学试题广东省广州市四校联考2022-2023学年高二上学期第一次月考化学试题
20-21高二下·江苏南京·期末
9 . NO2与N2O4能相互转化,热化学方程式为N2O4(g)⇌2NO2(g) ΔH=57kJ·mol-1,下列有关说法不 正确的是
| A.升高体系温度正反应速率增大,逆反应速率减小 |
| B.若容器体积不变,气体颜色不变时说明该反应建立化学平衡 |
C.其它条件不变,向平衡后的容器中再加入少量NO2, 的值不变 的值不变 |
| D.其他条件不变,减小体系的压强会提高N2O4的转化率 |
您最近一年使用:0次
2021-06-24更新
|
446次组卷
|
5卷引用:2021年秋季高三开学摸底考化学试卷02(江苏专用)
(已下线)2021年秋季高三开学摸底考化学试卷02(江苏专用)江苏省南京市六校联考2020-2021学年高二下学期期末考试化学试题(已下线)2.3.2 影响化学平衡状态的因素-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第2章基础巩固测评卷-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第2章能力提升测评卷-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)
10 . 在硫酸工业中,通过下列反应使SO2氧化为SO3:2SO2(g)+O2(g) 2SO3(g) △H=-196.6kJ/mol。下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。下列说法错误的是
2SO3(g) △H=-196.6kJ/mol。下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。下列说法错误的是
 2SO3(g) △H=-196.6kJ/mol。下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。下列说法错误的是
2SO3(g) △H=-196.6kJ/mol。下表列出了在不同温度和压强下,反应达到平衡时SO2的转化率。下列说法错误的是温度/℃ | 平衡时SO2的转化率/% | ||||
0.1MPa | 0.5MPa | 1MPa | 5MPa | 10MPa | |
450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
500 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
| A.从理论上分析,为了使二氧化硫尽可能多转化为三氧化硫,应选择的条件是450℃,10MPa |
| B.在实际生产中,选定的温度为400~500℃原因是考虑催化剂的活性最佳 |
| C.在实际生产中,为了增大SO2的转化率可以无限量通入空气 |
| D.在实际生产中,采用的压强为常压原因是常压时转化率已经很高,增大压强对设备及成本要求太高 |
您最近一年使用:0次
2021-01-15更新
|
294次组卷
|
3卷引用:山西省汾阳市汾阳中学2020-2021学年高二下学期开学考试化学试题
山西省汾阳市汾阳中学2020-2021学年高二下学期开学考试化学试题辽宁省丹东市2020-2021学年高二上学期期末考试化学试题(已下线)第29练 化学反应的调控-2023年高考化学一轮复习小题多维练(全国通用)



