真题
解题方法
1 . 氢能是理想清洁能源,氢能产业链由制氢、储氢和用氢组成。
(1)利用铁及其氧化物循环制氢,原理如图所示。反应器Ⅰ中化合价发生改变的元素有_______ ;含CO和 各1mol的混合气体通过该方法制氢,理论上可获得
各1mol的混合气体通过该方法制氢,理论上可获得_______ 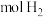 。
。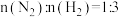 混合匀速通入合成塔,发生反应
混合匀速通入合成塔,发生反应 。海绵状的
。海绵状的 作催化剂,多孔
作催化剂,多孔 作为
作为 的“骨架”和气体吸附剂。
的“骨架”和气体吸附剂。
① 中含有CO会使催化剂中毒。
中含有CO会使催化剂中毒。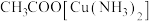 和氨水的混合溶液能吸收CO生成
和氨水的混合溶液能吸收CO生成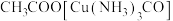 溶液,该反应的化学方程式为
溶液,该反应的化学方程式为_______ 。
② 含量与
含量与 表面积、出口处氨含量关系如图所示。
表面积、出口处氨含量关系如图所示。 含量大于
含量大于 ,出口处氨含量下降的原因是
,出口处氨含量下降的原因是_______ 。 可用于储氢。
可用于储氢。
①密闭容器中,其他条件不变,向含有催化剂的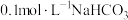 溶液中通入
溶液中通入 ,
, 产率随温度变化如图所示。温度高于
产率随温度变化如图所示。温度高于 ,
, 产率下降的可能原因是
产率下降的可能原因是_______ 。 ,CN是一种碳衍生材料)联合
,CN是一种碳衍生材料)联合 催化剂储氢,可能机理如图所示。氨基能将
催化剂储氢,可能机理如图所示。氨基能将 控制在催化剂表面,其原理是
控制在催化剂表面,其原理是_______ ;用重氢气(D2)代替H2,通过检测是否存在_______ (填化学式)确认反应过程中的加氢方式。
(1)利用铁及其氧化物循环制氢,原理如图所示。反应器Ⅰ中化合价发生改变的元素有
 各1mol的混合气体通过该方法制氢,理论上可获得
各1mol的混合气体通过该方法制氢,理论上可获得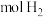 。
。
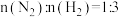 混合匀速通入合成塔,发生反应
混合匀速通入合成塔,发生反应 。海绵状的
。海绵状的 作催化剂,多孔
作催化剂,多孔 作为
作为 的“骨架”和气体吸附剂。
的“骨架”和气体吸附剂。①
 中含有CO会使催化剂中毒。
中含有CO会使催化剂中毒。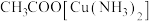 和氨水的混合溶液能吸收CO生成
和氨水的混合溶液能吸收CO生成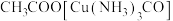 溶液,该反应的化学方程式为
溶液,该反应的化学方程式为②
 含量与
含量与 表面积、出口处氨含量关系如图所示。
表面积、出口处氨含量关系如图所示。 含量大于
含量大于 ,出口处氨含量下降的原因是
,出口处氨含量下降的原因是
 可用于储氢。
可用于储氢。①密闭容器中,其他条件不变,向含有催化剂的
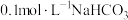 溶液中通入
溶液中通入 ,
, 产率随温度变化如图所示。温度高于
产率随温度变化如图所示。温度高于 ,
, 产率下降的可能原因是
产率下降的可能原因是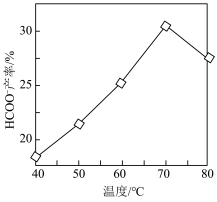
 ,CN是一种碳衍生材料)联合
,CN是一种碳衍生材料)联合 催化剂储氢,可能机理如图所示。氨基能将
催化剂储氢,可能机理如图所示。氨基能将 控制在催化剂表面,其原理是
控制在催化剂表面,其原理是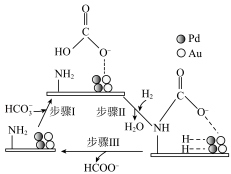
您最近一年使用:0次
名校
2 . 丙烯腈(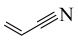 )是一种重要的化工原料,以
)是一种重要的化工原料,以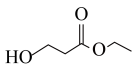 为原料合成丙烯腈的过程如下:
为原料合成丙烯腈的过程如下:

向密闭容器中通入一定量的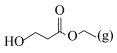 和
和 ,测得平衡时体系中含碳物质(乙醇除外)的物质的量分数[如:丙烯腈的物质的量分数
,测得平衡时体系中含碳物质(乙醇除外)的物质的量分数[如:丙烯腈的物质的量分数 ]随温度的变化如图。下列说法错误的是
]随温度的变化如图。下列说法错误的是
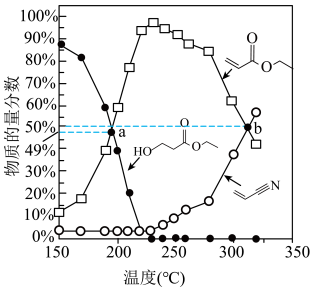
| A.“脱水”反应为吸热反应 |
| B.低于225℃时,“腈化”过程转化率低 |
C.a点 的转化率为51% 的转化率为51% |
D.b点 和 和 的物质的量之比为3:1 的物质的量之比为3:1 |
您最近一年使用:0次
2024-05-24更新
|
201次组卷
|
3卷引用:山东省德州市2024届高三下学期高考适应性练习(二)化学试题
名校
解题方法
3 . 湿法提银工艺中,浸出的Ag+需加入Cl-进行沉淀。25℃时,平衡体系中含Ag微粒的分布系数δ[如δ(AgCl )=
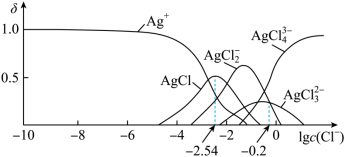
)=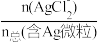 ]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
 )=
)=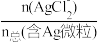 ]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
| A.AgCl溶解度随c(Cl-)增大而不断减小 |
| B.沉淀最彻底时,溶液中c(Ag+)=10-7.21mol•L-1 |
C.当c(Cl-)=10-2mol•L-1时,溶液中c(AgCl )>c(Ag+)>c(AgCl )>c(Ag+)>c(AgCl ) ) |
D.25℃时,AgCl +Cl- +Cl- AgCl AgCl 的平衡常数K=100.2 的平衡常数K=100.2 |
您最近一年使用:0次
名校
解题方法
4 . 汞及其化合物广泛应用于医药、冶金及其他精密高新科技领域。
(1)干燥的 固体上通入
固体上通入 可反应制得
可反应制得 和
和 ,反应的化学方程式为
,反应的化学方程式为___________ 。该反应中氧化产物是___________ 。
(2)富氧燃烧烟气中 的脱除主要是通过与
的脱除主要是通过与 反应实现,反应的化学方程式为
反应实现,反应的化学方程式为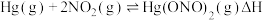
根据实验结果,有研究组提出了 与
与 的可能反应机理:
的可能反应机理:

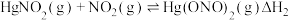

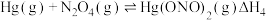
①根据盖斯定律,
___________ (写出一个代数式即可)。
②上述反应体系在一定条件下建立平衡后,下列说法正确的是___________ 。
A.增大 的浓度,可提高
的浓度,可提高 的平衡脱除率
的平衡脱除率
B.升高温度,正反应速率增大,逆反应速率减小
C.恒温恒压下充入 ,可提高原料的平衡转化率
,可提高原料的平衡转化率
D.加入催化剂,可降低反应活化能,提高脱除速率
③在常压、温度范围为15~60℃条件下,将浓度为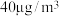 汞蒸气和
汞蒸气和 的
的 气体通入反应容器中,测得出口气流中的汞浓度随反应时间的变化如图1所示。
气体通入反应容器中,测得出口气流中的汞浓度随反应时间的变化如图1所示。 的平均脱除反应速率为
的平均脱除反应速率为___________ 
ⅱ)
___________ 0(填“>”或“<”)
④富氧燃烧烟气中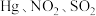 等污染物可通过配有循环水系统的分压精馏塔进行一体化脱除,污染物脱除率随循环水量的变化如图2所示。循环水的加入有利于
等污染物可通过配有循环水系统的分压精馏塔进行一体化脱除,污染物脱除率随循环水量的变化如图2所示。循环水的加入有利于 转化为
转化为 而脱除,但随着循环水量的增大,
而脱除,但随着循环水量的增大, 的去除率下降,其原因可能是
的去除率下降,其原因可能是___________ 。 溶液可用于手术刀消毒。
溶液可用于手术刀消毒。 与
与 的混合溶液中主要存在平衡:
的混合溶液中主要存在平衡:

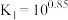
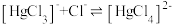
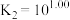
 的
的 溶液中加入
溶液中加入 固体(设溶液体积保持不变),溶液中含氯微粒的物质的量分数
固体(设溶液体积保持不变),溶液中含氯微粒的物质的量分数 随
随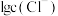 的变化如图所示
的变化如图所示 ]。
]。
①熔融状态的 不能导电,
不能导电, 是
是___________ (填“共价”或“离子”)化合物。
②A点溶液中
___________  。
。
③A点溶液中 的转化率为
的转化率为___________ (列出计算式)。
(1)干燥的
 固体上通入
固体上通入 可反应制得
可反应制得 和
和 ,反应的化学方程式为
,反应的化学方程式为(2)富氧燃烧烟气中
 的脱除主要是通过与
的脱除主要是通过与 反应实现,反应的化学方程式为
反应实现,反应的化学方程式为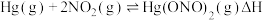
根据实验结果,有研究组提出了
 与
与 的可能反应机理:
的可能反应机理:
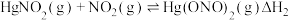

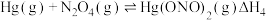
①根据盖斯定律,

②上述反应体系在一定条件下建立平衡后,下列说法正确的是
A.增大
 的浓度,可提高
的浓度,可提高 的平衡脱除率
的平衡脱除率B.升高温度,正反应速率增大,逆反应速率减小
C.恒温恒压下充入
 ,可提高原料的平衡转化率
,可提高原料的平衡转化率D.加入催化剂,可降低反应活化能,提高脱除速率
③在常压、温度范围为15~60℃条件下,将浓度为
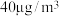 汞蒸气和
汞蒸气和 的
的 气体通入反应容器中,测得出口气流中的汞浓度随反应时间的变化如图1所示。
气体通入反应容器中,测得出口气流中的汞浓度随反应时间的变化如图1所示。
 的平均脱除反应速率为
的平均脱除反应速率为
ⅱ)

④富氧燃烧烟气中
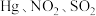 等污染物可通过配有循环水系统的分压精馏塔进行一体化脱除,污染物脱除率随循环水量的变化如图2所示。循环水的加入有利于
等污染物可通过配有循环水系统的分压精馏塔进行一体化脱除,污染物脱除率随循环水量的变化如图2所示。循环水的加入有利于 转化为
转化为 而脱除,但随着循环水量的增大,
而脱除,但随着循环水量的增大, 的去除率下降,其原因可能是
的去除率下降,其原因可能是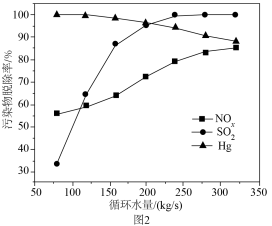
 溶液可用于手术刀消毒。
溶液可用于手术刀消毒。 与
与 的混合溶液中主要存在平衡:
的混合溶液中主要存在平衡:
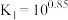
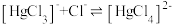
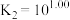
 的
的 溶液中加入
溶液中加入 固体(设溶液体积保持不变),溶液中含氯微粒的物质的量分数
固体(设溶液体积保持不变),溶液中含氯微粒的物质的量分数 随
随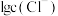 的变化如图所示
的变化如图所示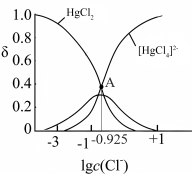
 ]。
]。①熔融状态的
 不能导电,
不能导电, 是
是②A点溶液中

 。
。③A点溶液中
 的转化率为
的转化率为
您最近一年使用:0次
2024-03-01更新
|
525次组卷
|
3卷引用:广东省广州市第二中学2023-2024学年高三上学期期末化学试卷
广东省广州市第二中学2023-2024学年高三上学期期末化学试卷(已下线)大题04 化学反应原理综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)广东省东莞市东华高级中学 东华松山湖高级中学 2024届高三下学期第三次模拟考试 化学试题
2024高三下·全国·专题练习
5 . 空气中CO2含量的控制和CO2资源利用具有重要意义。
已知25℃、101 下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:
下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:
I.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH1=+41.2kJ·mol-1
II.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=-49kJ·mol-1
III.CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH3=-165kJ·mol-1
向刚性密闭容器中通入一定量CO2和H2,发生反应I和反应II,温度对 和CH3OH的物质的量分数影响如图所示。
和CH3OH的物质的量分数影响如图所示。
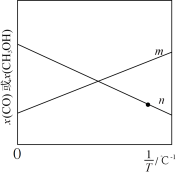
图中表示 物质的量分数的为
物质的量分数的为_______ (填“m”或“n”);为提高CH3OH的选择性,可采取的措施有_______ (写出1条即可)。
已知25℃、101
 下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:
下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:I.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH1=+41.2kJ·mol-1
II.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=-49kJ·mol-1
III.CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH3=-165kJ·mol-1
向刚性密闭容器中通入一定量CO2和H2,发生反应I和反应II,温度对
 和CH3OH的物质的量分数影响如图所示。
和CH3OH的物质的量分数影响如图所示。
图中表示
 物质的量分数的为
物质的量分数的为
您最近一年使用:0次
名校
解题方法
6 . 磷资源流失到水环境中会造成水体富营养化。已知: 基磁性纳米复合材料,由
基磁性纳米复合材料,由 和纳米
和纳米 经过超声分散制得。能通过纳米
经过超声分散制得。能通过纳米 物理吸附和
物理吸附和 溶出后通过化学反应等去除水体磷。已知:纳米
溶出后通过化学反应等去除水体磷。已知:纳米 颗粒表面带正电荷;部分物质的溶解性如下表。
颗粒表面带正电荷;部分物质的溶解性如下表。
(1)制备复合材料所需的纳米 :一定条件下,先将
:一定条件下,先将 和
和 晶体配制成混合溶液,再与氨水反应可制得纳米
晶体配制成混合溶液,再与氨水反应可制得纳米 ,实验装置如下:
,实验装置如下:
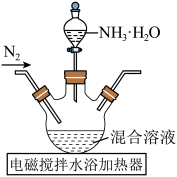
①氨水缓慢滴入,开始一段时间内未出现浑浊,原因是___________ 。
②制备纳米 需控温在50~60°℃之间,写出该反应的化学方程式:
需控温在50~60°℃之间,写出该反应的化学方程式:___________ 。
③配制混合溶液时按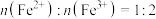 进行投料:实验中需不断通入
进行投料:实验中需不断通入 。通
。通 的目的是
的目的是___________ 。
(2)研究不同pH下向含磷(V)废水中加入 纳米复合材料的除磷效果:
纳米复合材料的除磷效果:
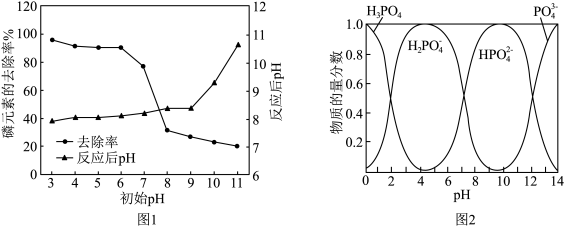
①从图1中可以看出初始pH为3~6时,磷的去除率较高且反应后pH均有一定的上升,反应过程中无气体生成。结合图2,写出对应的离子方程式:___________ 。
②当初始pH为9~10时,磷的去除率明显小于初始pH为3~6的去除率,是因为___________ 。
(3)除磷后续处理
除磷回收得到的磷矿物 ,可进一步转化为
,可进一步转化为 ,作为钾磷复合肥使用。设计由
,作为钾磷复合肥使用。设计由 浆料制备
浆料制备 晶体的实验方案:向含
晶体的实验方案:向含 的浆料中
的浆料中___________ ,干燥。[已知: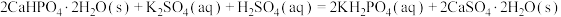 ;室温下从
;室温下从 饱和溶液中可结晶析出
饱和溶液中可结晶析出 晶体;实验中
晶体;实验中须选用 的试剂: 溶液、
溶液、 溶液,pH试纸,无水乙醇]
溶液,pH试纸,无水乙醇]
 基磁性纳米复合材料,由
基磁性纳米复合材料,由 和纳米
和纳米 经过超声分散制得。能通过纳米
经过超声分散制得。能通过纳米 物理吸附和
物理吸附和 溶出后通过化学反应等去除水体磷。已知:纳米
溶出后通过化学反应等去除水体磷。已知:纳米 颗粒表面带正电荷;部分物质的溶解性如下表。
颗粒表面带正电荷;部分物质的溶解性如下表。| 物质 |  |  |  |  |
| 溶解性 | 难溶 | 微溶 | 可溶 | 易溶 |
(1)制备复合材料所需的纳米
 :一定条件下,先将
:一定条件下,先将 和
和 晶体配制成混合溶液,再与氨水反应可制得纳米
晶体配制成混合溶液,再与氨水反应可制得纳米 ,实验装置如下:
,实验装置如下:
①氨水缓慢滴入,开始一段时间内未出现浑浊,原因是
②制备纳米
 需控温在50~60°℃之间,写出该反应的化学方程式:
需控温在50~60°℃之间,写出该反应的化学方程式:③配制混合溶液时按
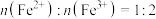 进行投料:实验中需不断通入
进行投料:实验中需不断通入 。通
。通 的目的是
的目的是(2)研究不同pH下向含磷(V)废水中加入
 纳米复合材料的除磷效果:
纳米复合材料的除磷效果:
①从图1中可以看出初始pH为3~6时,磷的去除率较高且反应后pH均有一定的上升,反应过程中无气体生成。结合图2,写出对应的离子方程式:
②当初始pH为9~10时,磷的去除率明显小于初始pH为3~6的去除率,是因为
(3)除磷后续处理
除磷回收得到的磷矿物
 ,可进一步转化为
,可进一步转化为 ,作为钾磷复合肥使用。设计由
,作为钾磷复合肥使用。设计由 浆料制备
浆料制备 晶体的实验方案:向含
晶体的实验方案:向含 的浆料中
的浆料中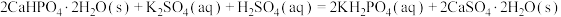 ;室温下从
;室温下从 饱和溶液中可结晶析出
饱和溶液中可结晶析出 晶体;实验中
晶体;实验中 溶液、
溶液、 溶液,pH试纸,无水乙醇]
溶液,pH试纸,无水乙醇]
您最近一年使用:0次
名校
解题方法
7 . 向 溶液中滴加
溶液中滴加 溶液,发生反应
溶液,发生反应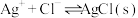 和
和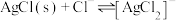 。
。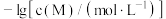 与
与 的关系如下图所示(其中
的关系如下图所示(其中 代表
代表 或
或 )。下列说法错误的是
)。下列说法错误的是
 溶液中滴加
溶液中滴加 溶液,发生反应
溶液,发生反应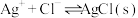 和
和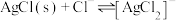 。
。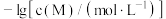 与
与 的关系如下图所示(其中
的关系如下图所示(其中 代表
代表 或
或 )。下列说法错误的是
)。下列说法错误的是
A.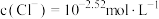 时,溶液中 时,溶液中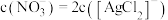 |
B.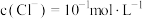 时,溶液中 时,溶液中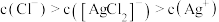 |
C. 的平衡常数 的平衡常数 的值为 的值为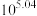 |
D.用 沉淀 沉淀 ,溶液中 ,溶液中 浓度过大时,沉淀效果不好 浓度过大时,沉淀效果不好 |
您最近一年使用:0次
2024-01-22更新
|
1200次组卷
|
6卷引用:2024年1月安徽普通高等学校招生考试适应性测试化学试题
2024年1月安徽普通高等学校招生考试适应性测试化学试题(已下线)选择题11-14(已下线)2024年1月“九省联考”安徽真题完全解读与考后提升(已下线)热点18 电解质溶液图像分析重庆市第八中学2023-2024学年高二下学期第一次月考化学试卷安徽省合肥市第一中学2023-2024学年高二下学期素质拓展(2)化学试题
名校
解题方法
8 . 习近平主席在第75届联合国大会提出:“我国要实现“2030年碳达峰、2060年碳中和的目标”。因此 的捕获利用与封存成为科学家研究的重要课题。
的捕获利用与封存成为科学家研究的重要课题。 和
和 的干法重整(DRM)反应可同时转化两种温室气体,并制备
的干法重整(DRM)反应可同时转化两种温室气体,并制备 和
和 。主要反应如下:
。主要反应如下:
反应Ⅰ: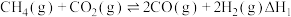 ;
;
反应Ⅱ: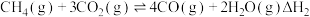 ;
;
反应Ⅲ: ;
;
已知:反应Ⅰ、Ⅱ的自发均需高温条件。
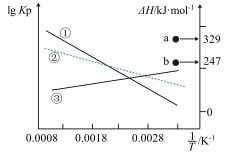
(1)上述三个反应的平衡常数 与温度T关系如图所示。图中a点代表的是
与温度T关系如图所示。图中a点代表的是___________ (填“Ⅰ”“Ⅱ”或“Ⅲ”)反应的 ,
,
___________  。
。
(2)将原料按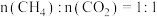 充入密闭容器中发生反应Ⅰ,保持体系压强为
充入密闭容器中发生反应Ⅰ,保持体系压强为 发生反应,达到平衡时
发生反应,达到平衡时 体积分数与温度的关系(图中黑线)如图所示:
体积分数与温度的关系(图中黑线)如图所示:
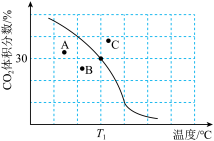
①T1℃,100kPa下,平衡时容器体积与初始容器体积之比为___________ ;该温度下,此反应的平衡常数
___________  (用平衡分压代替平衡浓度计算,分压=总压
(用平衡分压代替平衡浓度计算,分压=总压 物质的量分数)。
物质的量分数)。
②若A、B、C三点表示不同温度和压强下已达平衡时 的体积分数,
的体积分数,___________ 点对应的平衡常数最小,___________ 点对应的压强最大。
(3)在其他条件相同,不同催化剂(A、B)作用下,使原料 和
和 发生反应Ⅰ反应相同的时间,
发生反应Ⅰ反应相同的时间, 的产率随反应温度的变化如图:
的产率随反应温度的变化如图:
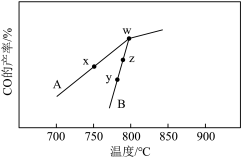
①在催化剂A、B作用下,它们正、逆反应活化能差值分别用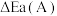 和
和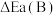 表示,则
表示,则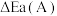
___________ 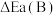 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②y点对应的逆反应速率v(逆)___________ z点对应的正反应速率v()正)(填“>”“<”或“=”)
 的捕获利用与封存成为科学家研究的重要课题。
的捕获利用与封存成为科学家研究的重要课题。 和
和 的干法重整(DRM)反应可同时转化两种温室气体,并制备
的干法重整(DRM)反应可同时转化两种温室气体,并制备 和
和 。主要反应如下:
。主要反应如下:反应Ⅰ:
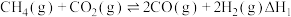 ;
;反应Ⅱ:
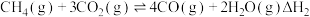 ;
;反应Ⅲ:
 ;
;已知:反应Ⅰ、Ⅱ的自发均需高温条件。
(1)上述三个反应的平衡常数
 与温度T关系如图所示。图中a点代表的是
与温度T关系如图所示。图中a点代表的是 ,
,
 。
。
(2)将原料按
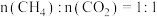 充入密闭容器中发生反应Ⅰ,保持体系压强为
充入密闭容器中发生反应Ⅰ,保持体系压强为 发生反应,达到平衡时
发生反应,达到平衡时 体积分数与温度的关系(图中黑线)如图所示:
体积分数与温度的关系(图中黑线)如图所示:
①T1℃,100kPa下,平衡时容器体积与初始容器体积之比为

 (用平衡分压代替平衡浓度计算,分压=总压
(用平衡分压代替平衡浓度计算,分压=总压 物质的量分数)。
物质的量分数)。②若A、B、C三点表示不同温度和压强下已达平衡时
 的体积分数,
的体积分数,(3)在其他条件相同,不同催化剂(A、B)作用下,使原料
 和
和 发生反应Ⅰ反应相同的时间,
发生反应Ⅰ反应相同的时间, 的产率随反应温度的变化如图:
的产率随反应温度的变化如图:
①在催化剂A、B作用下,它们正、逆反应活化能差值分别用
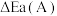 和
和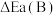 表示,则
表示,则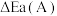
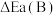 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②y点对应的逆反应速率v(逆)
您最近一年使用:0次
名校
9 . 将 晶体置于真空刚性容器中,升温可发生反应:
晶体置于真空刚性容器中,升温可发生反应: 和
和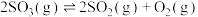 ,该体系达到平衡状态时
,该体系达到平衡状态时 的体积分数
的体积分数 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 晶体置于真空刚性容器中,升温可发生反应:
晶体置于真空刚性容器中,升温可发生反应: 和
和 ,该体系达到平衡状态时
,该体系达到平衡状态时 的体积分数
的体积分数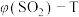 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
A.700 K前,只发生反应 |
B.650 K时,若容器内气体压强为 ,则 ,则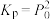 |
C.b点温度下, 分解率为8% 分解率为8% |
| D.在a点容器中加入催化剂,则b点将向上平移 |
您最近一年使用:0次
名校
解题方法
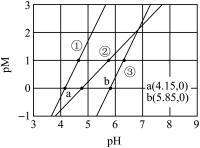
10 . 常温下,向含有CH3COOH、CuSO4、FeSO4的工业废水中逐滴加入NaOH溶液,pM随pH变化关系如图所示[pM表示 或
或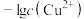 或
或 ],曲线①③斜率相同。已知:
],曲线①③斜率相同。已知: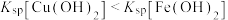 ;当离子浓度
;当离子浓度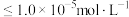 时,可认为该离子沉淀完全。下列说法不正确的是
时,可认为该离子沉淀完全。下列说法不正确的是
 或
或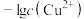 或
或 ],曲线①③斜率相同。已知:
],曲线①③斜率相同。已知: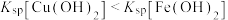 ;当离子浓度
;当离子浓度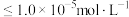 时,可认为该离子沉淀完全。下列说法不正确的是
时,可认为该离子沉淀完全。下列说法不正确的是
A.曲线①表示 与pH的关系 与pH的关系 |
B.pH=6时,溶液中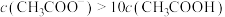 |
C.pH=7时,可认为 沉淀完全 沉淀完全 |
D.pH=8时 |
您最近一年使用:0次
2023-12-01更新
|
423次组卷
|
5卷引用:河北省沧州市部分高中2023-2024学年高三上学期11月期中考试化学试题
河北省沧州市部分高中2023-2024学年高三上学期11月期中考试化学试题(已下线)选择题11-15(已下线)寒假作业07 沉淀溶解平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题江西省宜春市丰城市第九中学2023-2024学年高二下学期4月月考化学试题



