1 . 对于反应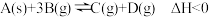 ,下列说法正确的是
,下列说法正确的是
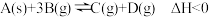 ,下列说法正确的是
,下列说法正确的是| A.加入催化剂,改变了反应的途径,反应的△H也随之改变 |
| B.该反应△S>0,△H<0,在任何条件下能自发进行 |
| C.恒温恒容条件下,混合气体密度不变达到化学平衡状态 |
| D.达到平衡状态后,若增加A的量,平衡向正反应方向移动 |
您最近一年使用:0次
2021-06-28更新
|
919次组卷
|
6卷引用:浙江省嘉兴市2020-2021学年高二下学期期末检测化学试题
浙江省嘉兴市2020-2021学年高二下学期期末检测化学试题(已下线)第二章 第四节 化学反应进行的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)专题2.3 化学反应的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)浙江省天台中学2021-2022学年高二上学期返校考试化学试题辽宁省葫芦岛市第八高级中学2021-2022学年高二上学期实验班第一次月考化学试题(已下线)考点24 化学反应的方向-备战2023年高考化学一轮复习考点帮(全国通用)
解题方法
2 .  和
和 是温室气体,将
是温室气体,将 和
和 转化为可利用的化学品,其能源和环境的双重意义不言自明,请回答以下问题:
转化为可利用的化学品,其能源和环境的双重意义不言自明,请回答以下问题:
(1)天然气还原 制备合成气的有关反应如下:
制备合成气的有关反应如下:
①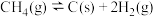
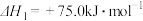
②

③
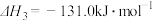
则

___________  。该反应自发进行的条件是
。该反应自发进行的条件是 ___________ (填“较高温度”或“较低温度”或“任何温度”)。
(2)H2在一定条件下还原 制备
制备 (沸点:100.7℃),能量变化如图所示。
(沸点:100.7℃),能量变化如图所示。

已知: ,
, 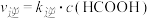 (
(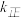 、
、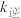 为速率常数,只与温度有关)。
为速率常数,只与温度有关)。
在1L恒容密闭容器中充入一定量 、
、 ,发生如下反应:
,发生如下反应:
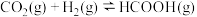

某温度下反应达到平衡, 的平衡转化率为80%,
的平衡转化率为80%,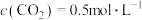 。
。
①达到平衡后,仅升高温度,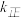 增大的倍数
增大的倍数 ___________ (填“大于”“小于”或“等于”)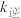 增大的倍数。
增大的倍数。
②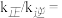
___________ 。
③使用高效催化剂,下列活化能变化合理的是___________ (填字母)。
 和
和 是温室气体,将
是温室气体,将 和
和 转化为可利用的化学品,其能源和环境的双重意义不言自明,请回答以下问题:
转化为可利用的化学品,其能源和环境的双重意义不言自明,请回答以下问题:(1)天然气还原
 制备合成气的有关反应如下:
制备合成气的有关反应如下:①
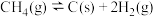
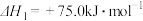
②


③

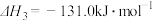
则


 。该反应自发进行的条件是
。该反应自发进行的条件是 (2)H2在一定条件下还原
 制备
制备 (沸点:100.7℃),能量变化如图所示。
(沸点:100.7℃),能量变化如图所示。
已知:
 ,
, 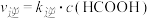 (
(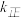 、
、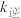 为速率常数,只与温度有关)。
为速率常数,只与温度有关)。在1L恒容密闭容器中充入一定量
 、
、 ,发生如下反应:
,发生如下反应: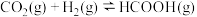

某温度下反应达到平衡,
 的平衡转化率为80%,
的平衡转化率为80%,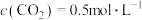 。
。①达到平衡后,仅升高温度,
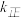 增大的倍数
增大的倍数 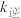 增大的倍数。
增大的倍数。②
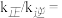
③使用高效催化剂,下列活化能变化合理的是
| 选项 | A | B | C | D |
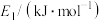 | 384 | 404 | 344 | 374 |
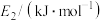 | 359 | 389 | 329 | 399 |
您最近一年使用:0次
名校
3 . 氯化硫酰( )常用作氧化剂,它是一种无色液体,熔点:
)常用作氧化剂,它是一种无色液体,熔点: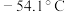 ,沸点:69.1℃,可用干燥的
,沸点:69.1℃,可用干燥的 和
和 在活性炭作催化剂的条件下制取:
在活性炭作催化剂的条件下制取: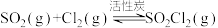
 。下列有关
。下列有关 制取的说法正确的是
制取的说法正确的是
 )常用作氧化剂,它是一种无色液体,熔点:
)常用作氧化剂,它是一种无色液体,熔点: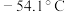 ,沸点:69.1℃,可用干燥的
,沸点:69.1℃,可用干燥的 和
和 在活性炭作催化剂的条件下制取:
在活性炭作催化剂的条件下制取: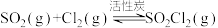
 。下列有关
。下列有关 制取的说法正确的是
制取的说法正确的是| A.该反应在高温下能自发进行 |
| B.使用活性炭作催化剂能缩短该反应达平衡的时间 |
C.反应中每消耗22.4L 转移的电子数目约为 转移的电子数目约为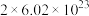 |
D.使 液化从平衡体系中分离,能加快正反应速率,增大 液化从平衡体系中分离,能加快正反应速率,增大 转化率 转化率 |
您最近一年使用:0次
2021-06-27更新
|
507次组卷
|
5卷引用:江苏省无锡市2020-2021学年期高二下学期期终教学质量抽测建议卷化学试题
江苏省无锡市2020-2021学年期高二下学期期终教学质量抽测建议卷化学试题(已下线)专题2.4 化学反应的调控(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)福建省龙岩市武平县第一中学2021-2022学年高二上学期9月月考化学试题广东省珠海市第二中学2022-2023学年高二上学期10月月考化学试题江苏省马坝高级中学2022-2023学年高三上学期9月份质量检测化学试题
4 . 工业上可溶性的钡盐常用重晶石(BaSO4)与焦炭在高温下还原得到,按物质的量之比1:3投料。主要发生如下反应:
①BaSO4(s)+2C(s) BaS(s)+2CO2(g)ΔH1=-98kJ•mol-1
BaS(s)+2CO2(g)ΔH1=-98kJ•mol-1
②BaSO4(s)+4C(s) BaS(s)+4CO(g)ΔH2=+571.2kJ•mol-1
BaS(s)+4CO(g)ΔH2=+571.2kJ•mol-1
③BaSO4(s)+4CO(g) BaS(s)+4CO2(g)ΔH3=-118.8kJ•mol-1
BaS(s)+4CO2(g)ΔH3=-118.8kJ•mol-1
④CO2(g)+C(s) 2CO(g)ΔH4
2CO(g)ΔH4
按要求回答下列问题:
(1)ΔH4=___ kJ•mol-1。
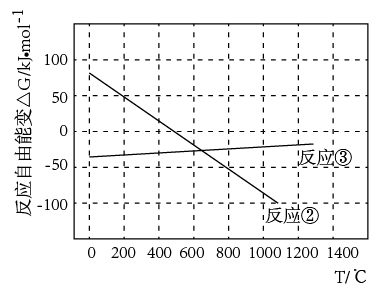
(2)已知体系自由能变ΔG=ΔH-TΔS,ΔG<0时反应自发进行。由下图可知工业上用焦炭还原重晶石发生反应②,至少需控制反应温度___ ℃以上。
(3)将重晶石与焦炭(固体均足量)在恒压密闭容器中控制1000℃温度下发生反应,下列能证明反应③达到平衡状态的是___ 。
A.气体的压强不变
B.CO2的体积分数保持不变
C.v(CO):v(CO2)=1:1
D.容器内气体密度不变
(4)T℃温度下,碳热还原硫酸钡反应达到平衡时,混合气体的总压强为P,其中CO的物质的量分数为α,则反应③的平衡常数Kp=__ 。[说明:对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)可表示平衡常数,记作Kp,如p(B)=p•x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数]。
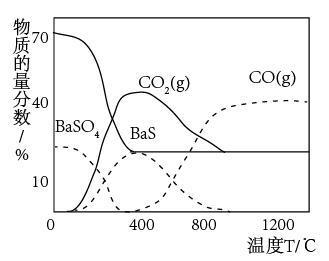
(5)常压下,不同反应温度下碳热还原硫酸钡反应体系各物质的组成如图所示。400℃以,反应①可以看成反应②和反应③连续进行的结果,由图可判断在400℃以下时反应②的速率___ 反应③(填“>”、“<”或“=”),理由是__ 。
①BaSO4(s)+2C(s)
 BaS(s)+2CO2(g)ΔH1=-98kJ•mol-1
BaS(s)+2CO2(g)ΔH1=-98kJ•mol-1②BaSO4(s)+4C(s)
 BaS(s)+4CO(g)ΔH2=+571.2kJ•mol-1
BaS(s)+4CO(g)ΔH2=+571.2kJ•mol-1③BaSO4(s)+4CO(g)
 BaS(s)+4CO2(g)ΔH3=-118.8kJ•mol-1
BaS(s)+4CO2(g)ΔH3=-118.8kJ•mol-1④CO2(g)+C(s)
 2CO(g)ΔH4
2CO(g)ΔH4
按要求回答下列问题:
(1)ΔH4=
(2)已知体系自由能变ΔG=ΔH-TΔS,ΔG<0时反应自发进行。由下图可知工业上用焦炭还原重晶石发生反应②,至少需控制反应温度
(3)将重晶石与焦炭(固体均足量)在恒压密闭容器中控制1000℃温度下发生反应,下列能证明反应③达到平衡状态的是
A.气体的压强不变
B.CO2的体积分数保持不变
C.v(CO):v(CO2)=1:1
D.容器内气体密度不变
(4)T℃温度下,碳热还原硫酸钡反应达到平衡时,混合气体的总压强为P,其中CO的物质的量分数为α,则反应③的平衡常数Kp=
(5)常压下,不同反应温度下碳热还原硫酸钡反应体系各物质的组成如图所示。400℃以,反应①可以看成反应②和反应③连续进行的结果,由图可判断在400℃以下时反应②的速率

您最近一年使用:0次
5 . 已知2H2O2(l)=2H2O(l)+O2(g),△H=-98kJ•mol-1。实验表明,纯的H2O2相对稳定,在54℃下恒温贮存2周后,浓度仍能保持99%,这是由于上述反应
| A.不能自发进行 | B.属于吸热反应 | C.平衡常数很小 | D.活化能较大 |
您最近一年使用:0次
2021-06-25更新
|
520次组卷
|
6卷引用: 浙江省杭州市2020-2021学年高二下学期期末教学质量检测化学试题
浙江省杭州市2020-2021学年高二下学期期末教学质量检测化学试题(已下线)第二章 第四节 化学反应进行的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)专题2.3 化学反应的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)山东省烟台市莱州第一中学2021-2022学年高二上学期10月月考化学试题(已下线)必考点04 化学反应的方向和调控-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)上海市青浦高级中学 2022-2023学年高二上学期期末线上质量检测化学试题
真题
名校
6 . 相同温度和压强下,关于物质熵的大小比较,合理的是
A. | B. |
C.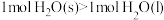 | D.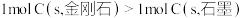 |
您最近一年使用:0次
2021-06-15更新
|
4478次组卷
|
26卷引用:第二章 第四节 化学反应进行的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)
(已下线)第二章 第四节 化学反应进行的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)2.3 化学反应的方向-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)辽宁省东北育才学校2021-2022学年高二上学期期中考试化学试题湖北省部分省级示范高中2021-2022学年高二上学期期中测试化学试题(已下线)2.3 化学反应的方向(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)浙江省吴兴高级中学高二 2021-2022学年上学期10月月考化学试题(已下线)2.1 化学反应的方向-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)安徽省亳州市第五完全中学2021-2022学年高二上学期期中考试化学试题(已下线)高中化学-高二上-9云南省玉溪市华宁县第二中学2021-2022年高二下学期开学考试化学试题第二章 化学反应速率与化学平衡 第三节 化学反应的方向(已下线)专题06 化学反应的方向及调控【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)2021年6月新高考浙江化学高考真题(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时36 化学平衡及平衡移动-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第20讲 化学平衡常数及转化率的计算(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题12.化学反应速率与化学平衡-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)2021年6月浙江高考化学试题变式题11-20(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)考点24 化学反应的方向-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第28练 化学反应的方向-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第20讲 化学平衡常数及转化率的计算(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)考点24 化学反应的方向(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第5讲 化学反应的调控
名校
解题方法
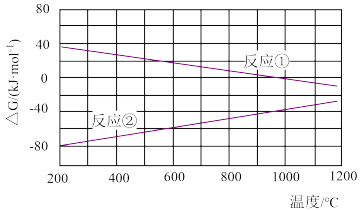
7 . 已知体系自由能变化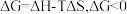 时反应能自发进行.两个氢化反应的
时反应能自发进行.两个氢化反应的 与温度的关系如图所示,下列说法正确的是
与温度的关系如图所示,下列说法正确的是
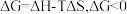 时反应能自发进行.两个氢化反应的
时反应能自发进行.两个氢化反应的 与温度的关系如图所示,下列说法正确的是
与温度的关系如图所示,下列说法正确的是
A.反应①的 |
B.反应②在 时的反应速率很快 时的反应速率很快 |
C.温度大于 时,反应①能自发进行 时,反应①能自发进行 |
D.反应②的 |
您最近一年使用:0次
2021-06-11更新
|
784次组卷
|
12卷引用:河南省天一大联考2020-2021学年高二下学期阶段性测试(三)化学试题
河南省天一大联考2020-2021学年高二下学期阶段性测试(三)化学试题(已下线)2.2.1 化学反应的方向-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)福建省龙岩市武平县第一中学2021-2022学年高二上学期9月月考化学试题(已下线)2.1 化学反应的方向-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第11讲 化学反应的方向-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)浙江省三校2022-2023学年高二上学期10月联考化学试题作业(十) 化学反应的方向第二章 第三节 化学反应的方向(已下线)考点24 化学反应的方向-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第28练 化学反应的方向-2023年高考化学一轮复习小题多维练(全国通用)(已下线)化学预测卷(八)-预测卷(浙江专版)(已下线)考点24 化学反应的方向(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
8 . 对于反应 ,下列有关说法不正确的是
,下列有关说法不正确的是
 ,下列有关说法不正确的是
,下列有关说法不正确的是A.该反应是熵增大反应(即 ) ) | B.该反应在高温下可能自发进行 |
C.增加 ,该反应平衡向右移动 ,该反应平衡向右移动 | D.升高温度,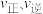 均增大,平衡向右移动 均增大,平衡向右移动 |
您最近一年使用:0次
2021-06-11更新
|
1233次组卷
|
10卷引用:河南省郑州市郊县2020-2021学年高二下学期期末考试化学试题
河南省郑州市郊县2020-2021学年高二下学期期末考试化学试题(已下线)第二章 第四节 化学反应进行的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)第2章 化学反应速率与化学平衡(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)辽宁省辽东南协作体2021-2022学年高二上学期第一次月考化学试题(已下线)期中测试卷02-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版)广东省深圳市观澜中学2022-2023学年高二上学期期中考试化学试题上海市行知中学2022-2023学年高二下学期3月月考化学试题湖北省宜昌市长阳土家族自治县第一高级中学2023-2024学年高二上学期9月月考化学试题甘肃省武威市天祝藏族自治县第一中学2022-2023学年高二下学期开学考试化学试题吉林省东北师范大学连山实验高中2023-2024学年高二上学期第一次月考化学试题
9 . 氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。
方法I:氨热分解法制氢气
相关化学键的键能数据
一定温度下,利用催化剂将 分解为
分解为 和
和 。回答下列问题:
。回答下列问题:
(1)反应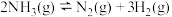

_______  ;
;
(2)已知该反应的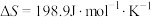 ,在下列哪些温度下反应能自发进行?
,在下列哪些温度下反应能自发进行?_______ (填标号)
A.25℃ B.125℃ C.225℃ D.325℃
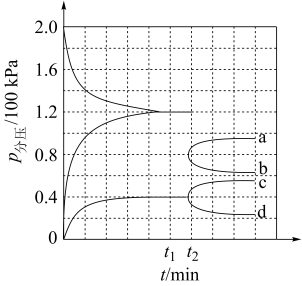
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将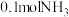 通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
①若保持容器体积不变, 时反应达到平衡,用
时反应达到平衡,用 的浓度变化表示
的浓度变化表示 时间内的反应速率
时间内的反应速率
_______  (用含
(用含 的代数式表示)
的代数式表示)
② 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是_______ (用图中a、b、c、d表示),理由是_______ ;
③在该温度下,反应的标准平衡常数
_______ 。(已知:分压=总压×该组分物质的量分数,对于反应 ,
, ,其中
,其中 ,
,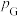 、
、 、
、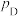 、
、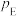 为各组分的平衡分压)。
为各组分的平衡分压)。
方法Ⅱ:氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示。
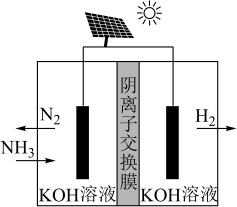
(4)电解过程中 的移动方向为
的移动方向为_______ (填“从左往右”或“从右往左”);
(5)阳极的电极反应式为_______ 。
方法I:氨热分解法制氢气
相关化学键的键能数据
| 化学键 |  |  |  |
键能 | 946 | 436.0 | 390.8 |
 分解为
分解为 和
和 。回答下列问题:
。回答下列问题:(1)反应
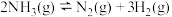

 ;
;(2)已知该反应的
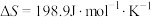 ,在下列哪些温度下反应能自发进行?
,在下列哪些温度下反应能自发进行?A.25℃ B.125℃ C.225℃ D.325℃
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将
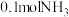 通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
①若保持容器体积不变,
 时反应达到平衡,用
时反应达到平衡,用 的浓度变化表示
的浓度变化表示 时间内的反应速率
时间内的反应速率
 (用含
(用含 的代数式表示)
的代数式表示)②
 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是③在该温度下,反应的标准平衡常数

 ,
, ,其中
,其中 ,
,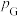 、
、 、
、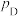 、
、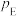 为各组分的平衡分压)。
为各组分的平衡分压)。方法Ⅱ:氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示。

(4)电解过程中
 的移动方向为
的移动方向为(5)阳极的电极反应式为
您最近一年使用:0次
2021-06-09更新
|
10832次组卷
|
14卷引用:湖北省鄂西南三校2023-2024学年高二下学期3月联考化学试题
湖北省鄂西南三校2023-2024学年高二下学期3月联考化学试题2021年新高考湖南化学高考真题(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(浙江专用)2021年湖南省高考化学试卷变式题11-19(已下线)专题12 化学反应原理综合题—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)回归教材重难点09 化学反应原理综合-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)押新高考卷17题 化学反应原理综合题-备战2022年高考化学临考题号押题(新高考通版)天津市第一中学2022届高三下学期5月月考化学试题(已下线)专题15 化学反应原理综合题-三年(2020-2022)高考真题分项汇编(已下线)考点23 化学平衡常数-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题17 原理综合题(已下线)专题17 原理综合题(已下线)专题15 化学反应原理综合题-2023年高考化学真题题源解密(全国通用)
解题方法
10 . CO2(g)+3H2(g)  CH3OH(g)+H2O(g)△H=﹣890 kJ•mol-1可用于甲醇的制备。下列有关该反应的说法正确的是
CH3OH(g)+H2O(g)△H=﹣890 kJ•mol-1可用于甲醇的制备。下列有关该反应的说法正确的是
 CH3OH(g)+H2O(g)△H=﹣890 kJ•mol-1可用于甲醇的制备。下列有关该反应的说法正确的是
CH3OH(g)+H2O(g)△H=﹣890 kJ•mol-1可用于甲醇的制备。下列有关该反应的说法正确的是| A.上述反应能在任何温度下自发进行 |
B.该反应的平衡常数K=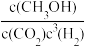 |
| C.该反应每生成1mol甲醇需消耗3×22.4 LH2 |
| D.用E表示键能,该反应△H=2E(C=O)+3E(H﹣H)﹣3E(C﹣H)﹣E(C﹣O)﹣3E(O﹣H) |
您最近一年使用:0次



