解题方法
1 . 下列说法不正确的是
| A.ΔH<0、ΔS>0的反应在任何温度下都能自发进行 |
| B.NH4HCO3(s) = NH3(g)+H2O(g)+CO2(g) ΔH=+185.57 kJ/mol 能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
| C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 |
| D.自发反应也可能需要加热才能进行 |
您最近一年使用:0次
2024-03-15更新
|
44次组卷
|
2卷引用:陕西省汉中市城固县城固县第二中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
2 . 下列基于事实做出的分析不正确 的是
A. 与Al发生铝热反应的条件为高温,说明该反应需吸收能量 与Al发生铝热反应的条件为高温,说明该反应需吸收能量 |
B.反应 在高温时才能自发进行,说明该反应熵变 在高温时才能自发进行,说明该反应熵变 |
| C.碳酸氢钠稀溶液与稀盐酸混合后溶液温度降低,说明该反应需吸收能量 |
| D.某浓度碳酸钠溶液升温时pH减小,说明水的电离程度比碳酸根离子的水解程度增大得更多 |
您最近一年使用:0次
2024-03-12更新
|
63次组卷
|
2卷引用:浙江省S9联盟2023-2024学年高二下学期4月期中考试化学试题
3 . Si是良好的半导体材料,在科技材料、电子产品等诸多领域都有重要的应用,制备高纯硅时发生主要反应有SiO2(s )+ 2C(s) = Si(s) +2CO(g) ΔH >0 ,关于该反应的自发进行描述正确 的是
| A.高温自发 | B.低温自发 | C.任意温度自发 | D.任意温度都不自发 |
您最近一年使用:0次
解题方法
4 . 反应进行的方向是化学反应原理的三个重要组成部分之一,下列说法中正确的是
A. , , 的反应一定可以自发进行 的反应一定可以自发进行 |
B. 、 、 与人体血液中的血红蛋白 与人体血液中的血红蛋白 建立平衡: 建立平衡: , , 中毒时应将中毒患者转移至高压氧仓吸氧 中毒时应将中毒患者转移至高压氧仓吸氧 |
C.可逆反应正向进行时,正反应具有自发性, 一定小于零 一定小于零 |
| D.根据反应的自发性可以预测该反应发生的快慢 |
您最近一年使用:0次
解题方法
5 . 甲烷是重要的气体燃料和化工原料,由 制取合成气(CO、
制取合成气(CO、 )的反应原理为
)的反应原理为
 。回答下列问题:
。回答下列问题:
(1)①当体系温度等于T K时 ,温度大于T时
,温度大于T时
___________ (填“>”“<”或“=”)0。
②在一定温度下,恒容密闭容器中发生上述反应,下列状态表示反应一定达到平衡状态的有___________ (填标号)。
A.
B.气体压强不再变化
C.单位时间每消耗1 mol ,同时产生3 mol
,同时产生3 mol 
D. 与
与 的物质的量之比为1∶3
的物质的量之比为1∶3
(2)在体积为1L的恒容密闭容器中通入1 mol 和1 mol
和1 mol  ,在不同条件下发生反应
,在不同条件下发生反应 ,测得平衡时
,测得平衡时 的体积分数与温度的关系如图所示。
的体积分数与温度的关系如图所示。
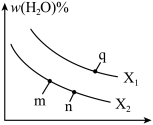
①该反应的平衡常数表达式
___________ 。
②若q点对应的纵坐标为30,此时甲烷的转化率为___________ ,该条件下平衡常数
___________ (保留两位有效数字)。
 制取合成气(CO、
制取合成气(CO、 )的反应原理为
)的反应原理为
 。回答下列问题:
。回答下列问题:(1)①当体系温度等于T K时
 ,温度大于T时
,温度大于T时
②在一定温度下,恒容密闭容器中发生上述反应,下列状态表示反应一定达到平衡状态的有
A.

B.气体压强不再变化
C.单位时间每消耗1 mol
 ,同时产生3 mol
,同时产生3 mol 
D.
 与
与 的物质的量之比为1∶3
的物质的量之比为1∶3(2)在体积为1L的恒容密闭容器中通入1 mol
 和1 mol
和1 mol  ,在不同条件下发生反应
,在不同条件下发生反应 ,测得平衡时
,测得平衡时 的体积分数与温度的关系如图所示。
的体积分数与温度的关系如图所示。
①该反应的平衡常数表达式

②若q点对应的纵坐标为30,此时甲烷的转化率为

您最近一年使用:0次
2019高二上·全国·专题练习
名校
解题方法
6 . 下列说法正确的是
A.反应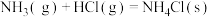 在室温下可自发进行,则该反应的 在室温下可自发进行,则该反应的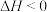 |
B. 在常温下能自发进行,则该反应的 在常温下能自发进行,则该反应的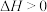 |
C. 室温下不能自发进行,则该反应的 室温下不能自发进行,则该反应的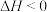 |
D.常温下,反应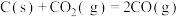 不能自发进行,则该反应的 不能自发进行,则该反应的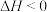 |
您最近一年使用:0次
2024-03-04更新
|
152次组卷
|
18卷引用:内蒙古翁牛特旗乌丹第二中学2019-2020学年高二上学期期中考试化学试题
内蒙古翁牛特旗乌丹第二中学2019-2020学年高二上学期期中考试化学试题浙江省宁波市北仑中学2023-2024学年高二上学期 期中化学试卷新疆实验中学2023-2024学年高二上学期期中考试化学试题(已下线)2019年9月29日《每日一题》选修4—— 每周一测2019年10月24日《每日一题》2019-2020学年高二化学人教选修4——化学反应方向的判断江西省新余市分宜中学2019-2020学年高二上学期第一次段考化学试题(已下线)【新东方】 2020-2安徽省桐城市天城中学2019-2020学年高二上学期段考化学试题(已下线)第02章 化学反应速率与化学平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)山东省临沂市沂水一中2020-2021学年高二9月月考化学试题河北省安平中学2020-2021学年高二上学期第一次月考化学试题黑龙江省龙东南六校2020-2021学年高二上学期期末联考化学试题(已下线)2.3 化学反应的方向-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)云南省玉溪师范学院附属中学2021-2022学年高二上学期期末考试化学试题(已下线)2.1 化学反应的方向-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)云南省昆明市第十中学2021-2022学年高二下学期3月月考化学试题浙江省宁波市北仑中学2023-2024学年高二上学期期初考试化学试题浙江省杭州师范大学附属中学2023-2024学年高二上学期期末考试化学试题
7 . 2022年6月5日,我国长征二号运载火箭搭载神舟十四号载人飞船顺利升空,其动力燃料是偏二甲肼,火箭发射时只要将其和四氧化二氮在发动机燃烧室混合即可,核心反应为: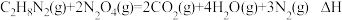 。对于该反应下列说法不正确的是
。对于该反应下列说法不正确的是
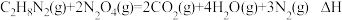 。对于该反应下列说法不正确的是
。对于该反应下列说法不正确的是A.用 表示键能之和,该反应 表示键能之和,该反应 (反应物) (反应物) (生成物) (生成物) |
B.由该热化学反应方程式可知,偏二甲肼的燃烧热为 |
| C.该反应物的总能量大于生成物总能量 |
D.该反应的 , , ,反应在任意条件下均能自发进行 ,反应在任意条件下均能自发进行 |
您最近一年使用:0次
名校
解题方法
8 . 下列化学理论、化工生产或实验事实引出的结论不正确的是
| 选项 | 事实 | 结论 |
| A | 化学反应的历程一般为:普通反应物分子 活化分子 活化分子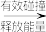 产物分子 产物分子 | 普通分子吸收能量转化为活化分子,活化分子间有适当的取向时,才能发生有效碰撞,生成产物分子 |
| B | 把Ba(OH)2•8H2O晶体与氯化铵晶体放入烧杯,用玻璃棒快速搅拌,烧杯变凉 | 反应物的总能量低于生成物的总能量 |
| C | 2NO(g)+2CO(g)=N2(g)+2CO2(g)反应△S<0,但是此反应可以自发进行 | 要判断反应自发进行的方向,必须综合考虑反应体系的焓变和熵变 |
| D | 在2L的密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g),把密闭容器的容积改为1L,重新发生该反应 2NH3(g),把密闭容器的容积改为1L,重新发生该反应 | 化学反应速率减慢 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-29更新
|
64次组卷
|
2卷引用:湖北省武汉市新洲区第一中学2024届高二上学期11月阶段测试化学试题
名校
9 . 在恒容、密闭的容器中放置一定量的NO和足量的C,发生反应: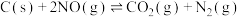 ,NO的平衡浓度与温度的关系如图所示。下列说法正确的是
,NO的平衡浓度与温度的关系如图所示。下列说法正确的是
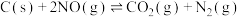 ,NO的平衡浓度与温度的关系如图所示。下列说法正确的是
,NO的平衡浓度与温度的关系如图所示。下列说法正确的是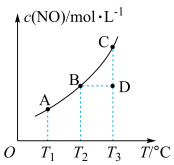
| A.增大压强或升高温度,NO的转化率均增大 |
B.在 时,若反应体系处于状态D,则 时,若反应体系处于状态D,则 |
C.状态A、B、C、D的平衡常数: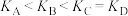 |
D.若该反应在任意温度下均能自发进行,则 |
您最近一年使用:0次
2024-02-23更新
|
115次组卷
|
3卷引用:辽宁省本溪市第一中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
10 . 工业燃烧煤、石油等化石燃料释放出大量氮氧化物、一氧化碳、二氧化碳等气体,严重污染空气。通过对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
(1)甲醇不仅是重要的化工原料,而且还是性能优良的能源和车用燃料。甲醇和水蒸气制取 的反应如下:
的反应如下:
反应Ⅰ: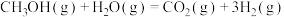
 平衡常数为
平衡常数为
反应Ⅱ:
 平衡常数为
平衡常数为
反应 的
的
______ (用含 的式子表示),平衡常数
的式子表示),平衡常数
______ (用含 的式子表示)。
的式子表示)。
(2)二氧化碳可以合成甲醇,一氧化碳也可以合成甲醇,用CO和 合成
合成 的化学方程式为
的化学方程式为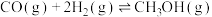
 ,向2L恒容密闭容器中加入2mol CO和4mol
,向2L恒容密闭容器中加入2mol CO和4mol  ,在适当的催化剂作用下,此反应能自发进行。
,在适当的催化剂作用下,此反应能自发进行。
①该反应
______ 0(填“>”、“<”或“=”)
②下列叙述能说明此反应达到平衡状态的是______ 。(填字母)
A.混合气体的平均相对分子质量保持不变 B.CO的转化率和 的转化率相等
的转化率相等
C.1mol CO生成的同时有2mol H-H键断裂 D.混合气体的密度保持不变
③按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示,请分析:
温度:
______  ;正反应速率:
;正反应速率: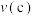
______ 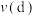 (填“>”、“<”或“=”)
(填“>”、“<”或“=”) kPa的容器中加入2mol CO和4mol
kPa的容器中加入2mol CO和4mol  ,发生反应,达到平衡。甲醇在平衡体系中所占的物质的量分数为0.25,则CO的平衡转化率
,发生反应,达到平衡。甲醇在平衡体系中所占的物质的量分数为0.25,则CO的平衡转化率
______ ,反应平衡常数表示为
______ ( 就是用各物质的分压代替各物质的平衡浓度来表示化学平衡常数,分压=总压×物质的量分数,用含
就是用各物质的分压代替各物质的平衡浓度来表示化学平衡常数,分压=总压×物质的量分数,用含 的式子表示)
的式子表示)
(1)甲醇不仅是重要的化工原料,而且还是性能优良的能源和车用燃料。甲醇和水蒸气制取
 的反应如下:
的反应如下:反应Ⅰ:
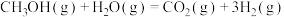
 平衡常数为
平衡常数为
反应Ⅱ:

 平衡常数为
平衡常数为
反应
 的
的
 的式子表示),平衡常数
的式子表示),平衡常数
 的式子表示)。
的式子表示)。(2)二氧化碳可以合成甲醇,一氧化碳也可以合成甲醇,用CO和
 合成
合成 的化学方程式为
的化学方程式为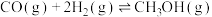
 ,向2L恒容密闭容器中加入2mol CO和4mol
,向2L恒容密闭容器中加入2mol CO和4mol  ,在适当的催化剂作用下,此反应能自发进行。
,在适当的催化剂作用下,此反应能自发进行。①该反应

②下列叙述能说明此反应达到平衡状态的是
A.混合气体的平均相对分子质量保持不变 B.CO的转化率和
 的转化率相等
的转化率相等C.1mol CO生成的同时有2mol H-H键断裂 D.混合气体的密度保持不变
③按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示,请分析:
温度:

 ;正反应速率:
;正反应速率: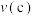
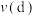 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)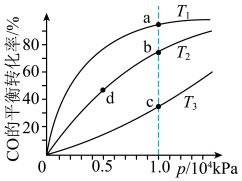
 kPa的容器中加入2mol CO和4mol
kPa的容器中加入2mol CO和4mol  ,发生反应,达到平衡。甲醇在平衡体系中所占的物质的量分数为0.25,则CO的平衡转化率
,发生反应,达到平衡。甲醇在平衡体系中所占的物质的量分数为0.25,则CO的平衡转化率

 就是用各物质的分压代替各物质的平衡浓度来表示化学平衡常数,分压=总压×物质的量分数,用含
就是用各物质的分压代替各物质的平衡浓度来表示化学平衡常数,分压=总压×物质的量分数,用含 的式子表示)
的式子表示)
您最近一年使用:0次
2024-02-21更新
|
69次组卷
|
2卷引用:浙江省宁波三锋教研联盟2023-2024学年高二上学期期中联考化学试题



