名校
1 . 下列说法不正确的是
| A.冰在室温下自动熔化成水,这是熵增的过程 |
| B.当ΔH<0,ΔS>0时,反应能自发进行 |
| C.2NO(g)+ 2CO(g) = N2(g)+ 2CO2(g)在常温下能自发进行,则该反应的ΔH>0 |
| D.反应NH3(g) + HCl(g) = NH4Cl(s)在室温下可自发进行,则该反应的ΔH<0 |
您最近一年使用:0次
名校
2 . 已知分解1 mol H2O2放出热量98 kJ。在含少量I-的溶液中,H2O2分解的机理为:
H2O2+I-→H2O+IO- 慢
H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法正确的是
H2O2+I-→H2O+IO- 慢
H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法正确的是
| A.是自发反应 | B.IO-也是该反应的催化剂 |
| C.整个反应的快慢由第一步决定 | D.反应活化能等于98 kJ·mol-1 |
您最近一年使用:0次
名校
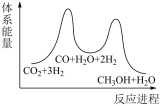
3 . 二氧化碳加氢制甲醇的总反应可表示为: ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:
①
②
体系能量变化如图所示,下列有关说法错误的是
 ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:①

②

体系能量变化如图所示,下列有关说法错误的是

| A.ΔH1>ΔH2 |
| B.步骤②反应ΔS<0 |
| C.二氧化碳加氢制甲醇的总反应决速步骤取决于步骤① |
D.二氧化碳加氢制甲醇的总反应的平衡常数K= |
您最近一年使用:0次
名校
4 . 下列说法正确的是
A.反应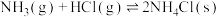 在低温下能自发进行,则该反应的 在低温下能自发进行,则该反应的 |
B.对于反应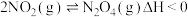 ,恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的 ,恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的 |
C.反应 ,在恒温恒压下,加入催化剂,平衡常数增大 ,在恒温恒压下,加入催化剂,平衡常数增大 |
| D.升高温度或加入催化剂能使单位体积内活化分子的百分数增大,但原因不同 |
您最近一年使用:0次
名校
5 . 研究化学反应进行的方向对于反应设计等具有重要意义,下列说法正确的是
| A.ΔH<0、ΔS>0的反应在温度低时不能自发进行 |
B.一定温度下,反应MgCl2(l) Mg(l)+Cl2(g)的ΔH>0、ΔS>0 Mg(l)+Cl2(g)的ΔH>0、ΔS>0 |
| C.反应CaCO3(s)=CaO(s)+CO2(g)在室温下不能自发进行,说明该反应的ΔH<0 |
| D.在其他外界条件不变的情况下,汽车排气管中使用催化剂,可以改变产生尾气的反应方向 |
您最近一年使用:0次
名校
解题方法
6 . 一定温度下,某密闭容器中加入足量的碳酸钙,发生反应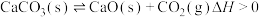 达到平衡,下列说法
达到平衡,下列说法不正确 的是
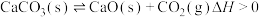 达到平衡,下列说法
达到平衡,下列说法A.将体积缩小为原来的一半,当体系再次达到平衡时, 的浓度不变 的浓度不变 |
| B.若温度升高,平衡正向移动,平衡常数增大 |
| C.该反应为吸热反应,高温能自发进行 |
| D.保持容器体积不变,充入He,平衡逆移 |
您最近一年使用:0次
名校
解题方法
7 . 下列有关说法正确的是

| A.某可逆反应若平衡朝正向移动,则平衡常数一定增大 |
B.反应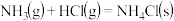 常温下可自发进行,该反应为吸热反应 常温下可自发进行,该反应为吸热反应 |
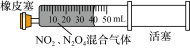
C.保持温度不变,将图中的活塞快速推至 处,新平衡时气体颜色变浅 处,新平衡时气体颜色变浅 |
D.向 溶液中加入少量水,溶液中 溶液中加入少量水,溶液中 与 与 的比值增大 的比值增大 |
您最近一年使用:0次
2024-01-07更新
|
77次组卷
|
4卷引用:福建省泉州市泉港区第一中学、厦门外国语学校石狮分校2023-2024学年高二上学期期中考试化学试题
名校
8 . 下列有关反应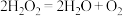 的说法中
的说法中不正确 的是
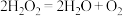 的说法中
的说法中A.生成标准状况下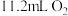 转移 转移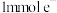 |
B. 溶液能催化该反应 溶液能催化该反应 |
C.该反应的熵变 |
| D.该反应在任意温度下均能自发进行 |
您最近一年使用:0次
名校
解题方法
9 . CO2经催化加氢可合成甲醇(CH3OH):
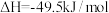 ,下列说法正确的是
,下列说法正确的是

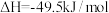 ,下列说法正确的是
,下列说法正确的是| A.该反应是放热反应,所以可以自发进行 |
| B.1molH2O在不同状态下的熵值为S(g)<S(s) |
| C.选择合适的催化剂,有可能使该反应在常温常压下以较快的速度进行 |
| D.一定条件下,若观察不到水蒸气的产生,则说明该条件下反应不能自发进行 |
您最近一年使用:0次
2024-01-07更新
|
174次组卷
|
3卷引用:四川省荥经中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
10 . 下列说法中正确的是
| A.热化学方程式未注明温度和压强时,∆H表示标准状况下的数据 |
| B.热化学方程式中各物质前的化学计量数不表示分子个数,只代表物质的量 |
| C.钙钛矿太阳能电池和锂离子电池的工作原理相同 |
| D.非自发反应在任何条件下都不能发生 |
您最近一年使用:0次



