1 . 下列说法中正确的是
| A.对有气体参加的化学反应,容器容积减小,反应物分子中活化分子的百分数增大,化学反应速率增大 |
| B.能够自发进行的反应一定都是熵增的过程 |
| C.中和等体积、等物质的量浓度的盐酸和醋酸,盐酸所需氢氧化钠的物质的量多于醋酸 |
| D.盐碱地(含NaCl、Na2CO3)不利于农作物生长,施加适量石膏可以降低土壤的碱性 |
您最近一年使用:0次
名校
解题方法
2 . 下列说法正确的是
| A.在常温下,放热反应一般能自发进行,吸热反应都不能自发进行 |
| B.NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g)△H=+185.57 kJ•mol-1,能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
| C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 |
| D.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 |
您最近一年使用:0次
解题方法
3 . 下列有关化学反应方向的描述中正确的是
| A.任何能使焓减小的过程都能自发进行 |
| B.自发反应一定是熵增加,非自发反应一定是熵不变或减少 |
| C.ΔH<0,ΔS>0,在通常状况下均可自发进行 |
| D.ΔH>0,ΔS>0,较低温度有利于反应自发进行 |
您最近一年使用:0次
解题方法
4 . 下列反应中 ,
, 的是
的是
 ,
, 的是
的是A. |
B.高温下能自发进行的反应: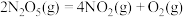 |
C.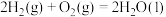 |
D.任何温度下均能自发进行的反应: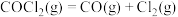 |
您最近一年使用:0次
名校
解题方法
5 . 杭州亚运会主火炬的燃料首次使用废碳再生的绿色甲醇,甲醇火炬被称为“零碳”火炬。目前,我国在相关设备及技术方面全球领先。请回答:
(1)二氧化碳催化加氢制甲醇的反应可表示为: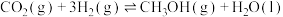 。
。
①已知: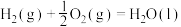
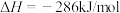


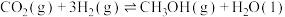
 =
=______ kJ/mol。该反应能自发进行的条件是______ 。
②在恒容条件下能加快二氧化碳催化加氢制甲醇的反应速率,并提高 转化率的措施是
转化率的措施是______ 。
③若二氧化碳催化加氢制甲醇的反应在恒温恒容的密闭容器中进行,能说明反应达到平衡状态的是______ ,(填字母)。
A.容器内压强不随时间变化 B.容器内各物质的浓度相等
C.单位时间消耗1mol ,同时生成3mol
,同时生成3mol D.混合气体的密度不再改变
D.混合气体的密度不再改变
(2)电催化法是制备甲醇的途径之一,原理如图所示。

①室温下, 溶液
溶液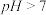 ,
, 水解的离子方程式为
水解的离子方程式为______ 。
② 电极的电极反应式为
电极的电极反应式为______ 。
③与其他有机合成相比,电有机合成的优点是______ 。
(1)二氧化碳催化加氢制甲醇的反应可表示为:
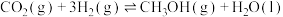 。
。①已知:
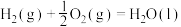
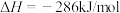


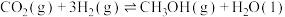
 =
=②在恒容条件下能加快二氧化碳催化加氢制甲醇的反应速率,并提高
 转化率的措施是
转化率的措施是③若二氧化碳催化加氢制甲醇的反应在恒温恒容的密闭容器中进行,能说明反应达到平衡状态的是
A.容器内压强不随时间变化 B.容器内各物质的浓度相等
C.单位时间消耗1mol
 ,同时生成3mol
,同时生成3mol D.混合气体的密度不再改变
D.混合气体的密度不再改变(2)电催化法是制备甲醇的途径之一,原理如图所示。

①室温下,
 溶液
溶液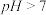 ,
, 水解的离子方程式为
水解的离子方程式为②
 电极的电极反应式为
电极的电极反应式为③与其他有机合成相比,电有机合成的优点是
您最近一年使用:0次
名校
解题方法
6 . 环戊二烯(C5H6)是一种重要的有机化工原料。
Ⅰ.环戊二烯容易二聚生成双环戊二烯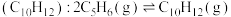 。不同温度下,溶液中环戊二烯的浓度(初始浓度为
。不同温度下,溶液中环戊二烯的浓度(初始浓度为 )与反应时间的关系如图所示。
)与反应时间的关系如图所示。
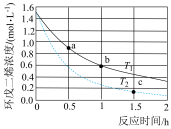
(1)反应开始至b点时,用双环戊二烯表示的平均速率为______  。
。
(2)T1______ T2(填“>”“<”或“=”)。
(3)a点的正反应速率______ b点的逆反应速率(填“>”“<”或“=”)。
Ⅱ.环戊二烯(C5H6)与环戊烯(C5H8)可发生相互转化。有如下反应:
反应ⅰ:
反应ⅱ: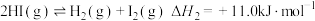
反应ⅲ: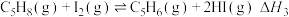
(4)反应i在______ (填“高温”或“低温”)下可自发进行。
(5)反应ⅲ的焓变
______  。
。
(6)某温度时,在1L恒容密闭容器中充入碘和环戊烯各1mol,只发生反应ⅲ,平衡时总压是起始总压的1.25倍。
①平衡时环戊烯的体积分数为______ 。
②该温度下,反应ⅲ的化学平衡常数K=______ 。
③保持温度和体积不变,向平衡体系中再充入1mol环戊二烯和1mol环戊烯,平衡______ 移动(填“向正反应方向”“向逆反应反向”或“不”)。
Ⅰ.环戊二烯容易二聚生成双环戊二烯
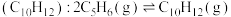 。不同温度下,溶液中环戊二烯的浓度(初始浓度为
。不同温度下,溶液中环戊二烯的浓度(初始浓度为 )与反应时间的关系如图所示。
)与反应时间的关系如图所示。
(1)反应开始至b点时,用双环戊二烯表示的平均速率为
 。
。(2)T1
(3)a点的正反应速率
Ⅱ.环戊二烯(C5H6)与环戊烯(C5H8)可发生相互转化。有如下反应:
反应ⅰ:

反应ⅱ:
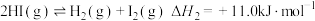
反应ⅲ:
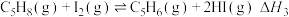
(4)反应i在
(5)反应ⅲ的焓变

 。
。(6)某温度时,在1L恒容密闭容器中充入碘和环戊烯各1mol,只发生反应ⅲ,平衡时总压是起始总压的1.25倍。
①平衡时环戊烯的体积分数为
②该温度下,反应ⅲ的化学平衡常数K=
③保持温度和体积不变,向平衡体系中再充入1mol环戊二烯和1mol环戊烯,平衡
您最近一年使用:0次
名校
解题方法
7 . 2024年2月国家工业和信息化部指出到2025年初步建立工业领域碳达峰碳中和标准体系, 有效转化是研究“碳中和”的重要方向。实现有效转化的一种常见途径是捕集
有效转化是研究“碳中和”的重要方向。实现有效转化的一种常见途径是捕集 转化为合成气(
转化为合成气( 和
和 ),再转化为烃类及含氧化合物等高附加值化学品(即费-托合成)。
),再转化为烃类及含氧化合物等高附加值化学品(即费-托合成)。
捕集 涉及下列反应:
涉及下列反应:
i.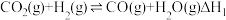
ii.
(1)有关物质能量变化如图所示,设稳定单质的焓(H)为0,则
_____________ ,利于该反应自发进行的条件是_____________ (填“高温”或“低温”)。

(2)在一定条件下,选择合适的催化剂只进行反应i: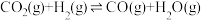 。调整
。调整 和
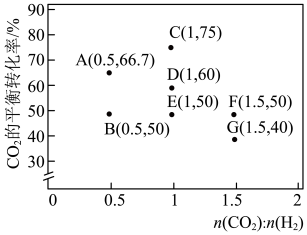
和 初始投料比,测得在一定投料比和一定温度下,该反应
初始投料比,测得在一定投料比和一定温度下,该反应 的平衡转化率如图所示。
的平衡转化率如图所示。
已知: 是以物质的量分数表示的化学平衡常数;对于反应
是以物质的量分数表示的化学平衡常数;对于反应 ,
,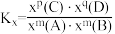 ,x为物质的量分数);反应速率
,x为物质的量分数);反应速率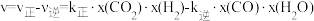 ,
, 分别为正、逆反应速率常数。
分别为正、逆反应速率常数。
①下列关于i反应说法不正确的是_____________ ;
a.催化剂参与了反应,改变了反应的活化能和
b.某温度反应达到平衡状态,升高温度,正反应速率提高的幅度更大
c.恒温恒压,混合气体密度不变可以作为反应达到平衡状态的标志
d.将 液化,及时分离,有利于提高反应物的转化率
液化,及时分离,有利于提高反应物的转化率
②B、E、F三点反应温度最高的是_____________ 点;
③计算E点所示的投料比在从起始到平衡的过程中,当 转化率达到
转化率达到 时,
时,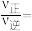
_____________ (用分数表示)。
(3)保持总压为 恒定,初始
恒定,初始 和
和 的物质的量之比
的物质的量之比 ,发生上述i、ii反应,不同温度下平衡组分物质的量分数如图。
,发生上述i、ii反应,不同温度下平衡组分物质的量分数如图。
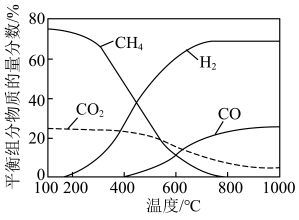
①在 以下时,
以下时, 含量高于
含量高于 的原因为
的原因为_____________ ;
②某温度下平衡体系中 和
和 的物质的量分数均为10%,此时反应i的平衡常数
的物质的量分数均为10%,此时反应i的平衡常数
_____________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 有效转化是研究“碳中和”的重要方向。实现有效转化的一种常见途径是捕集
有效转化是研究“碳中和”的重要方向。实现有效转化的一种常见途径是捕集 转化为合成气(
转化为合成气( 和
和 ),再转化为烃类及含氧化合物等高附加值化学品(即费-托合成)。
),再转化为烃类及含氧化合物等高附加值化学品(即费-托合成)。捕集
 涉及下列反应:
涉及下列反应:i.
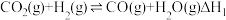
ii.

(1)有关物质能量变化如图所示,设稳定单质的焓(H)为0,则


(2)在一定条件下,选择合适的催化剂只进行反应i:
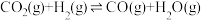 。调整
。调整 和
和 初始投料比,测得在一定投料比和一定温度下,该反应
初始投料比,测得在一定投料比和一定温度下,该反应 的平衡转化率如图所示。
的平衡转化率如图所示。
已知:
 是以物质的量分数表示的化学平衡常数;对于反应
是以物质的量分数表示的化学平衡常数;对于反应 ,
,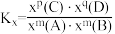 ,x为物质的量分数);反应速率
,x为物质的量分数);反应速率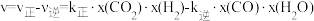 ,
, 分别为正、逆反应速率常数。
分别为正、逆反应速率常数。①下列关于i反应说法不正确的是
a.催化剂参与了反应,改变了反应的活化能和

b.某温度反应达到平衡状态,升高温度,正反应速率提高的幅度更大
c.恒温恒压,混合气体密度不变可以作为反应达到平衡状态的标志
d.将
 液化,及时分离,有利于提高反应物的转化率
液化,及时分离,有利于提高反应物的转化率②B、E、F三点反应温度最高的是
③计算E点所示的投料比在从起始到平衡的过程中,当
 转化率达到
转化率达到 时,
时,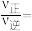
(3)保持总压为
 恒定,初始
恒定,初始 和
和 的物质的量之比
的物质的量之比 ,发生上述i、ii反应,不同温度下平衡组分物质的量分数如图。
,发生上述i、ii反应,不同温度下平衡组分物质的量分数如图。 
①在
 以下时,
以下时, 含量高于
含量高于 的原因为
的原因为②某温度下平衡体系中
 和
和 的物质的量分数均为10%,此时反应i的平衡常数
的物质的量分数均为10%,此时反应i的平衡常数
您最近一年使用:0次
名校
8 . 向 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 各
各 ,发生反应:
,发生反应: 。在不同温度下测得
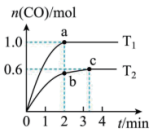
。在不同温度下测得 随时间变化的曲线如图所示。下列说法正确的是
随时间变化的曲线如图所示。下列说法正确的是
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 各
各 ,发生反应:
,发生反应: 。在不同温度下测得
。在不同温度下测得 随时间变化的曲线如图所示。下列说法正确的是
随时间变化的曲线如图所示。下列说法正确的是
| A.该反应在任意温度下均可自发进行 |
B. 温度下, 温度下, 的平衡转化率是30% 的平衡转化率是30% |
C. 、 、 两点平衡常数: 两点平衡常数: |
D. 温度下,0到 温度下,0到 内,用 内,用 表示的平均反应速率为0.1mol·L-1·min-1 表示的平均反应速率为0.1mol·L-1·min-1 |
您最近一年使用:0次
名校
9 . 利用二氧化碳和氢气合成甲醇可以有效降低二氧化碳的排放量。
已知:①
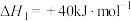

②


回答下面问题:
(1)利用二氧化碳和氢气合成甲醇的反应为:
 。已知该反应能够自发进行,则
。已知该反应能够自发进行,则
_______ (填“<”“>”或“=”)0,
_______ 0。该反应的平衡常数
_______ (用 和
和 表示),随着温度逐渐升高,
表示),随着温度逐渐升高, 将
将_______ (填“增大”或“减小”)。
(2)在某密闭容器中只发生反应②

①下面措施一定能提高CO的平衡转化率的是_______ 。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
②该反应的正活化能 (正)
(正)_______ (填“<”“>”或“=”)逆活化能 (逆)。
(逆)。
(3)在某密闭容器中通入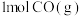 和
和 ,只发生反应②
,只发生反应②
 ,反应中CO的平衡转化率随温度和压强的变化如下:
,反应中CO的平衡转化率随温度和压强的变化如下:
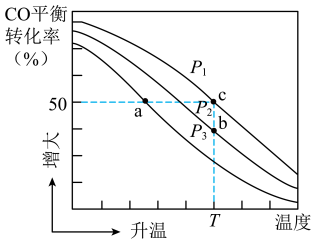
①随温度逐渐升高CO平衡转化率降低的原因是_______ 。
②压强 、
、 、
、 由大到小的顺序是
由大到小的顺序是_______ 。
③a、b、c三点对应的压强平衡常数分别为 、
、 、
、 ,由大到小的顺序是
,由大到小的顺序是_______ 。
④写出c点的压强平衡常数
_______ 。
已知:①

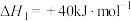

②



回答下面问题:
(1)利用二氧化碳和氢气合成甲醇的反应为:

 。已知该反应能够自发进行,则
。已知该反应能够自发进行,则


 和
和 表示),随着温度逐渐升高,
表示),随着温度逐渐升高, 将
将(2)在某密闭容器中只发生反应②


①下面措施一定能提高CO的平衡转化率的是
A.高温高压 B.高温低压 C.低温高压 D.低温低压
②该反应的正活化能
 (正)
(正) (逆)。
(逆)。(3)在某密闭容器中通入
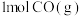 和
和 ,只发生反应②
,只发生反应②
 ,反应中CO的平衡转化率随温度和压强的变化如下:
,反应中CO的平衡转化率随温度和压强的变化如下:
①随温度逐渐升高CO平衡转化率降低的原因是
②压强
 、
、 、
、 由大到小的顺序是
由大到小的顺序是③a、b、c三点对应的压强平衡常数分别为
 、
、 、
、 ,由大到小的顺序是
,由大到小的顺序是④写出c点的压强平衡常数

您最近一年使用:0次
10 . 为了实现“碳中和”,研发 的利用技术成为热点。
的利用技术成为热点。
反应I:
反应Ⅱ:
请回答:
(1)反应I能够自发进行的条件是__________ 。
(2)向 的恒容密闭容器中充入
的恒容密闭容器中充入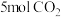 和
和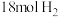 (起始压强为
(起始压强为 ),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量
),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量 与温度
与温度 的关系如下图所示。
的关系如下图所示。
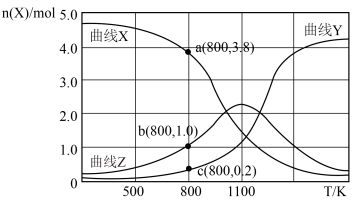
①写出曲线Y表示的含碳元素物质的化学式__________ 。
② 时,反应Ⅱ的平衡常数
时,反应Ⅱ的平衡常数
__________ [对于气相反应,用某组分 的平衡压强
的平衡压强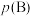 代替物质的量浓度
代替物质的量浓度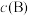 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如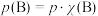 ,
, 为平衡总压强,
为平衡总压强,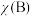 为平衡系统中
为平衡系统中 的物质的量分数]。
的物质的量分数]。
(3)可用 与
与 催化加氢制乙醇,反应原理为:
催化加氢制乙醇,反应原理为: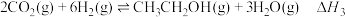 。经实验测定在不同投料比
。经实验测定在不同投料比 、
、 、
、 时
时 的平衡转化率与温度的关系如图所示
的平衡转化率与温度的关系如图所示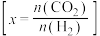 :
:

①上述反应的活化能 (正)
(正)__________  (逆)(填“
(逆)(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
② 、
、 、
、 由大到小的顺序是
由大到小的顺序是__________ 。
③从平衡角度分析,随温度升高,不同投料比时 的平衡转化率趋于相近的原因
的平衡转化率趋于相近的原因__________ 。
(4)科学家提出由 制取
制取 的太阳能工艺如图。已知“重整系统”发生的反应中
的太阳能工艺如图。已知“重整系统”发生的反应中 ,则
,则 的化学式为
的化学式为__________ 。

(5)水系可逆 电池可吸收利用
电池可吸收利用 ,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的
,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的 解离成
解离成 和
和 ,工作原理如图所示:
,工作原理如图所示:

①放电时复合膜中向 极移动的离子是
极移动的离子是__________ 。
②充电时多孔 纳米片电极的电极反应式为
纳米片电极的电极反应式为__________ 。
 的利用技术成为热点。
的利用技术成为热点。反应I:

反应Ⅱ:

请回答:
(1)反应I能够自发进行的条件是
(2)向
 的恒容密闭容器中充入
的恒容密闭容器中充入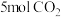 和
和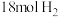 (起始压强为
(起始压强为 ),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量
),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量 与温度
与温度 的关系如下图所示。
的关系如下图所示。
①写出曲线Y表示的含碳元素物质的化学式
②
 时,反应Ⅱ的平衡常数
时,反应Ⅱ的平衡常数
 的平衡压强
的平衡压强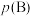 代替物质的量浓度
代替物质的量浓度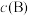 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如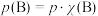 ,
, 为平衡总压强,
为平衡总压强,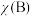 为平衡系统中
为平衡系统中 的物质的量分数]。
的物质的量分数]。(3)可用
 与
与 催化加氢制乙醇,反应原理为:
催化加氢制乙醇,反应原理为: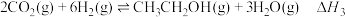 。经实验测定在不同投料比
。经实验测定在不同投料比 、
、 、
、 时
时 的平衡转化率与温度的关系如图所示
的平衡转化率与温度的关系如图所示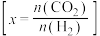 :
:
①上述反应的活化能
 (正)
(正) (逆)(填“
(逆)(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。②
 、
、 、
、 由大到小的顺序是
由大到小的顺序是③从平衡角度分析,随温度升高,不同投料比时
 的平衡转化率趋于相近的原因
的平衡转化率趋于相近的原因(4)科学家提出由
 制取
制取 的太阳能工艺如图。已知“重整系统”发生的反应中
的太阳能工艺如图。已知“重整系统”发生的反应中 ,则
,则 的化学式为
的化学式为
(5)水系可逆
 电池可吸收利用
电池可吸收利用 ,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的
,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的 解离成
解离成 和
和 ,工作原理如图所示:
,工作原理如图所示:
①放电时复合膜中向
 极移动的离子是
极移动的离子是②充电时多孔
 纳米片电极的电极反应式为
纳米片电极的电极反应式为
您最近一年使用:0次



