1 . 治理汽车尾气排放的NO、CO的办法是在汽车排气管上安装催化转化器,使NO与CO反应生成可参与大气生态循环的无毒气体,反应原理: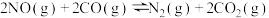 ,在298K、100kPa下,
,在298K、100kPa下,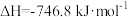 ,
,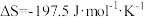 。下列说法错误的是
。下列说法错误的是
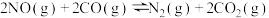 ,在298K、100kPa下,
,在298K、100kPa下,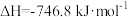 ,
,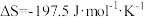 。下列说法错误的是
。下列说法错误的是| A.该反应为熵减小的反应 |
| B.该反应中反应物的总能量高于生成物的总能量 |
| C.该反应在任何条件下都不能自发进行 |
| D.其他条件不变时,加入催化剂,可以改变化学反应方向 |
您最近一年使用:0次
2022-09-01更新
|
397次组卷
|
2卷引用:湖南省长沙市湖南师范大学附属中学2022-2023学年高二上学期入学考试化学试题
解题方法
2 . 氮及其化合物与人类生产生活息息相关。
(1)氮气在雷电的作用下,生成氮的氧化物,再经复杂变化形成能供给植物营养的硝酸盐。涉及的部分反应:
I.2NO2(g)+H2O(l)=HNO3(aq)+HNO2(aq) △H1=-116.1 kJ·mol-1;
II.HNO3(aq)+2NO(g)+H2O(l)=3HNO2(aq) △H2=-75.9 kJ·mol-1;
III.3NO2(g)+H2O(l)=2HNO3(aq)+NO(g) △H3;
①△H3=____ kJ·mol-1。
②将两个充有等量NO2的A、B烧瓶,分别放入两个盛有等量的水的烧杯中,待气体颜色稳定后,若向右边的烧杯中加入5.0 g硝酸铵晶体,实验装置如图所示(略去铁架台等),则观察到B烧瓶中气体颜色____ (填“变深”、“不变”或“变浅”),其原因是_______ 。

(2)氮气是生产氮肥的主要原料。
①实验室可用氯化铵与消石灰反应制备少量NH3。
2NH4Cl(s)+Ca(OH)2(s)=CaCl2(s)+2NH3(g)+2H2O(g) △H>0,该反应在____ (填“高温”、“低温”或“任何温度”)下能自发进行,说明理由:____ 。
②已知N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1,工业合成氨通常选择30MPa左右,700K左右,以铁触媒为催化剂,分析工业合成氨时不选用更高的压强或更高的温度的可能原因:
2NH3(g) △H=-92.4 kJ·mol-1,工业合成氨通常选择30MPa左右,700K左右,以铁触媒为催化剂,分析工业合成氨时不选用更高的压强或更高的温度的可能原因:____ 。
(3)CO和NO是汽车尾气中的主要污染物,将它们转化为无害物质是重要的研究课题。
已知:在25℃时,
IV.2NO(g) N2(g)+O2(g) △H4=-180.5 kJ·mol-1 K4
N2(g)+O2(g) △H4=-180.5 kJ·mol-1 K4
V.CO(g)+ O2(g)
O2(g) CO2(g) △H5=-283.0 kJ·mol-1K5
CO2(g) △H5=-283.0 kJ·mol-1K5
①25℃时,反应2NO(g)+2CO(g) N2(g)+2CO2(g)的平衡常数K6=
N2(g)+2CO2(g)的平衡常数K6=____ (填含K4、K5的代数式)。
②在某恒温恒压的条件下,向密闭容器中充入2 mol NO和2 mol CO,仅发生反应2NO(g)+2CO(g) N2(g)+2CO2(g),此时混合气体的总体积为1 L,在t1时刻达到平衡状态,此时NO的转化率为40%,则该条件下的平衡常数K′6=
N2(g)+2CO2(g),此时混合气体的总体积为1 L,在t1时刻达到平衡状态,此时NO的转化率为40%,则该条件下的平衡常数K′6=____ (保留两位有效数字)。
(1)氮气在雷电的作用下,生成氮的氧化物,再经复杂变化形成能供给植物营养的硝酸盐。涉及的部分反应:
I.2NO2(g)+H2O(l)=HNO3(aq)+HNO2(aq) △H1=-116.1 kJ·mol-1;
II.HNO3(aq)+2NO(g)+H2O(l)=3HNO2(aq) △H2=-75.9 kJ·mol-1;
III.3NO2(g)+H2O(l)=2HNO3(aq)+NO(g) △H3;
①△H3=
②将两个充有等量NO2的A、B烧瓶,分别放入两个盛有等量的水的烧杯中,待气体颜色稳定后,若向右边的烧杯中加入5.0 g硝酸铵晶体,实验装置如图所示(略去铁架台等),则观察到B烧瓶中气体颜色

(2)氮气是生产氮肥的主要原料。
①实验室可用氯化铵与消石灰反应制备少量NH3。
2NH4Cl(s)+Ca(OH)2(s)=CaCl2(s)+2NH3(g)+2H2O(g) △H>0,该反应在
②已知N2(g)+3H2(g)
 2NH3(g) △H=-92.4 kJ·mol-1,工业合成氨通常选择30MPa左右,700K左右,以铁触媒为催化剂,分析工业合成氨时不选用更高的压强或更高的温度的可能原因:
2NH3(g) △H=-92.4 kJ·mol-1,工业合成氨通常选择30MPa左右,700K左右,以铁触媒为催化剂,分析工业合成氨时不选用更高的压强或更高的温度的可能原因:(3)CO和NO是汽车尾气中的主要污染物,将它们转化为无害物质是重要的研究课题。
已知:在25℃时,
IV.2NO(g)
 N2(g)+O2(g) △H4=-180.5 kJ·mol-1 K4
N2(g)+O2(g) △H4=-180.5 kJ·mol-1 K4V.CO(g)+
 O2(g)
O2(g) CO2(g) △H5=-283.0 kJ·mol-1K5
CO2(g) △H5=-283.0 kJ·mol-1K5①25℃时,反应2NO(g)+2CO(g)
 N2(g)+2CO2(g)的平衡常数K6=
N2(g)+2CO2(g)的平衡常数K6=②在某恒温恒压的条件下,向密闭容器中充入2 mol NO和2 mol CO,仅发生反应2NO(g)+2CO(g)
 N2(g)+2CO2(g),此时混合气体的总体积为1 L,在t1时刻达到平衡状态,此时NO的转化率为40%,则该条件下的平衡常数K′6=
N2(g)+2CO2(g),此时混合气体的总体积为1 L,在t1时刻达到平衡状态,此时NO的转化率为40%,则该条件下的平衡常数K′6=
您最近一年使用:0次
2022-08-23更新
|
186次组卷
|
3卷引用:辽宁省营口地区2022-2023学年高二上学期开学考试化学试题
名校
解题方法
3 . 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g) +H2O(g)。下图表示该反应进行过程中能量的变化。关于该反应的下列说法中正确的是


| A.ΔH>0, ΔS>0 | B.ΔH>0,ΔS<0 |
| C.ΔH<0, ΔS<0 | D.ΔH<0,ΔS>0 |
您最近一年使用:0次
2022-08-18更新
|
356次组卷
|
22卷引用:黑龙江省哈尔滨师范大学附属中学2021-2022学年高二上学期开学考试化学试题
黑龙江省哈尔滨师范大学附属中学2021-2022学年高二上学期开学考试化学试题河北省石家庄市第一中学2021-2022学年高二上学期开学考试化学试题安徽省六安市城南中学2020-2021学年高二上学期期中考试化学试题河南省长垣市第十中学2020-2021学年高二上学期第二次月考化学试题湖北省咸宁市通城二中2020-2021学年高二上学期10月月考化学试题内蒙古集宁新世纪中学2020-2021学年高二上学期期中考试化学试题(已下线)第二单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)山东省烟台市招远市第二中学2021-2022学年高二10月月考化学试题安徽省蚌埠第三中学2021-2022学年高二上学期10月教学质量检测化学试题辽宁省朝阳育英高考补习学校2021-2022学年高二10月月考化学试题黑龙江省哈尔滨市第六中学2021-2022学年高二上学期第一次月考化学试题河南省范县第一中学2021-2022学年高二上学期第二次月考检测化学试题贵州省凯里市第一中学2021-2022学年高二上学期期中考试化学(理科)试题(已下线)必考点04 化学反应的方向和调控-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)(已下线)章末培优2 专题2 化学反应速率与化学平衡-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)贵州省毕节市金沙县第一中学2021-2022学年高二上学期期中考试化学试题黑龙江省齐齐哈尔市恒昌中学校2021-2022学年高二上学期期中考试化学试题黑龙江省牡丹江市第三高级中学2022-2023学年高二上学期第一次月考化学试题福建泉州现代中学2021-2022学年高二上学期期中考试化学试题吉林省吉化第一高级中学校2021-2022学年高一下学期复课检测化学试题湖北省恩施州高中教育联盟2020-2021学年高一下学期期末考试化学试题(已下线)第20讲 化学平衡常数及转化率的计算(练)-2023年高考化学一轮复习讲练测(新教材新高考)
名校
4 . 二氧化碳的捕获、利用是实现碳中和的一个重要战略方向。回答下列问题:
(1)已知:常温下,反应CaO(s)+CO2(g) CaCO3(s)能自发进行。则该反应为
CaCO3(s)能自发进行。则该反应为____ (填“吸热”或“放热”)反应;上述反应达到平衡后,若其他条件不变,增大CaO的用量,CO2的转化率将____ (填“增大”“减小”或“不变”)。
(2)工业上以CO2和H2为原料合成CH3OH涉及的主要反应如下:
反应I.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49kJ·mol-1
反应II.CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41kJ·mol-1
CO(g)+H2O(g) △H2=+41kJ·mol-1
①将反应物混合气按进料比n(CO2):n(H2)=1:3通入反应装置,选择合适的催化剂发生反应。
不同温度和压强下,CH3OH平衡产率如图所示。则图中的压强p1____ (填“>”“=”或“<”)p2,推断的依据是____ 。
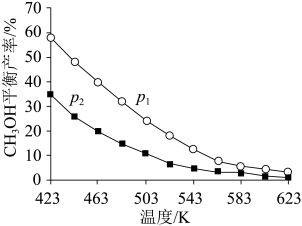
②T℃时,在体积为V的密闭容器中,反应I、II均达到化学平衡,CO2转化率为25%,且生成等物质的量的CH3OH和CO,则该温度下反应II的平衡常数的值为_____ (用分数表示)。
(3)调节溶液pH可实现工业废气中CO2的捕获和释放。已知20℃时碳酸的电离常数为Ka1、Ka2,当溶液pH=11时,c(H2CO3):c(HCO ):c(CO
):c(CO )=1:
)=1:____ :____ 。(用Ka1、Ka2表示)
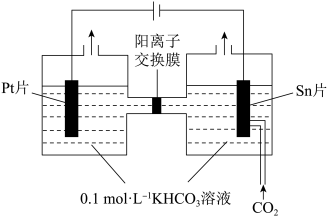
(4)电解CO2制HCOOH的原理如图所示,写出在Sn片上发生的电极反应式:____ 。
(1)已知:常温下,反应CaO(s)+CO2(g)
 CaCO3(s)能自发进行。则该反应为
CaCO3(s)能自发进行。则该反应为(2)工业上以CO2和H2为原料合成CH3OH涉及的主要反应如下:
反应I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49kJ·mol-1反应II.CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41kJ·mol-1
CO(g)+H2O(g) △H2=+41kJ·mol-1①将反应物混合气按进料比n(CO2):n(H2)=1:3通入反应装置,选择合适的催化剂发生反应。
不同温度和压强下,CH3OH平衡产率如图所示。则图中的压强p1

②T℃时,在体积为V的密闭容器中,反应I、II均达到化学平衡,CO2转化率为25%,且生成等物质的量的CH3OH和CO,则该温度下反应II的平衡常数的值为
(3)调节溶液pH可实现工业废气中CO2的捕获和释放。已知20℃时碳酸的电离常数为Ka1、Ka2,当溶液pH=11时,c(H2CO3):c(HCO
 ):c(CO
):c(CO )=1:
)=1:(4)电解CO2制HCOOH的原理如图所示,写出在Sn片上发生的电极反应式:

您最近一年使用:0次
2022-07-14更新
|
109次组卷
|
3卷引用:安徽省淮南市第一中学2023-2024学年高二下学期开学考试化学试题
解题方法
5 . 对于反应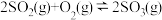
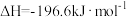 ,下列说法正确的是
,下列说法正确的是
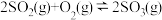
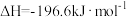 ,下列说法正确的是
,下列说法正确的是A.反应的 |
B.反应的平衡常数可表示为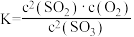 |
| C.使用高效催化剂能降低反应的焓变 |
| D.升温、加压和使用催化剂能增大SO3的生成速率 |
您最近一年使用:0次
2022-06-29更新
|
338次组卷
|
2卷引用:江苏省南京市临江高级中学2023-2024学年高二下学期期初考试化学试卷
6 . 化学在生产和日常生活中有着重要的应用。下列说法不正确的是
| A.明矾水解形成的Al(OH)3胶体能吸附水中的悬浮物,可用于水的净化 |
| B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
| C.电解NaCl饱和溶液,可制得金属钠 |
| D.2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H<0 |
您最近一年使用:0次
名校
解题方法
7 . Ⅰ.从氯二氟甲烷(CHClF2)中获得四氟乙烯(C2F4):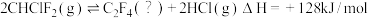 。
。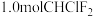 样品在18.5L容器内加热。反应达到平衡后,平衡混合物中含有
样品在18.5L容器内加热。反应达到平衡后,平衡混合物中含有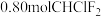 。
。
(1)写出四氟乙烯形成的高分子化合物聚四氟乙烯的结构简式_______ 。
(2)如图是一定条件下,反应物平衡时物质的量分数与压强的关系曲线。据此判断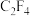 的状态是
的状态是 _______ (填“气体”、“液体”或“固体”)。
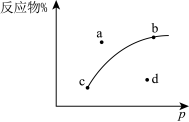
(3)该反应在_______ (填“高温”、“低温”或“任意温度”)的自发性更大;
(4)如图的a~d四点中,表示Q>K的点有_______ ;
(5)以平衡时气态物质的量分数表示平衡常数 ,其计算表达式为
,其计算表达式为 _______ 。
Ⅱ. 研究 氧化
氧化 制
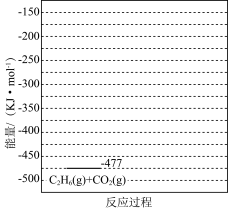
制 对资源综合利用有重要意义。相关的主要化学反应有(298K时,相关物质的相对能量如图):
对资源综合利用有重要意义。相关的主要化学反应有(298K时,相关物质的相对能量如图):
Ⅰ.C2H6(g) C2H4(g)+H2(g) △H1=136kJ·mol-1
C2H4(g)+H2(g) △H1=136kJ·mol-1
Ⅱ.C2H6(g)+CO2(g) C2H4(g)+H2O(g)+CO(g) △H2=177kJ·mol-1
C2H4(g)+H2O(g)+CO(g) △H2=177kJ·mol-1
Ⅲ.C2H6(g)+2CO2(g) 4CO(g)+3H2(g) △H3
4CO(g)+3H2(g) △H3
Ⅳ.CO2(g)+H2(g) CO(g)+H2O(g) △H4=41kJ·mol-1
CO(g)+H2O(g) △H4=41kJ·mol-1

(6)有研究表明,在催化剂存在下,反应Ⅱ分两步进行,过程如下:[C2H6(g)+CO2(g)]→[C2H4(g)+H2(g)+CO2(g)]→[C2H4(g)+CO(g)+H2O(g)],且第二步速率较慢(反应活化能为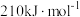 )。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量−反应过程图”,起点从[C2H6(g)+CO2(g)]的能量
)。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量−反应过程图”,起点从[C2H6(g)+CO2(g)]的能量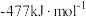 开始(如图)。
开始(如图)。_______
(7)① 和
和 按物质的量1:1投料,在923K和保持总压恒定的条件下,研究催化剂X对“
按物质的量1:1投料,在923K和保持总压恒定的条件下,研究催化剂X对“ 氧化
氧化 制
制 ”的影响,所得实验数据如下表:
”的影响,所得实验数据如下表:
结合具体反应分析,在催化剂X作用下, 氧化
氧化 的主要产物是
的主要产物是_______ ,判断依据是_______ 。
②采用选择性膜技术(可选择性地让某气体通过而离开体系)可提高 的选择性(生成
的选择性(生成 的物质的量与消耗
的物质的量与消耗 的物质的量之比)。在773K,乙烷平衡转化率为9.1%,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到11.0%。结合具体反应说明乙烷转化率增大的原因是
的物质的量之比)。在773K,乙烷平衡转化率为9.1%,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到11.0%。结合具体反应说明乙烷转化率增大的原因是_______ 。
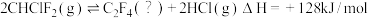 。
。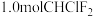 样品在18.5L容器内加热。反应达到平衡后,平衡混合物中含有
样品在18.5L容器内加热。反应达到平衡后,平衡混合物中含有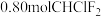 。
。(1)写出四氟乙烯形成的高分子化合物聚四氟乙烯的结构简式
(2)如图是一定条件下,反应物平衡时物质的量分数与压强的关系曲线。据此判断
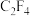 的状态是
的状态是 
(3)该反应在
(4)如图的a~d四点中,表示Q>K的点有
(5)以平衡时气态物质的量分数表示平衡常数
 ,其计算表达式为
,其计算表达式为 Ⅱ. 研究
 氧化
氧化 制
制 对资源综合利用有重要意义。相关的主要化学反应有(298K时,相关物质的相对能量如图):
对资源综合利用有重要意义。相关的主要化学反应有(298K时,相关物质的相对能量如图):Ⅰ.C2H6(g)
 C2H4(g)+H2(g) △H1=136kJ·mol-1
C2H4(g)+H2(g) △H1=136kJ·mol-1Ⅱ.C2H6(g)+CO2(g)
 C2H4(g)+H2O(g)+CO(g) △H2=177kJ·mol-1
C2H4(g)+H2O(g)+CO(g) △H2=177kJ·mol-1Ⅲ.C2H6(g)+2CO2(g)
 4CO(g)+3H2(g) △H3
4CO(g)+3H2(g) △H3Ⅳ.CO2(g)+H2(g)
 CO(g)+H2O(g) △H4=41kJ·mol-1
CO(g)+H2O(g) △H4=41kJ·mol-1
(6)有研究表明,在催化剂存在下,反应Ⅱ分两步进行,过程如下:[C2H6(g)+CO2(g)]→[C2H4(g)+H2(g)+CO2(g)]→[C2H4(g)+CO(g)+H2O(g)],且第二步速率较慢(反应活化能为
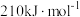 )。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量−反应过程图”,起点从[C2H6(g)+CO2(g)]的能量
)。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量−反应过程图”,起点从[C2H6(g)+CO2(g)]的能量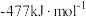 开始(如图)。
开始(如图)。
(7)①
 和
和 按物质的量1:1投料,在923K和保持总压恒定的条件下,研究催化剂X对“
按物质的量1:1投料,在923K和保持总压恒定的条件下,研究催化剂X对“ 氧化
氧化 制
制 ”的影响,所得实验数据如下表:
”的影响,所得实验数据如下表:| 催化剂 | 转化率C2H6/% | 转化率CO2/% | 产率C2H4/% |
| 催化剂X | 19.0 | 37.6 | 3.3 |
 氧化
氧化 的主要产物是
的主要产物是②采用选择性膜技术(可选择性地让某气体通过而离开体系)可提高
 的选择性(生成
的选择性(生成 的物质的量与消耗
的物质的量与消耗 的物质的量之比)。在773K,乙烷平衡转化率为9.1%,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到11.0%。结合具体反应说明乙烷转化率增大的原因是
的物质的量之比)。在773K,乙烷平衡转化率为9.1%,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到11.0%。结合具体反应说明乙烷转化率增大的原因是
您最近一年使用:0次
名校
8 . 下列有关电解质溶液的说法正确的是
| A.向0.1 mol·L-1 CH3COOH溶液中加入少量水,溶液中c(H+)/c(CH3COOH)减小 |
| B.利用焓判据可判断N2(g)+3H2(g)=2NH3(g) ∆H=-92.4 kJ·mol-1不能自发进行 |
| C.纯物质完全燃烧生成1 mol稳定氧化物时所放出的热量叫做该物质的燃烧热 |
| D.常温下,pH=2的醋酸与pH=12的NaOH溶液等体积混合后,溶液pH<7 |
您最近一年使用:0次
名校
解题方法
9 . 研究化学反应进行的方向对于反应设计等具有重要意义,下列说法正确的是
| A.2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g)在低温下能自发进行,则该反应的ΔH<0 |
| B.△H<0、△S>0的反应在温度低时不能自发进行 |
| C.常温下反应2Na2SO3(s)+O2(g)=2Na2SO4(s)能自发进行,则ΔH>0 |
| D.在其他外界条件不变的情况下,汽车排气管中使用催化剂,可改变产生尾气的反应方向 |
您最近一年使用:0次
2022-04-11更新
|
117次组卷
|
3卷引用:四川省遂宁中学校2021-2022学年高二下学期开学考试化学试题
名校
解题方法
10 . 下列反应在常温下均为非自发反应,在高温下仍为非自发的是
| A. NH4Cl(s) = NH3(g)+ HCl(g) |
B.Fe2O3(s) + C(s)=2Fe(s) + C(s)=2Fe(s) + CO2(g) CO2(g) |
C.Ag2O(s)=2Ag(s) + O2 (g) O2 (g) |
| D.2CO(g)=2C(s) + O2(g) |
您最近一年使用:0次



