名校
1 . 焦亚硫酸钠 是一种常用的还原剂,溶于水即生成
是一种常用的还原剂,溶于水即生成 ,用
,用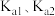 分别表示
分别表示 的一级与二级电离平衡常数。
的一级与二级电离平衡常数。 时,
时, 溶液中含硫微粒分布系数随
溶液中含硫微粒分布系数随 变化如图所示,已知
变化如图所示,已知 ,下列说法不正确的是
,下列说法不正确的是
 是一种常用的还原剂,溶于水即生成
是一种常用的还原剂,溶于水即生成 ,用
,用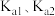 分别表示
分别表示 的一级与二级电离平衡常数。
的一级与二级电离平衡常数。 时,
时, 溶液中含硫微粒分布系数随
溶液中含硫微粒分布系数随 变化如图所示,已知
变化如图所示,已知 ,下列说法不正确的是
,下列说法不正确的是
A. 时, 时,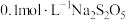 水溶液中 水溶液中 |
B.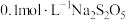 水溶液中 水溶液中 |
C.利用 氧化 氧化 回收单质硫,溶液中存在反应: 回收单质硫,溶液中存在反应: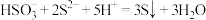 |
D.向 溶液中滴加 溶液中滴加 溶液,发生反应: 溶液,发生反应: ,其平衡常数 ,其平衡常数 |
您最近一年使用:0次
名校
2 . 向硫酸铜溶液中通入氨气,溶液中含Cu微粒存在如下平衡: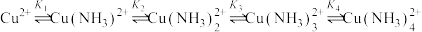 ,各含铜组分分布系数与
,各含铜组分分布系数与 关系如图所示。下列说法错误的是
关系如图所示。下列说法错误的是
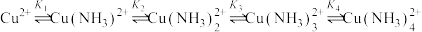 ,各含铜组分分布系数与
,各含铜组分分布系数与 关系如图所示。下列说法错误的是
关系如图所示。下列说法错误的是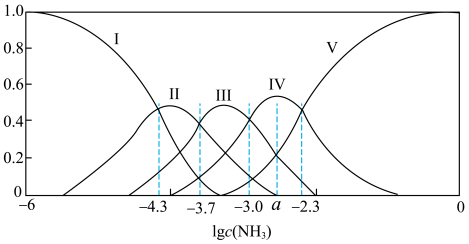
A.曲线Ⅰ代表 |
B.反应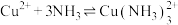 的平衡常数的值为 的平衡常数的值为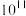 |
C.当溶液中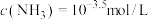 时,溶液中离子浓度最大的是 时,溶液中离子浓度最大的是 |
| D.a=-2.65 |
您最近一年使用:0次
名校
3 . 常温下,用 的
的 标准溶液滴定同浓度
标准溶液滴定同浓度 的
的 溶液。已知:草酸
溶液。已知:草酸 ,
,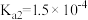 ;一水合氨
;一水合氨 。下列说法不正确的是
。下列说法不正确的是
 的
的 标准溶液滴定同浓度
标准溶液滴定同浓度 的
的 溶液。已知:草酸
溶液。已知:草酸 ,
,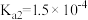 ;一水合氨
;一水合氨 。下列说法不正确的是
。下列说法不正确的是A.滴定过程中,溶液中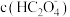 逐渐减小 逐渐减小 |
B. 时: 时: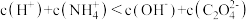 |
C. 时: 时: |
D. 分别为 分别为 和 和 时水的电离程度:前者>后着 时水的电离程度:前者>后着 |
您最近一年使用:0次
名校
4 . 亚砷酸(H3AsO3)可用于治疗白血病,亚砷酸在溶液中存在多种微粒形态,向1L0.1mol/LH3AsO3溶液中逐滴加入0.1mol/LKOH溶液,各种微粒的物质的量分数与溶液pH的关系如图所示,下列说法错误的是
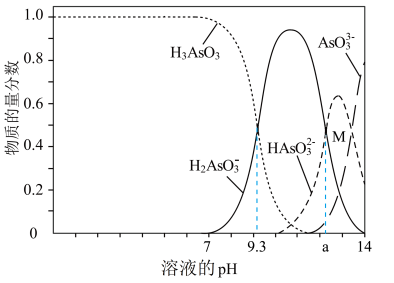
| A.人体血液的pH约为7.35-7.45,服用药物后血液中所含砷元素的主要微粒是H3AsO3 |
| B.该温度下,H3AsO3的电离平衡常数Ka的数量级为10-10 |
C. 时,溶液中: 时,溶液中: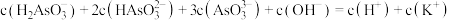 |
D.M点对应的溶液中: |
您最近一年使用:0次
名校
5 . 常温下,向一定浓度邻苯二甲酸钠( 表示)溶液中通入
表示)溶液中通入 气体,保持溶液体积和温度不变,测得
气体,保持溶液体积和温度不变,测得 与
与 [
[ 为
为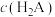 、
、 、
、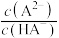 ;
; ]的变化关系如图所示,下列说法错误的是
]的变化关系如图所示,下列说法错误的是
 表示)溶液中通入
表示)溶液中通入 气体,保持溶液体积和温度不变,测得
气体,保持溶液体积和温度不变,测得 与
与 [
[ 为
为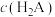 、
、 、
、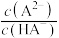 ;
; ]的变化关系如图所示,下列说法错误的是
]的变化关系如图所示,下列说法错误的是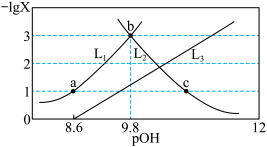
A.曲线 表示 表示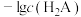 |
B. 点溶液中: 点溶液中: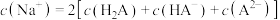 |
C. 的 的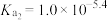 |
D.该溶液中通入和 等物质的量的 等物质的量的 时溶液显碱性 时溶液显碱性 |
您最近一年使用:0次
2024-04-15更新
|
250次组卷
|
2卷引用:重庆市巴蜀中学2023-2024学年高三下学期 适应性月考卷(八)化学试题
名校
6 . 下列方案设计、现象和结论都正确的是
| 编号 | 实验目的 | 方案设计 | 现象与结论 |
| A | 比较 与 与 的酸性强弱 的酸性强弱 | 分别测 、 、 两饱和溶液的 两饱和溶液的 |  溶液 溶液 小,则酸性 小,则酸性 |
| B | 验证 溶液中存在水解平衡 溶液中存在水解平衡 | 往含有酚酞 溶液中加入少量 溶液中加入少量 晶体 晶体 | 溶液红色变浅,则 溶液中存在水解平衡 溶液中存在水解平衡 |
| C | 比较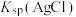 与 与 的大小 的大小 | 向足量 溶液中先加入少量 溶液中先加入少量 溶液,再加入 溶液,再加入 溶液 溶液 | 先生成白色沉淀,再生成淡黄色沉淀,则 |
| D | 探究压强对化学平衡的影响 | 快速压缩装有 、 、 平衡混合气体的针筒活塞 平衡混合气体的针筒活塞 | 平衡后气体颜色变深,则增大压强,平衡向生成 的方向移动 的方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 .  时,下图表示起始浓度为
时,下图表示起始浓度为 的
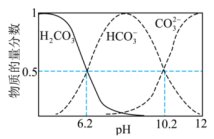
的 溶液中各含碳粒子物质的量分数与
溶液中各含碳粒子物质的量分数与 的变化关系。已知:
的变化关系。已知: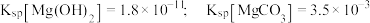 。下列说法错误的是
。下列说法错误的是
 时,下图表示起始浓度为
时,下图表示起始浓度为 的
的 溶液中各含碳粒子物质的量分数与
溶液中各含碳粒子物质的量分数与 的变化关系。已知:
的变化关系。已知: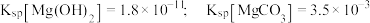 。下列说法错误的是
。下列说法错误的是
A.起始时,溶液中一定有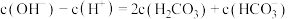 |
B.当 时,溶液中 时,溶液中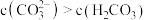 |
C.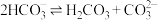 的平衡常数 的平衡常数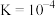 |
D.当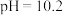 时,向溶液中加入足量 时,向溶液中加入足量 溶液,溶液中会产生两种沉淀 溶液,溶液中会产生两种沉淀 |
您最近一年使用:0次
名校
解题方法
8 . 下列实验操作及现象与结论均正确的是
实验操作及现象 | 结论 | |
A | 向氢氧化铁胶体中插入碳棒,连接直流电源,连接负极的碳棒周围颜色变深 | 氢氧化铁胶体带正电 |
B | 常温下,将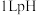 均为2的 均为2的 溶液和 溶液和 溶液分别与相同大小的 溶液分别与相同大小的 片反应, 片反应, 溶液产生气体平均速率较快 溶液产生气体平均速率较快 | 酸性: |
C | 向淀粉溶液中加入稀硫酸,加热,一段时间后,冷却,再加入新制的 ,加热,未出现砖红色沉淀 ,加热,未出现砖红色沉淀 | 淀粉未水解 |
D | 点燃氯气,然后把导管伸入盛有氢气的集气瓶,产生苍白色火焰,集气瓶口有白雾 | 白雾是盐酸小液滴 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 甲胺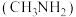 是一种弱碱
是一种弱碱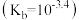 ,可与盐酸反应生成盐酸盐(用
,可与盐酸反应生成盐酸盐(用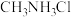 表示)。下列叙述不正确的是
表示)。下列叙述不正确的是
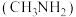 是一种弱碱
是一种弱碱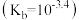 ,可与盐酸反应生成盐酸盐(用
,可与盐酸反应生成盐酸盐(用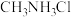 表示)。下列叙述不正确的是
表示)。下列叙述不正确的是A.甲胺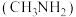 中氮原子采用 中氮原子采用 杂化 杂化 |
B. 水溶液的 水溶液的 |
C.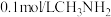 水溶液加水稀释, 水溶液加水稀释, 降低 降低 |
D.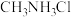 水溶液中: 水溶液中: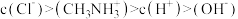 |
您最近一年使用:0次
名校
10 . 某温度下,向 和
和 的混合溶液中逐滴加入某浓度的
的混合溶液中逐滴加入某浓度的 溶液,测得溶液中的离子浓度的关系如图所示,已知该温度下
溶液,测得溶液中的离子浓度的关系如图所示,已知该温度下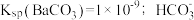 的电离平衡常数为
的电离平衡常数为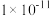 ,下列说法错误的是
,下列说法错误的是
 和
和 的混合溶液中逐滴加入某浓度的
的混合溶液中逐滴加入某浓度的 溶液,测得溶液中的离子浓度的关系如图所示,已知该温度下
溶液,测得溶液中的离子浓度的关系如图所示,已知该温度下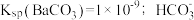 的电离平衡常数为
的电离平衡常数为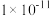 ,下列说法错误的是
,下列说法错误的是
A.该温度下a点溶液的 为7 为7 |
B.b点溶液中存在 |
C.b点溶液中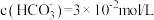 |
D.a、b、c三点溶液中 最大的是c点 最大的是c点 |
您最近一年使用:0次
2024-03-17更新
|
154次组卷
|
2卷引用:重庆市七校联盟2023-2024学年高三下学期第一次月考化学试题



