名校
解题方法
1 . 已知HF的酸性强于CH3COOH,常温下有下列三种溶液,有关叙述中不正确的是
| 编号 | ① | ② | ③ |
| pH | 11 | 3 | 3 |
| 溶液 | NaOH溶液 | CH3COOH溶液 | HF溶液 |
| A.②、③混合后: c(H+)=c(F-)+c(CH3COO-)+c(OH-) |
| B.①、②等体积混合后:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C.中和相同体积的②、③,需消耗相同体积的① |
| D.向③中加入CH3COONa固体,HF的电离平衡向右移动 |
您最近一年使用:0次
名校
解题方法
2 . 下列离子方程式书写正确的是
A.NaHCO3的电离:NaHCO3  Na+ + Na+ +  |
| B.铁与稀硝酸反应:Fe +2H+ = Fe 2+ + H2↑ |
C.AlCl3溶液与Na2S溶液反应:2Al3++ 3S2-+ 6H2O  2Al(OH)3 + 3H2S 2Al(OH)3 + 3H2S |
D.以Pt为电极材料电解AgNO3溶液:4Ag+ + 2H2O 4Ag + O2↑+ 4H+ 4Ag + O2↑+ 4H+ |
您最近一年使用:0次
名校
解题方法
3 . 填空题(共12分)
(1)室温下,将等体积的氨水与盐酸溶液混合后,若混合溶液中c( )=c(Cl-),则溶液中的pH值
)=c(Cl-),则溶液中的pH值____ 7(填“>”、“<”或“=”,下同),混合前c(NH3·H2O)_____ c(HCl)
(2)等浓度的NH4Cl和氨水溶液中,水电离出的H+浓度,前者______ 后者。
(3)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_______ 。
(4)在配制硫化钠溶液时,为了抑制水解,可以加入少量的________ 。
(5)Na2SO3溶液与CaCl2溶液混合会生成难溶的CaSO3(Ksp=3.1×10−1),现将等体积的CaCl2溶液与Na2SO3溶液混合,若混合前Na2SO3溶液浓度为2×10−1 mol∙L−1,则生成沉淀所需CaCl2溶液的最小浓度为________ 。
(1)室温下,将等体积的氨水与盐酸溶液混合后,若混合溶液中c(
 )=c(Cl-),则溶液中的pH值
)=c(Cl-),则溶液中的pH值(2)等浓度的NH4Cl和氨水溶液中,水电离出的H+浓度,前者
(3)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
(4)在配制硫化钠溶液时,为了抑制水解,可以加入少量的
(5)Na2SO3溶液与CaCl2溶液混合会生成难溶的CaSO3(Ksp=3.1×10−1),现将等体积的CaCl2溶液与Na2SO3溶液混合,若混合前Na2SO3溶液浓度为2×10−1 mol∙L−1,则生成沉淀所需CaCl2溶液的最小浓度为
您最近一年使用:0次
名校
解题方法
4 . 常温下,有0.1mol/L的四种溶液:①HCl ②CH3COOH ③NaOH ④Na2CO3。
(1)用化学用语解释溶液②呈酸性的原因:___________ 。
(2)溶液③的pH=___________ 。
(3)溶液①、②分别与等浓度、等体积的溶液③恰好完全反应,消耗的体积:①_____ ②(填“>”、“<”或"=")。
(4)溶液④加热后碱性增强,结合化学用语解释原因:___________ 。
(5)常温下,下列关于溶液②的判断正确的是___________ 。
a.c(CH3COO-)=0.1mol/L b.溶液中c(H+)>c(CH3COO-)>c(OH-)
c.加入CH3COONa(s),c(H+)不变 d.滴入NaOH浓溶液,溶液导电性增强
(1)用化学用语解释溶液②呈酸性的原因:
(2)溶液③的pH=
(3)溶液①、②分别与等浓度、等体积的溶液③恰好完全反应,消耗的体积:①
(4)溶液④加热后碱性增强,结合化学用语解释原因:
(5)常温下,下列关于溶液②的判断正确的是
a.c(CH3COO-)=0.1mol/L b.溶液中c(H+)>c(CH3COO-)>c(OH-)
c.加入CH3COONa(s),c(H+)不变 d.滴入NaOH浓溶液,溶液导电性增强
您最近一年使用:0次
名校
5 . 完成下列问题
(1)硫酸铝水解的离子方程式是___________ ,为了抑制其水解,配制时可以加入少量的___________ (填化学式)。
(2)饱和NH4Cl溶液加入镁条,则观察到有气泡产生,点燃有爆鸣声,此气体为___________ 产生该气体的原因是___________ (用离子方程式表示),微热后能放出有刺激性气味的气体,该气体是___________ ,产生该气体的原因是___________ 。
(1)硫酸铝水解的离子方程式是
(2)饱和NH4Cl溶液加入镁条,则观察到有气泡产生,点燃有爆鸣声,此气体为
您最近一年使用:0次
名校
6 . 为了配制NH 的浓度与Cl-的浓度之比为1∶1的溶液,可在NH4Cl溶液中加入
的浓度与Cl-的浓度之比为1∶1的溶液,可在NH4Cl溶液中加入
①适量的HCl ②适量的(NH4)2SO4 ③适量的氨水 ④适量的NaOH
 的浓度与Cl-的浓度之比为1∶1的溶液,可在NH4Cl溶液中加入
的浓度与Cl-的浓度之比为1∶1的溶液,可在NH4Cl溶液中加入①适量的HCl ②适量的(NH4)2SO4 ③适量的氨水 ④适量的NaOH
| A.①② | B.②③ | C.③④ | D.①④ |
您最近一年使用:0次
名校
解题方法
7 . 实验小组制备硫代硫酸钠(Na2S2O3)并探究其性质。
资料:ⅰ.S2O +2H+=S↓+SO2↑+H2O
+2H+=S↓+SO2↑+H2O
ⅱ.Fe3++3S2O
 Fe(S2O3)
Fe(S2O3) (紫黑色)
(紫黑色)
ⅲ.Ag2S2O3是难溶于水、可溶于Na2S2O3溶液的白色固体。
(1)实验室可利用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制备Na2S2O3,装置如下图。

①用化学用语解释Na2S和Na2CO3的混合溶液呈碱性的原因:S2-+H2O HS-+OH-、
HS-+OH-、___________ 。
②为了保证Na2S2O3的产量,实验中通入的SO2不能过量。要控制SO2的生成速率,可以采取的措施有:___________ (写出一条)。
(2)探究Na2S2O3溶液与不同金属的硫酸盐溶液间反应的多样性。
①Ⅰ中产生白色沉淀的离子方程式为___________ 。
②经检验,现象Ⅱ中的沉淀有Al(OH)3和S,用平衡移动原理解释Ⅱ中的现象:___________ 。
③经检验,现象中的无色溶液中含有Fe2+。从化学反应速率和限度的角度解释Ⅲ中Fe3+与S2O 反应的实验现象:
反应的实验现象:___________ 。
以上实验说明:Na2S2O3溶液与金属阳离子反应的多样性和阳离子的性质有关。
资料:ⅰ.S2O
 +2H+=S↓+SO2↑+H2O
+2H+=S↓+SO2↑+H2O ⅱ.Fe3++3S2O

 Fe(S2O3)
Fe(S2O3) (紫黑色)
(紫黑色)ⅲ.Ag2S2O3是难溶于水、可溶于Na2S2O3溶液的白色固体。
(1)实验室可利用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制备Na2S2O3,装置如下图。

①用化学用语解释Na2S和Na2CO3的混合溶液呈碱性的原因:S2-+H2O
 HS-+OH-、
HS-+OH-、②为了保证Na2S2O3的产量,实验中通入的SO2不能过量。要控制SO2的生成速率,可以采取的措施有:
(2)探究Na2S2O3溶液与不同金属的硫酸盐溶液间反应的多样性。
| 实验 | 试剂 | 现象 | |
 | 试管 | 滴管 | |
| 2mL0.1mol/LNa2S2O3溶液 | Ag2SO4溶液(浓度约为0.03mol/L) | Ⅰ.局部生成白色沉淀,振荡后沉淀溶解,得到无色溶液 | |
| 0.03mol/LAl2(SO4)3溶液 | Ⅱ.一段时间后,生成沉淀 | ||
| 0.03mol/LFe2(SO4)3溶液 | Ⅲ.混合后溶液先变成紫黑色,30s时溶液几乎变为无色 | ||
②经检验,现象Ⅱ中的沉淀有Al(OH)3和S,用平衡移动原理解释Ⅱ中的现象:
③经检验,现象中的无色溶液中含有Fe2+。从化学反应速率和限度的角度解释Ⅲ中Fe3+与S2O
 反应的实验现象:
反应的实验现象:以上实验说明:Na2S2O3溶液与金属阳离子反应的多样性和阳离子的性质有关。
您最近一年使用:0次
2023-12-27更新
|
51次组卷
|
2卷引用:北京市第八中学2022-2023学年高二上学期期中考试化学试题
名校
8 . 25℃时,在20.0mL0.10mol/L氨水中滴入0.10mol·L-1的盐酸,溶液pH与所加盐酸的体积关系如图所示。下列有关叙述不正确的是


| A.a点对应溶液中已电离的NH3·H2O为10-2.8mol·L-1 |
| B.b点对应盐酸的体积小于20.0mL |
C.b点对应溶液中c(Cl-)=c(NH ) ) |
D.加入10mL盐酸时:c(NH )>c(NH3·H2O) >c(Cl-) )>c(NH3·H2O) >c(Cl-) |
您最近一年使用:0次
2023-12-26更新
|
136次组卷
|
2卷引用:北京市第八中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
9 . 下列说法不正确的是
A.将NaOH溶液从常温加热至 ,溶液的pH变小但仍保持碱性 ,溶液的pH变小但仍保持碱性 |
| B.常温下,pH=3的醋酸溶液中加醋酸钠固体,醋酸的电离程度和水电离的c(H+)均减小 |
| C.常温下,pH=7的氯化铵和氨水混合液,加少量水稀释后pH不变 |
| D.常温下,向AgCl悬浊液中加入少量稀盐酸,AgCl溶解度减小,Ksp不变,c(Ag+)减小 |
您最近一年使用:0次
名校
解题方法
10 . 常温下,下列有关电解质溶液的说法正确的是
| A.pH= 4的H2S溶液与pH= 10的NaOH溶液等体积混合,所得混合溶液中:c(Na+)+c(H+)=c(OH-)+ 2c(S2-) + c(HS-) |
B.将CH3COONa溶液从20℃升温至30℃,溶液中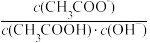 增大 增大 |
C.向0.1 mol·L-1CH3COOH溶液中加入少量水,溶液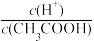 减小 减小 |
| D.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液中:c(Na+)>c(CH3COO-)> c(H+)>c(OH-) |
您最近一年使用:0次



