解题方法
1 . 常温下,向0.1mol∙L-1二元弱酸H2A溶液中逐滴加入NaOH溶液,H2A、HA-、A2-的物质的量分数[已知 ]。随pH的变化如图所示。下列叙述正确的是
]。随pH的变化如图所示。下列叙述正确的是
 ]。随pH的变化如图所示。下列叙述正确的是
]。随pH的变化如图所示。下列叙述正确的是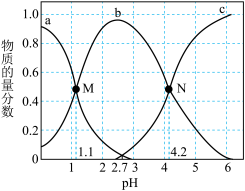
| A.a曲线代表A2-的物质的量分数随pH的变化 |
| B.溶液pH=1时的导电能力强于pH=6时的导电能力 |
| C.H2A第二步电离常数Ka2=10-4.2 |
| D.N点pH=4.2时,c(A2-)=c(HA-),溶液中不存在H2A分子 |
您最近一年使用:0次
2 . 常温下0.2mol•L-1NaHCO3溶液与0.1mol•L-1Na2CO3溶液等体积混合后,下列关于说法不正确 的是
A.NaHCO3=Na++ | B.c(Na+)>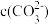 > > >c(OH-) >c(OH-) |
C.c(H+)+c(Na+)=c(OH-)+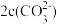 + + | D.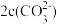 + + + +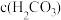 <c(Na+) <c(Na+) |
您最近一年使用:0次
3 . 在一定条件下,Na2S溶液存在水解平衡;S2-+H2O HS-+OH-。下列说法正确的是
HS-+OH-。下列说法正确的是
 HS-+OH-。下列说法正确的是
HS-+OH-。下列说法正确的是| A.加水稀释,平衡正移,HS-浓度增大 | B.升高温度, 减少 减少 |
| C.稀释溶液,水解平衡常数不变 | D.加入NaOH固体,溶液pH减小 |
您最近一年使用:0次
4 . 物质的量浓度相同的NaX、NaY和NaZ溶液,其pH依次为9、11、10,则HX、HY、HZ的电离平衡常数由大到小的顺序是
| A.HX,HZ, HY | B.HX,HY,HZ |
| C.HZ,HY,HX | D.HY,HZ,HX |
您最近一年使用:0次
名校
5 . 在室温下,下列四种溶液:①0.1 mol/L NH4Cl溶液,②0.1 mol/L CH3COONH4溶液,③0.1mol/L NH4HSO4溶液,④0.1 mol/L氨水。
(1)溶液①呈酸性的原因是___________ (用离子方程式表示)。
(2)溶液③的电离方程式为___________
(3)在上述①、②、 ③、④溶液中c ( )浓度由大到小的顺序是
)浓度由大到小的顺序是___________ (填序号)。
(4)25℃时,将pH=9的NaOH溶液与p=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为___________ 。
(5)25℃时,向0.1mol/L FeCl3溶液中加入④溶液,若Fe(OH)3的Ksp=1×10-39,当铁离子恰好完全沉淀时[当c(Fe3+)小于10-6mol/L时,可忽略不计],溶液的pH=___________ 。
(1)溶液①呈酸性的原因是
(2)溶液③的电离方程式为
(3)在上述①、②、 ③、④溶液中c (
 )浓度由大到小的顺序是
)浓度由大到小的顺序是(4)25℃时,将pH=9的NaOH溶液与p=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为
(5)25℃时,向0.1mol/L FeCl3溶液中加入④溶液,若Fe(OH)3的Ksp=1×10-39,当铁离子恰好完全沉淀时[当c(Fe3+)小于10-6mol/L时,可忽略不计],溶液的pH=
您最近一年使用:0次
6 . 已知25℃时,部分弱电解质的电离平衡常数数据如下表:
回答下列问题:
(1)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的 由小到大的顺序为
由小到大的顺序为___________ (填字母序号)。
(2)常温下,0.1mol/L醋酸溶液加水稀释过程中,下列表达式的数据减小的是___________(填字母序号)。
(3)25℃时,将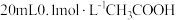 溶液和
溶液和 溶液分别与
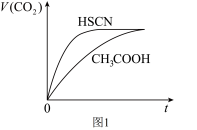
溶液分别与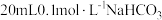 溶液混合,实验测得产生的气体体积(V)随时间(t)变化如图1所示:反应初始阶段两种溶液产生
溶液混合,实验测得产生的气体体积(V)随时间(t)变化如图1所示:反应初始阶段两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是___________ 反应结束后所得两溶液中,c(SCN-)_________ c(CH3COO-)(填“>”“<”或“=”)。
(4)体积均为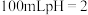 的
的 与一元酸
与一元酸 ,加水稀释过程中
,加水稀释过程中 与溶液体积的关系如图2所示,则
与溶液体积的关系如图2所示,则 的电离平衡常数
的电离平衡常数___________ (填“大于”、“小于”或“等于”) 的电离平衡常数。
的电离平衡常数。

(5)25℃时,在 与
与 的混合溶液中,若测得
的混合溶液中,若测得 ,则溶液中
,则溶液中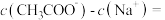
________ mol/L(填精确值),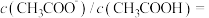
___________ 。
| 弱酸化学式 |  |  |  |  |
| 电离平衡常数 | 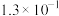 |  |  | 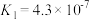 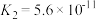 |
(1)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的
 由小到大的顺序为
由小到大的顺序为(2)常温下,0.1mol/L醋酸溶液加水稀释过程中,下列表达式的数据减小的是___________(填字母序号)。
A. | B. |
C.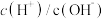 | D. |
(3)25℃时,将
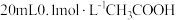 溶液和
溶液和 溶液分别与
溶液分别与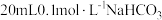 溶液混合,实验测得产生的气体体积(V)随时间(t)变化如图1所示:反应初始阶段两种溶液产生
溶液混合,实验测得产生的气体体积(V)随时间(t)变化如图1所示:反应初始阶段两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是
(4)体积均为
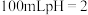 的
的 与一元酸
与一元酸 ,加水稀释过程中
,加水稀释过程中 与溶液体积的关系如图2所示,则
与溶液体积的关系如图2所示,则 的电离平衡常数
的电离平衡常数 的电离平衡常数。
的电离平衡常数。
(5)25℃时,在
 与
与 的混合溶液中,若测得
的混合溶液中,若测得 ,则溶液中
,则溶液中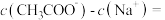
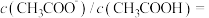
您最近一年使用:0次
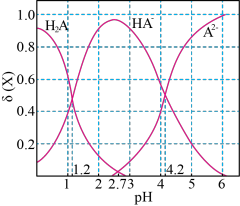
7 . 常温下,将0.1mol/L的二元弱酸H2A溶液与NaOH溶液混合,H2A、HA-、A2-的物质的量浓度分数 随体系pH的变化如图所示【已知
随体系pH的变化如图所示【已知 】。下列叙述错误的是
】。下列叙述错误的是
 随体系pH的变化如图所示【已知
随体系pH的变化如图所示【已知 】。下列叙述错误的是
】。下列叙述错误的是 
A. 时,溶液中一定存在c(Na+)+c(H+)=c(OH-)+3c(HA-) 时,溶液中一定存在c(Na+)+c(H+)=c(OH-)+3c(HA-) |
B.常温下,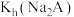 的数量级为 的数量级为 |
C. 时, 时,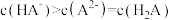 |
| D.混合溶液始终存在c(Na+)= c(HA-)+2c(A2-) |
您最近一年使用:0次
8 . 下列说法正确的是
A.常温下, 的 的 溶液中,由水电离的 溶液中,由水电离的 |
B.将 的 的 溶液和 溶液和 的 的 溶液等体积混合,所得溶液 溶液等体积混合,所得溶液 |
C. 氨水和 氨水和 溶液等体积混合后所得溶液pH>7,则c(NH 溶液等体积混合后所得溶液pH>7,则c(NH )>c(NH3·H2O) )>c(NH3·H2O) |
D.向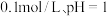 的 的 溶液中加入 溶液中加入 溶液反应的离子方程式为: 溶液反应的离子方程式为: |
您最近一年使用:0次
9 . 亚磷酸(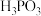 )是一种二元弱酸,常温下电离常数
)是一种二元弱酸,常温下电离常数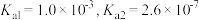 ,下列说法正确的是
,下列说法正确的是
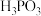 )是一种二元弱酸,常温下电离常数
)是一种二元弱酸,常温下电离常数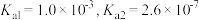 ,下列说法正确的是
,下列说法正确的是A.H3PO3与足量的 溶液反应生成的Na2HPO3是酸式盐 溶液反应生成的Na2HPO3是酸式盐 |
| B.NaH2PO3溶液显酸性 |
C.向亚磷酸溶液中加入少量 固体,则 固体,则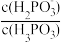 变小 变小 |
D.对 的亚磷酸溶液加水稀释,溶液中所有离子浓度均减小 的亚磷酸溶液加水稀释,溶液中所有离子浓度均减小 |
您最近一年使用:0次
名校
解题方法
10 . 已知HF的酸性强于CH3COOH,常温下有下列三种溶液,有关叙述中不正确的是
| 编号 | ① | ② | ③ |
| pH | 11 | 3 | 3 |
| 溶液 | NaOH溶液 | CH3COOH溶液 | HF溶液 |
| A.②、③混合后: c(H+)=c(F-)+c(CH3COO-)+c(OH-) |
| B.①、②等体积混合后:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C.中和相同体积的②、③,需消耗相同体积的① |
| D.向③中加入CH3COONa固体,HF的电离平衡向右移动 |
您最近一年使用:0次



