名校
1 . 某一元弱酸HA在水中的电离方程式是HA H++A-,回答下列问题:
H++A-,回答下列问题:
(1)向纯水中加入适量HA,水的电离平衡将向______ (填“正”、"逆")反应方向移动。
(2)若向(1)所得溶液中加入适量NaCl溶液,以上平衡将向________ (填"正"、"逆")反应方向移动,溶液中c(A-)将________ (填"增大"、"减小"或"不变"),溶液中c(OH-)将________ (填“增大”、“减小”或“不变”)。
(3)在25℃下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应平衡时溶液中c(NH )=c(Cl-),则溶液显
)=c(Cl-),则溶液显_______ 性(填"酸"、"碱"或"中"),a________ 0.01(填">"、"="或"<"),用含a的代数式表示NH3•H2O的电离常数Kb=________ 。
(4)常温时,取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8。试回答以下问题:
①混合溶液的pH=8的原因是_______ (用离子方程式表示)。
②求出混合液中下列算式的精确计算结果(填具体数字,用科学计数法保留两位有效数字):c(Na+)-c(A-)=_______ mol/L;c(OH-)-c(HA)=________ mol/L。
 H++A-,回答下列问题:
H++A-,回答下列问题:(1)向纯水中加入适量HA,水的电离平衡将向
(2)若向(1)所得溶液中加入适量NaCl溶液,以上平衡将向
(3)在25℃下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应平衡时溶液中c(NH
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显(4)常温时,取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8。试回答以下问题:
①混合溶液的pH=8的原因是
②求出混合液中下列算式的精确计算结果(填具体数字,用科学计数法保留两位有效数字):c(Na+)-c(A-)=
您最近一年使用:0次
名校
2 . 下列化学用语表示正确的是
| A.HF在水溶液中电离:HF=H++F- |
B.Na2S在水溶液中水解:S2-+H2O HS-+OH- HS-+OH- |
C.BaSO4在水溶液中电离:BaSO4 Ba2++SO Ba2++SO |
D.弱酸的酸式盐NaHB在水溶液中水解:HB-+H2O H3O++B2- H3O++B2- |
您最近一年使用:0次
名校
3 . 化学与生产、生活密切相关。根据盐类水解的知识,判断下列说法正确的是
①利用明矾可清除铜表面的铜锈
②配制FeSO4溶液时,将FeSO4固体溶于稀盐酸中然后稀释至所需浓度
③将CuCl2溶液和CuSO4溶液分别加热、蒸干、灼烧,所得固体成分相同
④明矾可作净水剂,原理为Al3++3H2O Al(OH)3↓+3H+
Al(OH)3↓+3H+
⑤废旧钢材焊接前,可用饱和NH4Cl溶液处理焊点的铁锈
⑥可利用水解反应制备无机化合物,如用TiCl4制备TiO2
⑦将草木灰与NH4Cl混合施用,可更好地为植物提供N、K两种营养元素
⑧加热纯碱溶液可以增强其去油污的能力
①利用明矾可清除铜表面的铜锈
②配制FeSO4溶液时,将FeSO4固体溶于稀盐酸中然后稀释至所需浓度
③将CuCl2溶液和CuSO4溶液分别加热、蒸干、灼烧,所得固体成分相同
④明矾可作净水剂,原理为Al3++3H2O
 Al(OH)3↓+3H+
Al(OH)3↓+3H+⑤废旧钢材焊接前,可用饱和NH4Cl溶液处理焊点的铁锈
⑥可利用水解反应制备无机化合物,如用TiCl4制备TiO2
⑦将草木灰与NH4Cl混合施用,可更好地为植物提供N、K两种营养元素
⑧加热纯碱溶液可以增强其去油污的能力
| A.①②⑤⑦ | B.④⑤⑥⑧ | C.①⑤⑥⑧ | D.③④⑤⑧ |
您最近一年使用:0次
2023-10-04更新
|
162次组卷
|
2卷引用:河南省南阳市第一中学校2022-2023学年高二上学期12月月考化学试题
名校
4 .  时,将
时,将 气体缓慢通入
气体缓慢通入 的氨水中,溶液的
的氨水中,溶液的 、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比 [
、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比 [ ]的关系如下图所示。若忽略溶液体积变化,下列错误的是
]的关系如下图所示。若忽略溶液体积变化,下列错误的是
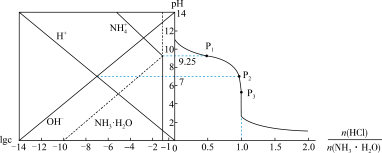
 时,将
时,将 气体缓慢通入
气体缓慢通入 的氨水中,溶液的
的氨水中,溶液的 、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比 [
、体系中粒子浓度的对数值(lgc)与反应物的物质的量之比 [ ]的关系如下图所示。若忽略溶液体积变化,下列错误的是
]的关系如下图所示。若忽略溶液体积变化,下列错误的是
A. 时, 时, 的电离平衡常数为 的电离平衡常数为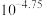 |
B. 时, 时,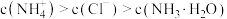 |
C. 所示溶液: 所示溶液: |
D.水的电离程度: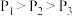 |
您最近一年使用:0次
名校
解题方法
5 . 下列实验操作能达到目的的是
| 选项 | A | B | C | D |
| 实验 | 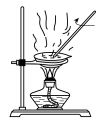 蒸发  溶液提取 溶液提取 固体 固体 |  探究催化剂对化学反应速率的影响 | 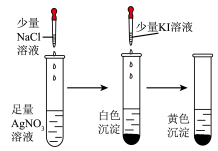 验证  和 和 的 的 大小 大小 |  碱式滴定管排气泡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
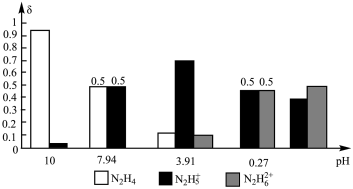
6 .  可看作二元弱碱,在水中发生电离:
可看作二元弱碱,在水中发生电离: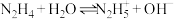 ,
, 。25℃时,向
。25℃时,向 溶液中滴入盐酸,滴加过程中
溶液中滴入盐酸,滴加过程中 、
、 、
、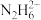 三种微粒的物质的量分数
三种微粒的物质的量分数 [如
[如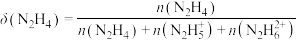 ]随
]随 的变化如图所示,下列叙述正确的是
的变化如图所示,下列叙述正确的是
 可看作二元弱碱,在水中发生电离:
可看作二元弱碱,在水中发生电离: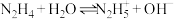 ,
, 。25℃时,向
。25℃时,向 溶液中滴入盐酸,滴加过程中
溶液中滴入盐酸,滴加过程中 、
、 、
、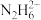 三种微粒的物质的量分数
三种微粒的物质的量分数 [如
[如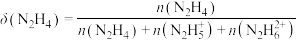 ]随
]随 的变化如图所示,下列叙述正确的是
的变化如图所示,下列叙述正确的是
A.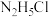 溶液显碱性 溶液显碱性 |
B.当 时,溶液中存在 时,溶液中存在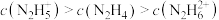 |
C.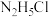 溶液中存在 溶液中存在 |
D.反应 的 的 |
您最近一年使用:0次
7 . 下列物质加入水中后,对水的电离平衡影响不同于其他三种的是
A. 固体 固体 | B. | C. 固体 固体 | D. 固体 固体 |
您最近一年使用:0次
8 . 请回答下列问题:(25℃时,部分物质的电离平衡常数如表所示)
(1)用蒸馏水稀释 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是_______
a.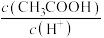 b.
b. c.
c.
(2)在25℃时对氨水进行如下操作,请填写下列空白。
①若向氨水中加入稀硫酸,使氨水恰好被中和,所得溶液的
___________ (填“>”“=”或“<”)7,用离子方程式表示其原因:___________ 。
(3)相同温度下,等pH的 溶液、
溶液、 溶液和
溶液和 溶液,三种溶液的物质的量浓度
溶液,三种溶液的物质的量浓度 、
、 、
、 由大到小排序为
由大到小排序为___________ 。
(4)25℃时 的水解平衡常数Kh=
的水解平衡常数Kh=___________ (结果保留1位有效数字)。
| 化学式 |  |  |  |  |
| 电离平衡常数 |  |  | 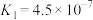  | 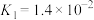 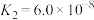 |
 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是a.
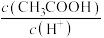 b.
b. c.
c.
(2)在25℃时对氨水进行如下操作,请填写下列空白。
①若向氨水中加入稀硫酸,使氨水恰好被中和,所得溶液的

(3)相同温度下,等pH的
 溶液、
溶液、 溶液和
溶液和 溶液,三种溶液的物质的量浓度
溶液,三种溶液的物质的量浓度 、
、 、
、 由大到小排序为
由大到小排序为(4)25℃时
 的水解平衡常数Kh=
的水解平衡常数Kh=
您最近一年使用:0次
名校
解题方法
9 . 常温下,向30mL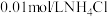 溶液中加入
溶液中加入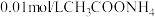 溶液,溶液的pH随加入
溶液,溶液的pH随加入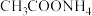 溶液的体积的变化如图。下列说法正确的是
溶液的体积的变化如图。下列说法正确的是

已知: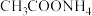 溶液的pH约为7
溶液的pH约为7
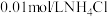 溶液中加入
溶液中加入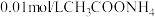 溶液,溶液的pH随加入
溶液,溶液的pH随加入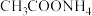 溶液的体积的变化如图。下列说法正确的是
溶液的体积的变化如图。下列说法正确的是
已知:
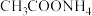 溶液的pH约为7
溶液的pH约为7A.上图说明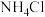 溶液中存在水解平衡 溶液中存在水解平衡 |
B.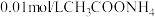 溶液中的 溶液中的 比 比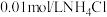 溶液中的大 溶液中的大 |
C.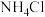 溶液中存在: 溶液中存在: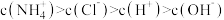 |
D.溶液的pH变化是 浓度改变造成的 浓度改变造成的 |
您最近一年使用:0次
2023-10-04更新
|
179次组卷
|
7卷引用:北京市北京一零一中学2022-2023学年高二上学期期中考试化学试题
解题方法
10 . 常温下,下列有关溶液的说法正确的是
A.浓度相同的①NH4Cl②NH4Al(SO4)2③(NH4)2CO3溶液中 浓度的大小顺序为③>②>① 浓度的大小顺序为③>②>① |
| B.在CH3COOH和CH3COONa浓度相等的混合溶液中(溶液呈酸性):c(CH3COOH)>c(Na+)>c(CH3COO-) |
| C.NaHS溶液加水稀释,c(Na+)与c(HS-)的比值将减小 |
| D.已知在相同条件下Ka(HCOOH)>Ka(CH3COOH),则在HCOONa与CH3COOK浓度相等的混合溶液中存在:c(Na+)-c(HCOO-)>c(K+)-c(CH3COO-) |
您最近一年使用:0次



