名校
1 . 下列有关电解质溶液的说法正确的是
A.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中 减小 减小 |
B.将CH3COONa溶液从20℃升温至30℃,溶液中 增大 增大 |
C.向盐酸中加入氨水至中性,溶液中 >1 >1 |
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中 不变 不变 |
您最近一年使用:0次
2024-01-12更新
|
89次组卷
|
2卷引用:广西南宁市第二中学2022-2023学年高二上学期12月月考化学试卷
2 . 合理应用和处理氮的化合物,在生产、生活中有重要意义。
(1)尿素 [CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:
 。该反应的化学平衡常数的表达式
。该反应的化学平衡常数的表达式
___________ 。关于该反应的下列说法正确的是___________ (填序号)。
a.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b.在平衡体系中增加水的用量可使该反应的平衡常数增大
c.降低温度使尿素的转化率增大
②尿素在一定条件下可将氮的氧化物还原为氮气。密闭容器中以等物质的量的 和
和 为原料,在120℃、催化剂作用下反应生成尿素:
为原料,在120℃、催化剂作用下反应生成尿素: ,混合气体中
,混合气体中 的物质的量百分含量 [
的物质的量百分含量 [ ]随时间变化关系如图所示。则a点的正反应速率
]随时间变化关系如图所示。则a点的正反应速率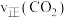
___________ b点的逆反应速率 (填“>”、“=”或“<”);氨气的平衡转化率是
(填“>”、“=”或“<”);氨气的平衡转化率是___________ 。

(2)实验室可用 溶液吸收
溶液吸收 ,反应为
,反应为 。含
。含 的水溶液与
的水溶液与 恰好完全反应得
恰好完全反应得 溶液A,溶液B为
溶液A,溶液B为 的
的 溶液,则两溶液中
溶液,则两溶液中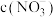 、
、 、和
、和 由大到小的顺序为
由大到小的顺序为___________ 。(已知 的电离常数
的电离常数 ,
, 的电离常数
的电离常数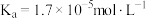 ),可使溶液A和溶液B的
),可使溶液A和溶液B的 相等的方法是
相等的方法是___________ 。
a.向溶液A中加适量水 b.向溶液A中加适量
c.向溶液B中加适量水 d.向溶液B中加适量
(1)尿素 [CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:

 。该反应的化学平衡常数的表达式
。该反应的化学平衡常数的表达式
a.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b.在平衡体系中增加水的用量可使该反应的平衡常数增大
c.降低温度使尿素的转化率增大
②尿素在一定条件下可将氮的氧化物还原为氮气。密闭容器中以等物质的量的
 和
和 为原料,在120℃、催化剂作用下反应生成尿素:
为原料,在120℃、催化剂作用下反应生成尿素: ,混合气体中
,混合气体中 的物质的量百分含量 [
的物质的量百分含量 [ ]随时间变化关系如图所示。则a点的正反应速率
]随时间变化关系如图所示。则a点的正反应速率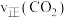
 (填“>”、“=”或“<”);氨气的平衡转化率是
(填“>”、“=”或“<”);氨气的平衡转化率是
(2)实验室可用
 溶液吸收
溶液吸收 ,反应为
,反应为 。含
。含 的水溶液与
的水溶液与 恰好完全反应得
恰好完全反应得 溶液A,溶液B为
溶液A,溶液B为 的
的 溶液,则两溶液中
溶液,则两溶液中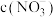 、
、 、和
、和 由大到小的顺序为
由大到小的顺序为 的电离常数
的电离常数 ,
, 的电离常数
的电离常数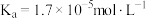 ),可使溶液A和溶液B的
),可使溶液A和溶液B的 相等的方法是
相等的方法是a.向溶液A中加适量水 b.向溶液A中加适量

c.向溶液B中加适量水 d.向溶液B中加适量

您最近一年使用:0次
3 . 电解质在水溶液中存在各种行为,如电离、水解、沉淀溶解等,据所学知识回答下列问题:
(1)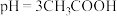 溶液中水电离出来的
溶液中水电离出来的 和溶液中的
和溶液中的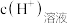 之比是
之比是___________ 。
(2)25℃时,将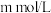 的醋酸和
的醋酸和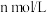 的氢氧化钠溶液等体积混合后,溶液的
的氢氧化钠溶液等体积混合后,溶液的 ,则溶液中
,则溶液中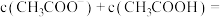
___________ ,m与n的大小关系是m___________ n(填“>”“=”或“<”)。
(3)将 分别放入:①
分别放入:① 水②
水② 溶液③
溶液③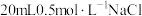 溶液④
溶液④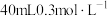 盐酸,各溶液中
盐酸,各溶液中 的浓度由大到小的排列顺序是
的浓度由大到小的排列顺序是___________ (用字母表示)。
(4)氯化铁溶液蒸干并灼烧的产物是___________ ,原因是___________ 。
(5)25℃时,醋酸的电离常数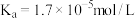 ,则该温度下
,则该温度下 的水解平衡常数
的水解平衡常数
___________  (保留到小数点后一位)。
(保留到小数点后一位)。
(1)
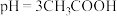 溶液中水电离出来的
溶液中水电离出来的 和溶液中的
和溶液中的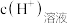 之比是
之比是(2)25℃时,将
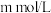 的醋酸和
的醋酸和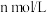 的氢氧化钠溶液等体积混合后,溶液的
的氢氧化钠溶液等体积混合后,溶液的 ,则溶液中
,则溶液中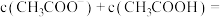
(3)将
 分别放入:①
分别放入:① 水②
水② 溶液③
溶液③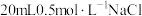 溶液④
溶液④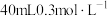 盐酸,各溶液中
盐酸,各溶液中 的浓度由大到小的排列顺序是
的浓度由大到小的排列顺序是(4)氯化铁溶液蒸干并灼烧的产物是
(5)25℃时,醋酸的电离常数
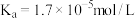 ,则该温度下
,则该温度下 的水解平衡常数
的水解平衡常数
 (保留到小数点后一位)。
(保留到小数点后一位)。
您最近一年使用:0次
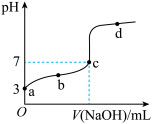
4 . 常温下向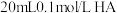 溶液中逐滴加入
溶液中逐滴加入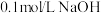 溶液,其
溶液,其 变化曲线如图所示(忽略温度变化)。下列说法中不正确的是
变化曲线如图所示(忽略温度变化)。下列说法中不正确的是
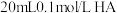 溶液中逐滴加入
溶液中逐滴加入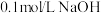 溶液,其
溶液,其 变化曲线如图所示(忽略温度变化)。下列说法中不正确的是
变化曲线如图所示(忽略温度变化)。下列说法中不正确的是
A.由题可知 为弱酸 为弱酸 |
| B.c点时,酸过量 |
C.滴定到b点时, |
D.滴定到d点时,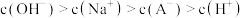 |
您最近一年使用:0次
解题方法
5 . 下列说法正确的是
A.室温下,向 的稀氨水中加入 的稀氨水中加入 氢氧化钠溶液, 氢氧化钠溶液, 的电离平衡不移动 的电离平衡不移动 |
B.浓度为   溶液,升高温度, 溶液,升高温度, 不变,但醋酸的电离程度增大 不变,但醋酸的电离程度增大 |
C.用等浓度的 溶液分别中和等 溶液分别中和等 值的 值的 、 、 溶液, 溶液, 消耗的 消耗的 体积大,说明酸性 体积大,说明酸性 |
D.室温下, 的盐酸与 的盐酸与 的氨水等体积混合后 的氨水等体积混合后 |
您最近一年使用:0次
名校
解题方法
6 . 南宁三中化学小组设计了如图所示的数字化实验装置,研究常温下,向30mL0.1mol/LH2A溶液中逐滴加入等浓度NaOH溶液时pH的变化情况,并绘制出溶液中含A元素的微粒的物质的量分数与溶液pH的关系(如图所示),下列说法错误的是


| A.pH=4.0时,溶液中n(HA-)约为2.73×10-4mol |
| B.滴定时,应将左边的酸式滴定管换成右边的碱式滴定管 |
| C.常温下,Na2A的水解常数为10-11 |
| D.0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)<0.1mol/L |
您最近一年使用:0次
2023-06-21更新
|
94次组卷
|
2卷引用:广西 南宁市第三中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
7 . 常温下,向0.1mol/L的HR溶液中逐滴滴入0.1mol/L的c(NH3•H2O)溶液,所得溶液pH及导电性变化如图所示。下列分析错误的是


| A.a~b点导电能力增强说明HR为弱酸 |
| B.a~c点,溶液中离子数目先增大再减小 |
C.b点溶液pH=7。说明c(NH )=c(R-) )=c(R-) |
| D.水的电离程度:b>c |
您最近一年使用:0次
名校
解题方法
8 . 常温下,下列溶液中微粒的物质的量浓度关系正确的是
| A.pH=8的CH3COONa溶液和pH=8的NaOH溶液,由水电离产生的OH-浓度相等 |
| B.0.01mol/LNaOH溶液与等体积pH=2醋酸混合后的溶液:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C.0.2mol/LNH3•H2O溶液与0.1mol/LHCl溶液等体积混合:c(Cl-)+c(H+)>c(NH3•H2O)+c(OH-) |
D.向氨水中加入氯化铵固体,溶液中 比值变小 比值变小 |
您最近一年使用:0次
名校
解题方法
9 . 以下说法正确的是
A.醋酸溶液中,适当加热或加水,均能使溶液中 增大 增大 |
| B.向水中通入氨气,水的电离平衡逆向移动,溶液中c(OH-)减小 |
C.向Na2S溶液中通入适量的Cl2,可使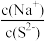 减小 减小 |
| D.常温下,已知Ka(HF)>Ka(HCN),则同浓度的NaF溶液的pH比NaCN溶液的大 |
您最近一年使用:0次
名校
10 . 下列离子方程式书写正确的是
A.K2HPO4溶液呈弱碱性的主要原因:HPO +H2O +H2O H3O++PO H3O++PO |
B.向NH4HCO3溶液加入过量NaOH溶液:HCO +OH-=CO +OH-=CO +H2O +H2O |
C.在NaAlO2溶液中滴入足量Ca(HCO3)2溶液:AlO +HCO +HCO +H2O+Ca2+=Al(OH)3↓+CaCO3↓ +H2O+Ca2+=Al(OH)3↓+CaCO3↓ |
D.在10mL0.1mol/L(NH4)2Fe(SO4)2溶液中滴加10mL0.1mol/L的Ba(OH)2溶液:2NH +SO +SO +Ba2++2OH-═BaSO4↓+2NH3+H2O +Ba2++2OH-═BaSO4↓+2NH3+H2O |
您最近一年使用:0次



