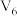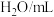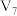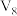名校
1 . 有A、B、C、D四种强电解质 ,它们在水中电离产生下列离子(每种物质只含一种阴离子且互不重复).
已知:①A、C溶液的 均大于7,四种物质的溶液中只有A、B的溶液中水的电离程度均大于纯水的电离程度;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无现象.
均大于7,四种物质的溶液中只有A、B的溶液中水的电离程度均大于纯水的电离程度;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无现象.
(1)A是___________ ,B是___________ (填化学式).
(2)写出C和D反应的离子方程式____________________________________ .
(3)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是_______________________________________________ .
阳离子 |
|
阴离子 |
|
 均大于7,四种物质的溶液中只有A、B的溶液中水的电离程度均大于纯水的电离程度;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无现象.
均大于7,四种物质的溶液中只有A、B的溶液中水的电离程度均大于纯水的电离程度;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无现象.(1)A是
(2)写出C和D反应的离子方程式
(3)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是
您最近一年使用:0次
名校
2 . 回答下列问题
(1)纯水在 时,
时, ,在此温度下,将
,在此温度下,将 的氢氧化钠溶液
的氢氧化钠溶液 与
与 的硫酸溶液
的硫酸溶液 混合(设混合后溶液体积为原两溶液体积之和)所得溶液的
混合(设混合后溶液体积为原两溶液体积之和)所得溶液的 ,则
,则
___________ .
(2)若某溶液中只存在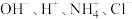 四种离子,且
四种离子,且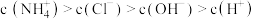 ,该溶液的溶质是
,该溶液的溶质是___________ .
(3)某同学在稀硫酸与锌反应制取氢气的实验中发现加入少量硫酸铜溶液可加快该反应中氢气的生成速率.为了进一步研究所加硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量 粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间.
粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间.
请完成此实验设计,其中
___________ ,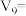
___________ .
(4)常温下,用 溶液作
溶液作 捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品
捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品 .若某次捕捉后得到
.若某次捕捉后得到 的溶液,则溶液中
的溶液,则溶液中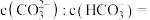
___________ [常温下,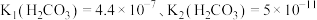 ].
].
(5)常温下,将 的醋酸与
的醋酸与 溶液等体积混合,充分反应后,溶液中存在
溶液等体积混合,充分反应后,溶液中存在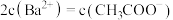 ,则该混合溶液中醋酸的电离常数
,则该混合溶液中醋酸的电离常数
___________ (用含a和b的代数式表示)
(1)纯水在
 时,
时, ,在此温度下,将
,在此温度下,将 的氢氧化钠溶液
的氢氧化钠溶液 与
与 的硫酸溶液
的硫酸溶液 混合(设混合后溶液体积为原两溶液体积之和)所得溶液的
混合(设混合后溶液体积为原两溶液体积之和)所得溶液的 ,则
,则
(2)若某溶液中只存在
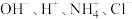 四种离子,且
四种离子,且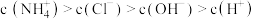 ,该溶液的溶质是
,该溶液的溶质是(3)某同学在稀硫酸与锌反应制取氢气的实验中发现加入少量硫酸铜溶液可加快该反应中氢气的生成速率.为了进一步研究所加硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量
 粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间.
粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间.混合溶液组成 | A | B | C | D | E | F |
| 30 |
|
|
|
|
|
饱和 | 0 | 0.5 | 2.5 | 5 |
| 20 |
|
|
|
|
| 10 | 0 |

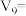
(4)常温下,用
 溶液作
溶液作 捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品
捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品 .若某次捕捉后得到
.若某次捕捉后得到 的溶液,则溶液中
的溶液,则溶液中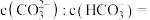
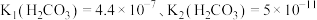 ].
].(5)常温下,将
 的醋酸与
的醋酸与 溶液等体积混合,充分反应后,溶液中存在
溶液等体积混合,充分反应后,溶液中存在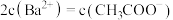 ,则该混合溶液中醋酸的电离常数
,则该混合溶液中醋酸的电离常数
您最近一年使用:0次
名校
3 . 下列说法正确的是
A. 时, 时, 为9的 为9的 溶液和 溶液和 为5的 为5的 溶液中,水的电离程度不同 溶液中,水的电离程度不同 |
B.测定中和热实验中,用氨水代替 溶液做实验,所得反应热偏低 溶液做实验,所得反应热偏低 |
C. 时,等体积等物质的量浓度的 时,等体积等物质的量浓度的 和 和 溶液中所含离子总数前者大 溶液中所含离子总数前者大 |
D. 溶液与 溶液与 氨水等体积混合: 氨水等体积混合: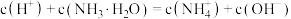 |
您最近一年使用:0次
名校
解题方法
4 . 下列实验操作能够达到预期目的的是
A.用 试纸测定某浓度 试纸测定某浓度 溶液的 溶液的 为4 为4 |
B.加热 能得到纯净的无水氯化镁 能得到纯净的无水氯化镁 |
| C.增大压强,可以提高单位体积内活化分子的百分数,从而提高化学反应速率 |
D.中和 与体积均相同的 与体积均相同的 和氨水,消耗 和氨水,消耗 的量前者小于后者 的量前者小于后者 |
您最近一年使用:0次
名校
5 . 为了测定含有 、
、 和
和 的试样中各物质的质量分数,进行如下实验
的试样中各物质的质量分数,进行如下实验
①称取 试样,加水溶解,配成
试样,加水溶解,配成 试样溶液.
试样溶液.
②用酸式滴定管量取 试样溶液放入锥形瓶中,并加入
试样溶液放入锥形瓶中,并加入 滴酚酞试液,用
滴酚酞试液,用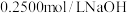 溶液滴定,消耗
溶液滴定,消耗 溶液
溶液 .
.
③再取 试样溶液放入另一锥形瓶中,用
试样溶液放入另一锥形瓶中,用 的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液
的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液 .已知:
.已知: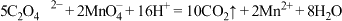
(1)已知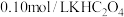 溶液
溶液 约为3,其中含碳元素的粒子浓度由大到小的顺序为
约为3,其中含碳元素的粒子浓度由大到小的顺序为___________ .
(2)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的 的质量分数
的质量分数___________ .(填“偏大”、“偏小”或“无影响”)
(3)步骤③中判断滴定终点的方法是___________________________________________________
(4)原试样中 的质量分数为
的质量分数为___________ , 的质量分数为
的质量分数为___________ .
 、
、 和
和 的试样中各物质的质量分数,进行如下实验
的试样中各物质的质量分数,进行如下实验①称取
 试样,加水溶解,配成
试样,加水溶解,配成 试样溶液.
试样溶液.②用酸式滴定管量取
 试样溶液放入锥形瓶中,并加入
试样溶液放入锥形瓶中,并加入 滴酚酞试液,用
滴酚酞试液,用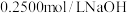 溶液滴定,消耗
溶液滴定,消耗 溶液
溶液 .
.③再取
 试样溶液放入另一锥形瓶中,用
试样溶液放入另一锥形瓶中,用 的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液
的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液 .已知:
.已知: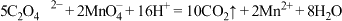
(1)已知
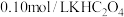 溶液
溶液 约为3,其中含碳元素的粒子浓度由大到小的顺序为
约为3,其中含碳元素的粒子浓度由大到小的顺序为(2)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的
 的质量分数
的质量分数(3)步骤③中判断滴定终点的方法是
(4)原试样中
 的质量分数为
的质量分数为 的质量分数为
的质量分数为
您最近一年使用:0次
名校
6 . 电解质溶液的电导率越大,导电能力越强.现用 的
的 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和
的盐酸和 溶液,利用传感器测得滴定过程中溶液的电导率如图所示.下列说法不正确的是
溶液,利用传感器测得滴定过程中溶液的电导率如图所示.下列说法不正确的是
 的
的 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和
的盐酸和 溶液,利用传感器测得滴定过程中溶液的电导率如图所示.下列说法不正确的是
溶液,利用传感器测得滴定过程中溶液的电导率如图所示.下列说法不正确的是
A.曲线①代表滴定 溶液的曲线 溶液的曲线 |
B.A点溶液中: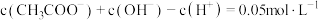 |
C.在相同温度下,A、B、C三点溶液中水电离的 |
D.D点溶液中: |
您最近一年使用:0次
2024-01-16更新
|
58次组卷
|
2卷引用:河南省济源第一中学2022-2023学年高二上学期11月月考 化学试题
名校
7 . NaOH溶液可用于多种气体的处理。
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3。
①Na2CO3俗称纯碱,因CO 水解而使其水溶液呈碱性,写出CO
水解而使其水溶液呈碱性,写出CO 水解的离子方程式:
水解的离子方程式:_______ 。写出等浓度的Na2CO3和NaHCO3的混合溶液中各离子浓度大小关系为______ 。已知25℃时,CO 的水解平衡常数Kh=2×10-4mol/L,当溶液中c(HCO
的水解平衡常数Kh=2×10-4mol/L,当溶液中c(HCO ):c(CO
):c(CO )=20:1时,溶液的pH=
)=20:1时,溶液的pH=_______ 。
②泡沫灭火器中通常装有NaHCO3溶液和Al2(SO4)3溶液,请写出这两种溶液混合时反应的离子方程式:_______ 。
(2)烟气中的SO2可引起酸雨,可利用氢氧化钠溶液吸收。吸收SO2的过程中,溶液中H2SO3、HSO 、SO
、SO 三者所占物质的量分数(a)随pH变化的关系如图所示。
三者所占物质的量分数(a)随pH变化的关系如图所示。

①由图可知H2SO3第一级电离平衡常数Ka1=________ 。
②当用含3molNaOH的溶液吸收标准状况下的44.8LSO2时,写出该混合液的物料守恒表达式:_________ 。
③图中pH=7时,溶液中离子浓度关系正确的是_______ 。
A.c(Na+)>2c(SO )>c(HSO
)>c(HSO )
)
B.c(Na+)=c(SO )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)
C.c(OH-)=c(H+)+c(H2SO3)+c(HSO )
)
D.c(Na+)>c(HSO )>c(SO
)>c(SO )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3。
①Na2CO3俗称纯碱,因CO
 水解而使其水溶液呈碱性,写出CO
水解而使其水溶液呈碱性,写出CO 水解的离子方程式:
水解的离子方程式: 的水解平衡常数Kh=2×10-4mol/L,当溶液中c(HCO
的水解平衡常数Kh=2×10-4mol/L,当溶液中c(HCO ):c(CO
):c(CO )=20:1时,溶液的pH=
)=20:1时,溶液的pH=②泡沫灭火器中通常装有NaHCO3溶液和Al2(SO4)3溶液,请写出这两种溶液混合时反应的离子方程式:
(2)烟气中的SO2可引起酸雨,可利用氢氧化钠溶液吸收。吸收SO2的过程中,溶液中H2SO3、HSO
 、SO
、SO 三者所占物质的量分数(a)随pH变化的关系如图所示。
三者所占物质的量分数(a)随pH变化的关系如图所示。
①由图可知H2SO3第一级电离平衡常数Ka1=
②当用含3molNaOH的溶液吸收标准状况下的44.8LSO2时,写出该混合液的物料守恒表达式:
③图中pH=7时,溶液中离子浓度关系正确的是
A.c(Na+)>2c(SO
 )>c(HSO
)>c(HSO )
)B.c(Na+)=c(SO
 )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)C.c(OH-)=c(H+)+c(H2SO3)+c(HSO
 )
)D.c(Na+)>c(HSO
 )>c(SO
)>c(SO )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
您最近一年使用:0次
名校
8 . 现有常温下的4种溶液:①0.01mol/LCH3COOH溶液,②0.01mol/LHCl溶液,③pH=12的氨水,④pH=12的NaOH溶液。回答下列问题:
(1)4种溶液中水的电离程度最大的是________ (填序号)。
(2)将4种溶液同等程度稀释10倍后,溶液pH由大到小的顺序是________ 。
(3)若将①④混合后所得溶液中的c(CH3COO-)>c(H+),则下列说法正确的是________ 。
(4)若将②③混合后所得溶液的pH=7,则消耗溶液的体积:②________ ③(填">"“<"或"=")。
(5)若将②④混合后所得溶液的pH=10,则消耗②和④溶液的体积比: =
=_______ 。
(6)室温下pH=9的NaOH溶液和pH=9的CH3COONa溶液,设由水电离产生的OH-的物质的量浓度分别为c(A)和c(B),则c(A):c(B)=_________ 。
(7)若氨水与SO2恰好生成正盐,则此时溶液呈________ (填"酸性"或“碱性"),向上述溶液中通入________ (填"NH3"或"SO2")可使溶液呈中性,此时溶液中
________ 2(填“>”“<”或“=“)。
(已知常温下NH3·H2O的Kb=1.8×10-5mol/L,H2SO3的Ka1=1.5×10-2mol/L,Ka2=6.3×10-8mol/L)
(1)4种溶液中水的电离程度最大的是
(2)将4种溶液同等程度稀释10倍后,溶液pH由大到小的顺序是
(3)若将①④混合后所得溶液中的c(CH3COO-)>c(H+),则下列说法正确的是
| A.溶液一定呈酸性 | B.溶液一定呈碱性。 |
| C.溶液一定呈中性 | D.溶液可能呈酸性、中性或碱性 |
(5)若将②④混合后所得溶液的pH=10,则消耗②和④溶液的体积比:
 =
=(6)室温下pH=9的NaOH溶液和pH=9的CH3COONa溶液,设由水电离产生的OH-的物质的量浓度分别为c(A)和c(B),则c(A):c(B)=
(7)若氨水与SO2恰好生成正盐,则此时溶液呈

(已知常温下NH3·H2O的Kb=1.8×10-5mol/L,H2SO3的Ka1=1.5×10-2mol/L,Ka2=6.3×10-8mol/L)
您最近一年使用:0次
名校
9 . 某一元弱酸HA在水中的电离方程式是HA H++A-,回答下列问题:
H++A-,回答下列问题:
(1)向纯水中加入适量HA,水的电离平衡将向______ (填“正”、"逆")反应方向移动。
(2)若向(1)所得溶液中加入适量NaCl溶液,以上平衡将向________ (填"正"、"逆")反应方向移动,溶液中c(A-)将________ (填"增大"、"减小"或"不变"),溶液中c(OH-)将________ (填“增大”、“减小”或“不变”)。
(3)在25℃下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应平衡时溶液中c(NH )=c(Cl-),则溶液显
)=c(Cl-),则溶液显_______ 性(填"酸"、"碱"或"中"),a________ 0.01(填">"、"="或"<"),用含a的代数式表示NH3•H2O的电离常数Kb=________ 。
(4)常温时,取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8。试回答以下问题:
①混合溶液的pH=8的原因是_______ (用离子方程式表示)。
②求出混合液中下列算式的精确计算结果(填具体数字,用科学计数法保留两位有效数字):c(Na+)-c(A-)=_______ mol/L;c(OH-)-c(HA)=________ mol/L。
 H++A-,回答下列问题:
H++A-,回答下列问题:(1)向纯水中加入适量HA,水的电离平衡将向
(2)若向(1)所得溶液中加入适量NaCl溶液,以上平衡将向
(3)在25℃下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应平衡时溶液中c(NH
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显(4)常温时,取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8。试回答以下问题:
①混合溶液的pH=8的原因是
②求出混合液中下列算式的精确计算结果(填具体数字,用科学计数法保留两位有效数字):c(Na+)-c(A-)=
您最近一年使用:0次
名校
10 . 下列化学用语表示正确的是
| A.HF在水溶液中电离:HF=H++F- |
B.Na2S在水溶液中水解:S2-+H2O HS-+OH- HS-+OH- |
C.BaSO4在水溶液中电离:BaSO4 Ba2++SO Ba2++SO |
D.弱酸的酸式盐NaHB在水溶液中水解:HB-+H2O H3O++B2- H3O++B2- |
您最近一年使用:0次

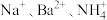
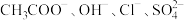
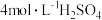 溶液/
溶液/




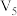
 溶液/
溶液/