名校
解题方法
1 . “吃饺子要蘸醋”是很多中国人传统的饮食习惯,我们对醋酸的使用有着悠久的历史。
(1) 的醋酸和盐酸各
的醋酸和盐酸各 分别稀释至
分别稀释至 ,所得醋酸的
,所得醋酸的
_______ (填“>”“<”或“=”)所得盐酸的 。
。
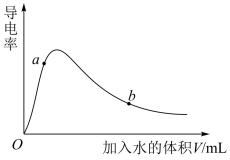
(2)取 冰醋酸作导电性实验,测得其导电率随加入水的量的变化如图所示。
冰醋酸作导电性实验,测得其导电率随加入水的量的变化如图所示。
①由水电离出的氢离子 :a
:a_______ b(填“>”“<”或“=”)。
②使图中b点对应的溶液中 增大、
增大、 减小,可采用的方法是
减小,可采用的方法是_______ (填标号)。
A.加入 B.加入
B.加入 固体 C.加入浓硫酸 D.加入
固体 C.加入浓硫酸 D.加入 固体
固体
(3)向面食中加入适量的醋可以中和其中过量的食用碱而改善口感,已知 时,三种弱酸的电离平衡常数如下表,写出过量醋酸与
时,三种弱酸的电离平衡常数如下表,写出过量醋酸与 溶液反应的离子方程式:
溶液反应的离子方程式:_______ ;判断 结合质子能力由大到小顺序为
结合质子能力由大到小顺序为_______ 。
(4)吃醋虽好但不宜过量,不然容易造成牙齿酸软,甚至引发龋齿,牙齿的主要成分是羟基磷灰石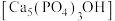 ,市面上含氟牙膏常添加了
,市面上含氟牙膏常添加了 来预防龋齿,请结合化学用语解释含氟牙膏预防龋齿的原因:
来预防龋齿,请结合化学用语解释含氟牙膏预防龋齿的原因:_______ [已知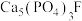 难溶于酸]。
难溶于酸]。
(5)常温下,某同学取 物质的量浓度为
物质的量浓度为 的醋酸,向其中滴入
的醋酸,向其中滴入
 溶液,当滴入的
溶液,当滴入的 溶液的体积为
溶液的体积为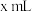 ,溶液呈中性,则醋酸的电离平衡常数
,溶液呈中性,则醋酸的电离平衡常数
_______ (用含x的代数式表示)。

(1)
 的醋酸和盐酸各
的醋酸和盐酸各 分别稀释至
分别稀释至 ,所得醋酸的
,所得醋酸的
 。
。(2)取
 冰醋酸作导电性实验,测得其导电率随加入水的量的变化如图所示。
冰醋酸作导电性实验,测得其导电率随加入水的量的变化如图所示。①由水电离出的氢离子
 :a
:a②使图中b点对应的溶液中
 增大、
增大、 减小,可采用的方法是
减小,可采用的方法是A.加入
 B.加入
B.加入 固体 C.加入浓硫酸 D.加入
固体 C.加入浓硫酸 D.加入 固体
固体(3)向面食中加入适量的醋可以中和其中过量的食用碱而改善口感,已知
 时,三种弱酸的电离平衡常数如下表,写出过量醋酸与
时,三种弱酸的电离平衡常数如下表,写出过量醋酸与 溶液反应的离子方程式:
溶液反应的离子方程式: 结合质子能力由大到小顺序为
结合质子能力由大到小顺序为| 弱酸 |  |  |  |
| 电离平衡常数 | 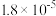 | 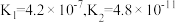 | 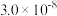 |
(4)吃醋虽好但不宜过量,不然容易造成牙齿酸软,甚至引发龋齿,牙齿的主要成分是羟基磷灰石
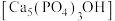 ,市面上含氟牙膏常添加了
,市面上含氟牙膏常添加了 来预防龋齿,请结合化学用语解释含氟牙膏预防龋齿的原因:
来预防龋齿,请结合化学用语解释含氟牙膏预防龋齿的原因: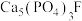 难溶于酸]。
难溶于酸]。(5)常温下,某同学取
 物质的量浓度为
物质的量浓度为 的醋酸,向其中滴入
的醋酸,向其中滴入
 溶液,当滴入的
溶液,当滴入的 溶液的体积为
溶液的体积为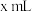 ,溶液呈中性,则醋酸的电离平衡常数
,溶液呈中性,则醋酸的电离平衡常数
您最近一年使用:0次
2024-02-26更新
|
125次组卷
|
2卷引用:云南省大理州民族中学2023-2024学年高二下学期见面考化学试题
2 . 氧化铍(BeO) 广泛用于原子能、宇航等领域。一种以铍矿石 (主要成分为Be2SiO4,少量MnO等)为原料提取氧化铍的工艺流程如图所示。
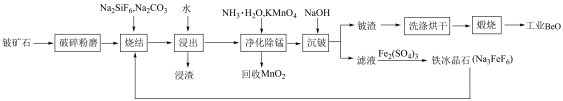
已知:烧结时,未发生氧化还原反应:烧结后,Be、Mn元素以可溶性的Na2BeF4、Na2MnF4形式存在,其余元素以稳定氧化物的形式存在。
回答下列问题:
(1)“烧结”前,将铍矿石“破碎粉磨”的目的是______ 。
(2)“浸渣”的成分为_____ (填化学式)。
(3)“净化除锰”步骤的离子反应方程式为_____________ 。
(4)“沉铍”时,先加入足量NaOH溶液,得到含铍粒子是________ (填粒子符号), 再加热煮沸,调节pH=11,得到颗粒状Be(OH)2。从化学平衡移动的角度解释上述反应原理__________ 。
(5)铁冰晶石(Na3FeF6) 晶体中存在的作用力有__________ ,Fe'+ 的杂化方式是____ (填标号)。
A.dsp2 B.sp3d2 C.sp2 D.sp3

已知:烧结时,未发生氧化还原反应:烧结后,Be、Mn元素以可溶性的Na2BeF4、Na2MnF4形式存在,其余元素以稳定氧化物的形式存在。
回答下列问题:
(1)“烧结”前,将铍矿石“破碎粉磨”的目的是
(2)“浸渣”的成分为
(3)“净化除锰”步骤的离子反应方程式为
(4)“沉铍”时,先加入足量NaOH溶液,得到含铍粒子是
(5)铁冰晶石(Na3FeF6) 晶体中存在的作用力有
A.dsp2 B.sp3d2 C.sp2 D.sp3
您最近一年使用:0次
名校
3 . 电子工业中,常用FeCl3溶液作为印刷电路铜板蚀刻液。请按要求回答下列问题:
(1)若向FeCl3溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该反应的离子方程式为___________ ,该过程中调节溶液的pH为5,则c(Fe3+)=___________ mol·L-1。(已知:Ksp[Fe(OH)3]=2.8×10-39)
(2)某探究小组设计如图所示线路处理废液和资源回收:

①用足量FeCl3溶液蚀刻铜板后的废液中含有的金属阳离子有___________ 。
②FeCl3蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是___________ 。
③步骤①中加入H2O2溶液的目的是___________ 。
④已知:生成氢氧化物沉淀时溶液的pH如表所示:
根据表中数据推测调节溶液pH的范围是___________ 。
⑤写出步骤②中生成CO2的离子方程式:___________ [已知Cu2(OH)2CO3难溶于水]。
(1)若向FeCl3溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该反应的离子方程式为
(2)某探究小组设计如图所示线路处理废液和资源回收:

①用足量FeCl3溶液蚀刻铜板后的废液中含有的金属阳离子有
②FeCl3蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是
③步骤①中加入H2O2溶液的目的是
④已知:生成氢氧化物沉淀时溶液的pH如表所示:
| Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 4.7 | 7.0 | 1.9 |
| 沉淀完全时 | 6.7 | 9.0 | 3.2 |
根据表中数据推测调节溶液pH的范围是
⑤写出步骤②中生成CO2的离子方程式:
您最近一年使用:0次
名校
4 . 氮氧化铝(AlON)具有多晶陶瓷在材料制备方面的优势,有着广阔的应用前景。工业上利用某铝土矿(含Al2O3及少量的MgO等杂质)生产氮氧化铝的流程如图所示。回答下列问题:
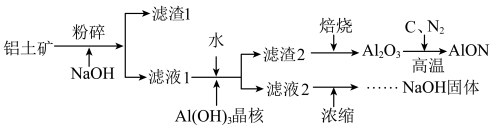
(1)为提高铝土矿碱浸的速率,除粉碎外,还可以采取的措施是_____ (写出一项即可)
(2)滤液1的溶质有NaOH、_____ 。滤渣2的成分是_____ 。向滤液1中加水的目的是_______ 。该过程也可用通入足量的_____ 气体的方法来代替。
(3)滤液2浓缩的过程中常会吸收空气中的CO2,为得到纯净的NaOH,需要加入适量____ (填化学式)。整个流程中,可循环的物质是_____ 。
(4)写出制备AlON的化学方程式_______ 。
(5)取1吨Al2O3质量分数为91.8%的铝土矿样品,利用上述流程AlON,最终制得氮氧化铝820.8kg,则氮氧化铝的产率为______ 。

(1)为提高铝土矿碱浸的速率,除粉碎外,还可以采取的措施是
(2)滤液1的溶质有NaOH、
(3)滤液2浓缩的过程中常会吸收空气中的CO2,为得到纯净的NaOH,需要加入适量
(4)写出制备AlON的化学方程式
(5)取1吨Al2O3质量分数为91.8%的铝土矿样品,利用上述流程AlON,最终制得氮氧化铝820.8kg,则氮氧化铝的产率为
您最近一年使用:0次
2019-09-24更新
|
267次组卷
|
2卷引用:云南省云南师范大学附属中学2019-2020学年高三上学期第二次月考理科综合化学试题
名校
解题方法
5 . 钛矿工业中的硫酸酸性废水富含Ti、Fe等元素,其综合利用如下:
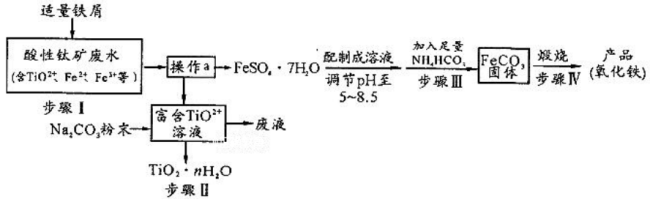
已知:TiO2+易水解,只能存在于强酸性溶液中。
(1)TiO2+钛的化合价为________________________ 。
(2)步骤Ⅰ中检验钛矿废水中加入铁屑是否足量的试剂是________________________ 。
(3)操作a是蒸发浓缩、冷却结晶、______________________________________________ 。
(4)步骤Ⅲ中发生反应的化学方程式为________________________ ;反应温度一般需控制在35℃以下,其目的是____________________________________ 。
(5)已知Ksp=[Fe(OH)2] = 8×10-16。步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5, c(Fe2+) = 1×10-6mol/L。试判断所得的FeCO3中________ (填“有”或“没有”)Fe(OH)2;步骤Ⅳ中,为了得到较为纯净的Fe2O3,除了适当的温度外,还需要采取的措施是_________________ 。
(6)向“富含TiO2+溶液”中加入Na2CO3粉末易得到固体TiO2• nH2O。请结合原理和化学用语解释其原因_________________________________ 。

已知:TiO2+易水解,只能存在于强酸性溶液中。
(1)TiO2+钛的化合价为
(2)步骤Ⅰ中检验钛矿废水中加入铁屑是否足量的试剂是
(3)操作a是蒸发浓缩、冷却结晶、
(4)步骤Ⅲ中发生反应的化学方程式为
(5)已知Ksp=[Fe(OH)2] = 8×10-16。步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5, c(Fe2+) = 1×10-6mol/L。试判断所得的FeCO3中
(6)向“富含TiO2+溶液”中加入Na2CO3粉末易得到固体TiO2• nH2O。请结合原理和化学用语解释其原因
您最近一年使用:0次
2019-01-10更新
|
309次组卷
|
3卷引用:云南省曲靖市会泽县第一中学2019-2020学年高二上学期第一次段考化学试题
名校
6 . 某小组同学设计如下实验,研究亚铁盐与H2O2溶液的反应。
【实验I】试剂:酸化的0.5mol·L-1 FeSO4溶液(pH =0.2),5%H2O2溶液(pH=5)。
(1)上述实验中H2O2溶液与FeSO4溶液反应的离子方程式是________________________ 。
(2)产生气泡的原因是______________________ 。
【实验Ⅱ】试剂:未酸化的0.5mol·L-1FeSO4溶液(pH=3),5% H2O2溶液(pH=5)
(3)将上述混合物分离,得到棕黄色沉淀和红褐色胶体。取部分棕黄色沉淀洗净,加4 mol·L-1盐酸,沉淀溶解得到黄色溶液。初步判断该沉淀中含有Fe2O3,经检验还含有SO42-。检验棕黄色沉淀中SO42-的方法是_______________ 。
(4)对于生成红褐色胶体的原因,提出两种假设:
ⅰ.H2O2溶液氧化Fe2+消耗H+
ii.Fe2+氧化的产物发生了水解
①根据实验Ⅱ记录否定假设ⅰ,理由是____________________ 。
②实验验证假设ⅱ: 取__________ 溶液,加热,溶液变为红褐色,pH下降,证明假设ii成立。
(5)将FeSO4溶液加入H2O2溶液后,产生红褐色胶体,反应的离子方程式是_________________ 。
【实验Ⅲ】若用FeCl2溶液替代FeSO4溶液,其余操作与实验Ⅱ相同,除了产生与Ⅱ相同的现象外,还生成刺激性气味气体,该气体能使湿润的蓝色石蕊试纸变红但不褪色。
(6)产生刺激性气味气体的原因是___________________ 。
(7)由实验I、Ⅱ、Ⅲ可知,亚铁盐与H2O2反应的现象与______________ (至少写两点)有关。
【实验I】试剂:酸化的0.5mol·L-1 FeSO4溶液(pH =0.2),5%H2O2溶液(pH=5)。
| 操作 | 现象 |
| 取2mL上述FeSO4溶液于试管中,加入5滴5%H2O2溶液 | 溶液立即变为棕黄色,稍后,产生气泡。测得反应后溶液pH = 0.9 |
| 向反应后的溶液中加入KSCN溶液 | 溶液变红 |
(2)产生气泡的原因是
【实验Ⅱ】试剂:未酸化的0.5mol·L-1FeSO4溶液(pH=3),5% H2O2溶液(pH=5)
| 操作 | 现象 |
| 取2mL5%H2O2溶液于试管中, 加入5滴上述FeSO4溶液, | 溶液立即变为棕黄色,产生大量气泡,并放热,反应混合物颜色加深且有浑浊。测得反应后溶液pH =1.4 |
(4)对于生成红褐色胶体的原因,提出两种假设:
ⅰ.H2O2溶液氧化Fe2+消耗H+
ii.Fe2+氧化的产物发生了水解
①根据实验Ⅱ记录否定假设ⅰ,理由是
②实验验证假设ⅱ: 取
(5)将FeSO4溶液加入H2O2溶液后,产生红褐色胶体,反应的离子方程式是
【实验Ⅲ】若用FeCl2溶液替代FeSO4溶液,其余操作与实验Ⅱ相同,除了产生与Ⅱ相同的现象外,还生成刺激性气味气体,该气体能使湿润的蓝色石蕊试纸变红但不褪色。
(6)产生刺激性气味气体的原因是
(7)由实验I、Ⅱ、Ⅲ可知,亚铁盐与H2O2反应的现象与
您最近一年使用:0次
2017-06-05更新
|
724次组卷
|
6卷引用:云南省峨山彝族自治县第一中学2018届高三第四次模拟考试化学试题
7 . 钴及其化合物在工业中运用广泛,从某工业废料中制备草酸钴的工业流程如图:

已知:①废料中主要含有三氧化二钴。含少量Fe2O3、Al2O3、MnO、CaO、SiO2等;
②浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)在浸出过程中加入Co2O3与盐酸反应生成气体,此反应的离子方程式为___________________ ;实验室中检验该气体的方法是________________ 。
(2)加入试剂A的目的是_________________ ,废渣的主要成分是_______________ ,在浸出液中先加入双氧水反应,再加入碳酸钠的原因是(试用离子方程式和必要的文字简述其理)___________ 。
(3)萃取后余液中加入(NH4)2C2O4沉淀Co2+,判断Co2+沉淀完全的操作是____________________ 。
(4)萃取剂对金属离子的萃取率与pH的关系如下图所示,在滤液II中适宜萃取的pH为_____ (填序号)

A.接近2.0 B.接近3.0 C.接近5.0
(5)在空气中加热CoC2O4固体,经测定,210℃~290℃的过程中只产生CO2和一种化合物,该化合物中钴元素的质量分数为73.44%。此过程发生反应的化学方程式是________________________ 。

已知:①废料中主要含有三氧化二钴。含少量Fe2O3、Al2O3、MnO、CaO、SiO2等;
②浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(2)加入试剂A的目的是
(3)萃取后余液中加入(NH4)2C2O4沉淀Co2+,判断Co2+沉淀完全的操作是
(4)萃取剂对金属离子的萃取率与pH的关系如下图所示,在滤液II中适宜萃取的pH为

A.接近2.0 B.接近3.0 C.接近5.0
(5)在空气中加热CoC2O4固体,经测定,210℃~290℃的过程中只产生CO2和一种化合物,该化合物中钴元素的质量分数为73.44%。此过程发生反应的化学方程式是
您最近一年使用:0次



