名校
1 . 在日常生产生活中,经常涉及化学反应原理,下列过程或现象与盐类水解无关的是
| A.加热氯化铁溶液,颜色变深 |
B. 与 与 溶液可用作焊接金属时的除锈剂 溶液可用作焊接金属时的除锈剂 |
| C.氯化钙溶液中滴加甲基橙,溶液显黄色 |
D.实验室中盛放 溶液的试剂瓶不能用磨口玻璃塞 溶液的试剂瓶不能用磨口玻璃塞 |
您最近半年使用:0次
2024-03-09更新
|
176次组卷
|
2卷引用:云南省昆明市云南师范大学实验中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
2 . “吃饺子要蘸醋”是很多中国人传统的饮食习惯,我们对醋酸的使用有着悠久的历史。
(1) 的醋酸和盐酸各
的醋酸和盐酸各 分别稀释至
分别稀释至 ,所得醋酸的
,所得醋酸的
_______ (填“>”“<”或“=”)所得盐酸的 。
。
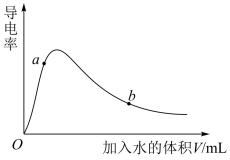
(2)取 冰醋酸作导电性实验,测得其导电率随加入水的量的变化如图所示。
冰醋酸作导电性实验,测得其导电率随加入水的量的变化如图所示。
①由水电离出的氢离子 :a
:a_______ b(填“>”“<”或“=”)。
②使图中b点对应的溶液中 增大、
增大、 减小,可采用的方法是
减小,可采用的方法是_______ (填标号)。
A.加入 B.加入
B.加入 固体 C.加入浓硫酸 D.加入
固体 C.加入浓硫酸 D.加入 固体
固体
(3)向面食中加入适量的醋可以中和其中过量的食用碱而改善口感,已知 时,三种弱酸的电离平衡常数如下表,写出过量醋酸与
时,三种弱酸的电离平衡常数如下表,写出过量醋酸与 溶液反应的离子方程式:
溶液反应的离子方程式:_______ ;判断 结合质子能力由大到小顺序为
结合质子能力由大到小顺序为_______ 。
(4)吃醋虽好但不宜过量,不然容易造成牙齿酸软,甚至引发龋齿,牙齿的主要成分是羟基磷灰石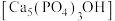 ,市面上含氟牙膏常添加了
,市面上含氟牙膏常添加了 来预防龋齿,请结合化学用语解释含氟牙膏预防龋齿的原因:
来预防龋齿,请结合化学用语解释含氟牙膏预防龋齿的原因:_______ [已知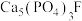 难溶于酸]。
难溶于酸]。
(5)常温下,某同学取 物质的量浓度为
物质的量浓度为 的醋酸,向其中滴入
的醋酸,向其中滴入
 溶液,当滴入的
溶液,当滴入的 溶液的体积为
溶液的体积为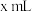 ,溶液呈中性,则醋酸的电离平衡常数
,溶液呈中性,则醋酸的电离平衡常数
_______ (用含x的代数式表示)。

(1)
 的醋酸和盐酸各
的醋酸和盐酸各 分别稀释至
分别稀释至 ,所得醋酸的
,所得醋酸的
 。
。(2)取
 冰醋酸作导电性实验,测得其导电率随加入水的量的变化如图所示。
冰醋酸作导电性实验,测得其导电率随加入水的量的变化如图所示。①由水电离出的氢离子
 :a
:a②使图中b点对应的溶液中
 增大、
增大、 减小,可采用的方法是
减小,可采用的方法是A.加入
 B.加入
B.加入 固体 C.加入浓硫酸 D.加入
固体 C.加入浓硫酸 D.加入 固体
固体(3)向面食中加入适量的醋可以中和其中过量的食用碱而改善口感,已知
 时,三种弱酸的电离平衡常数如下表,写出过量醋酸与
时,三种弱酸的电离平衡常数如下表,写出过量醋酸与 溶液反应的离子方程式:
溶液反应的离子方程式: 结合质子能力由大到小顺序为
结合质子能力由大到小顺序为| 弱酸 |  |  |  |
| 电离平衡常数 | 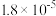 | 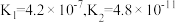 | 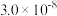 |
(4)吃醋虽好但不宜过量,不然容易造成牙齿酸软,甚至引发龋齿,牙齿的主要成分是羟基磷灰石
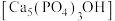 ,市面上含氟牙膏常添加了
,市面上含氟牙膏常添加了 来预防龋齿,请结合化学用语解释含氟牙膏预防龋齿的原因:
来预防龋齿,请结合化学用语解释含氟牙膏预防龋齿的原因: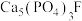 难溶于酸]。
难溶于酸]。(5)常温下,某同学取
 物质的量浓度为
物质的量浓度为 的醋酸,向其中滴入
的醋酸,向其中滴入
 溶液,当滴入的
溶液,当滴入的 溶液的体积为
溶液的体积为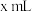 ,溶液呈中性,则醋酸的电离平衡常数
,溶液呈中性,则醋酸的电离平衡常数
您最近半年使用:0次
2024-02-26更新
|
115次组卷
|
2卷引用:云南省大理州民族中学2023-2024学年高二下学期见面考化学试题
3 . 常温下稀 溶液中,下列操作能使
溶液中,下列操作能使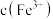 增大的是
增大的是
 溶液中,下列操作能使
溶液中,下列操作能使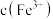 增大的是
增大的是| A.加水稀释 | B.加入几滴稀 | C.加入适量 | D.加热 |
您最近半年使用:0次
2024-01-14更新
|
139次组卷
|
2卷引用:云南省大理州2023-2024学年高二上学期教学质量监测化学试题
名校
解题方法
4 . 已知常温下,几种物质的电离平衡常数,下列说法正确的是
弱酸 | HCOOH(甲酸) |
| HCN |
K(25℃) |
|
|
|
A.三种酸性强弱关系: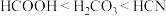 |
B. 的电离方程式为: 的电离方程式为: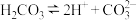 |
C.向 溶液中通入HCN气体: 溶液中通入HCN气体: |
D.等物质的量浓度的 和 和 溶液的pH: 溶液的pH: |
您最近半年使用:0次
2023-12-12更新
|
177次组卷
|
3卷引用:云南省开远市第一中学校2023-2024学年高二上学期12月月考化学试题
名校
解题方法
5 . 下列说法不正确的是
| A.在一定条件下,Na2S溶液加入CuSO4固体,HS-浓度减小 |
| B.加水稀释,水解常数Kh增大,pH减小 |
| C.25℃时,Ka(HCOOH)=1.0×10-4,该温度下HCOO-的水解常数为1.0×10-10 |
| D.某温度下,一元弱酸HA的Ka越小,则NaA的Kh越大 |
您最近半年使用:0次
2023-08-14更新
|
684次组卷
|
4卷引用:云南省开远市第一中学校2023-2024学年高二下学期3月月考化学试题
6 . 氧化铍(BeO) 广泛用于原子能、宇航等领域。一种以铍矿石 (主要成分为Be2SiO4,少量MnO等)为原料提取氧化铍的工艺流程如图所示。
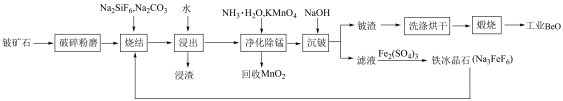
已知:烧结时,未发生氧化还原反应:烧结后,Be、Mn元素以可溶性的Na2BeF4、Na2MnF4形式存在,其余元素以稳定氧化物的形式存在。
回答下列问题:
(1)“烧结”前,将铍矿石“破碎粉磨”的目的是______ 。
(2)“浸渣”的成分为_____ (填化学式)。
(3)“净化除锰”步骤的离子反应方程式为_____________ 。
(4)“沉铍”时,先加入足量NaOH溶液,得到含铍粒子是________ (填粒子符号), 再加热煮沸,调节pH=11,得到颗粒状Be(OH)2。从化学平衡移动的角度解释上述反应原理__________ 。
(5)铁冰晶石(Na3FeF6) 晶体中存在的作用力有__________ ,Fe'+ 的杂化方式是____ (填标号)。
A.dsp2 B.sp3d2 C.sp2 D.sp3

已知:烧结时,未发生氧化还原反应:烧结后,Be、Mn元素以可溶性的Na2BeF4、Na2MnF4形式存在,其余元素以稳定氧化物的形式存在。
回答下列问题:
(1)“烧结”前,将铍矿石“破碎粉磨”的目的是
(2)“浸渣”的成分为
(3)“净化除锰”步骤的离子反应方程式为
(4)“沉铍”时,先加入足量NaOH溶液,得到含铍粒子是
(5)铁冰晶石(Na3FeF6) 晶体中存在的作用力有
A.dsp2 B.sp3d2 C.sp2 D.sp3
您最近半年使用:0次
7 . 下列方程式与所给事实不相符的是
A.向ZnS浊液中滴加 溶液,白色浑浊变为黑色: 溶液,白色浑浊变为黑色: |
B.用白醋去除水垢的离子方程式: |
C.向 溶液中滴加少量浓 溶液中滴加少量浓 ,溶液橙色加深: ,溶液橙色加深: |
D.氯化铵的水溶液显酸性: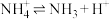 |
您最近半年使用:0次
2023-05-08更新
|
256次组卷
|
3卷引用:云南省大理市下关第一中学2023-2024学年高二下学期开学化学试题
8 . 借助pH传感器测得0.1mol•L-1NaHCO3溶液在先升温、后降温过程中pH变化如图所示。下列分析不合理的是
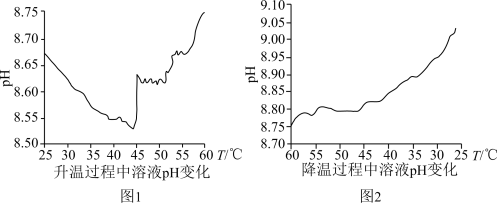

A.图甲中25℃时,溶液中存在关系:c(Na+)=c(HCO )+c(H2CO3)+c(CO )+c(H2CO3)+c(CO ) ) |
B.图甲中25~45℃过程,溶液pH逐渐减小,说明HCO 的电离平衡对pH影响较大 的电离平衡对pH影响较大 |
| C.图甲中45~60℃过程,溶液pH逐渐增大,可能是NaHCO3分解生成Na2CO3导致的结果 |
D.图乙中降温过程,溶液pH逐渐增大,可能是HCO 或CO 或CO 水解平衡正移所致 水解平衡正移所致 |
您最近半年使用:0次
名校
解题方法
9 . 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈红色 | 稀硝酸将Fe氧化为Fe3+,有H2生成 |
| B | 将铜粉加入1.0 mol∙L-1Fe2(SO4)3溶液中 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
| C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| D | 向滴有酚酞的碳酸钠溶液中加入少量的氯化钡固体 | 有白色沉淀生成,溶液的红色变浅 | 碳酸钠溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
10 . 下列现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 等体积等浓度的MgCl2和NaOH溶液混合后,再滴加几滴FeCl3 | 先产生白色沉淀,后沉淀消失 | Fe3+水解出H+造成Mg(OH)2溶解 |
| B | 将通过灼热碎瓷片后的石蜡油蒸气通入到溴水中 | 溴水褪色 | 产物中一定含乙烯 |
| C | SO2分别通入石蕊、品红溶液 | 前者变红,后者褪色 | SO2漂白具有选择性 |
| D | 向5mL0.1mol/LK2Cr2O7溶液滴加5滴浓硫酸 | 溶液颜色由橙色变黄色 | 浓硫酸溶于水放热使平衡移动 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-12-09更新
|
534次组卷
|
4卷引用:云南省大理白族自治州民族中学2023-2024学年高三上学期1月月考理综试卷







