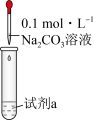
1 . 根据下列实验操作和现象能推出相应结论或目的的是
| 选项 | 实验操作和现象 | 实验目的或结论 |
| A | 向 溶液中滴加 溶液中滴加 溶液,产生白色沉淀 溶液,产生白色沉淀 |  和 和 发生了相互促进的水解反应 发生了相互促进的水解反应 |
| B | 向 溶液中加入 溶液中加入 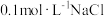 溶液,出现白色沉淀,再加入几滴 溶液,出现白色沉淀,再加入几滴 的 的 溶液,有黑色沉淀生成 溶液,有黑色沉淀生成 | 证明 的溶解度大于 的溶解度大于 的溶解度 的溶解度 |
| C | 向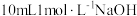 溶液中滴加饱和 溶液中滴加饱和 溶液,有红褐色物质产生 溶液,有红褐色物质产生 | 制备 胶体 胶体 |
| D | 向 溶液中通入 溶液中通入 气体,产生黑色沉淀 气体,产生黑色沉淀 | 氢硫酸为强酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-07更新
|
545次组卷
|
6卷引用:福建省莆田市2022-2023学年高三毕业班第四次教学质量检测化学试题
名校
解题方法
2 . 利用下列装置进行实验,能达到实验目的的是
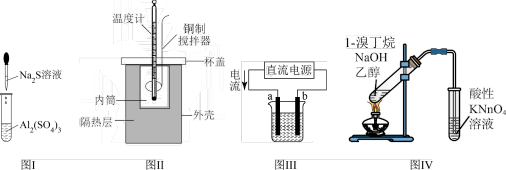
A.图Ⅰ装置可制备 固体 固体 |
| B.图Ⅱ装置可测定中和反应的反应热 |
C.图Ⅲ装置可实现铁上镀铜,a极为铜,电解质溶液可以是 溶液 溶液 |
| D.图Ⅳ装置可检验1-溴丁烷和氢氧化钠乙醇溶液反应的产物 |
您最近一年使用:0次
2023-03-03更新
|
859次组卷
|
5卷引用:山东省济宁市2023届高三一模考试(3月)化学试题
解题方法
3 . 碳酸亚铁(白色固体,难溶于水)是一种重要的工业原料,可用于制备补血剂乳酸亚铁。某研究小组通过下列实验,寻找利用复分解反应制备 的最佳方案:
的最佳方案:
(1)实验Ⅰ中产生红褐色沉淀的原因是___________ (用方程式表示)。
(2)实验Ⅱ中产生 的离子方程式为
的离子方程式为___________ 。
(3)为了探究实验Ⅲ中 起的作用,甲同学设计了实验Ⅳ进行探究:
起的作用,甲同学设计了实验Ⅳ进行探究:
实验Ⅳ中加入 固体的目的是
固体的目的是___________ 。对比实验Ⅱ、Ⅲ、Ⅳ,甲同学得出结论:
 水解产生
水解产生 ,降低溶液
,降低溶液 ,减少了副产物
,减少了副产物 的产生。
的产生。
乙同学认为该实验方案不够严谨,应补充的对比实验操作是___________ ,再取该溶液一滴管,与2 1
1
 溶液混合。
溶液混合。
(4)小组同学进一步讨论认为,定性实验现象并不能直接证明实验Ⅲ中 的纯度最高,需要利用如图所示的装置进行定量测定。分别将实验Ⅰ、Ⅱ、Ⅲ中的沉淀进行过滤、洗涤、干燥后称量,然后转移至A处的广口瓶中。
的纯度最高,需要利用如图所示的装置进行定量测定。分别将实验Ⅰ、Ⅱ、Ⅲ中的沉淀进行过滤、洗涤、干燥后称量,然后转移至A处的广口瓶中。

①A中分液漏斗中的试剂为___________ 。
②为测定 的纯度,除样品总质量外,还需测定的物理量是
的纯度,除样品总质量外,还需测定的物理量是___________ 。
(5)实验反思:经测定,实验Ⅲ中的 纯度高于实验Ⅰ和实验Ⅱ。通过以上实验分析,制备
纯度高于实验Ⅰ和实验Ⅱ。通过以上实验分析,制备 实验成功的关键因素是
实验成功的关键因素是___________ 。
 的最佳方案:
的最佳方案:| 实验 | 试剂 | 现象 | |
| 滴管 | 试管 | ||
 | 0.8  溶液 溶液(  ) ) | 1  溶液( 溶液( ) ) | 实验Ⅰ:立即产生灰绿色沉淀,5 后出现明显的红褐色 后出现明显的红褐色 |
0.8  溶液 溶液(  ) ) | 1  溶液( 溶液( ) ) | 实验Ⅱ:产生白色沉淀及少量无色气泡,2 后出现明显的灰绿色 后出现明显的灰绿色 | |
0.8  溶液(  ) ) | 1  溶液( 溶液( ) ) | 实验Ⅲ:产生白色沉淀及无色气泡,较长时间保持白色 | |
(2)实验Ⅱ中产生
 的离子方程式为
的离子方程式为(3)为了探究实验Ⅲ中
 起的作用,甲同学设计了实验Ⅳ进行探究:
起的作用,甲同学设计了实验Ⅳ进行探究:| 操作 | 现象 | |
| 实验Ⅳ | 向0.8  溶液中加入 溶液中加入 固体配制成混合溶液(已知 固体配制成混合溶液(已知 对实验无影响,忽略混合后溶液体积变化)。再取该溶液一滴管,与2 对实验无影响,忽略混合后溶液体积变化)。再取该溶液一滴管,与2 1 1  溶液混合。 溶液混合。 | 与实验Ⅲ现象相同 |
 固体的目的是
固体的目的是 水解产生
水解产生 ,降低溶液
,降低溶液 ,减少了副产物
,减少了副产物 的产生。
的产生。乙同学认为该实验方案不够严谨,应补充的对比实验操作是
 1
1
 溶液混合。
溶液混合。(4)小组同学进一步讨论认为,定性实验现象并不能直接证明实验Ⅲ中
 的纯度最高,需要利用如图所示的装置进行定量测定。分别将实验Ⅰ、Ⅱ、Ⅲ中的沉淀进行过滤、洗涤、干燥后称量,然后转移至A处的广口瓶中。
的纯度最高,需要利用如图所示的装置进行定量测定。分别将实验Ⅰ、Ⅱ、Ⅲ中的沉淀进行过滤、洗涤、干燥后称量,然后转移至A处的广口瓶中。
①A中分液漏斗中的试剂为
②为测定
 的纯度,除样品总质量外,还需测定的物理量是
的纯度,除样品总质量外,还需测定的物理量是(5)实验反思:经测定,实验Ⅲ中的
 纯度高于实验Ⅰ和实验Ⅱ。通过以上实验分析,制备
纯度高于实验Ⅰ和实验Ⅱ。通过以上实验分析,制备 实验成功的关键因素是
实验成功的关键因素是
您最近一年使用:0次
4 . 下列实验操作可以达到实验目的的是
| 选项 | 实验目的 | 实验操作及现象 |
| A | 比较CH3COOH和H2CO3的酸性 | 用pH计分别测定0.1000mol/LCH3COONH4溶液和Na2CO3溶液的pH后者大于前者 |
| B | 检验铁锈中含有二价铁 | 将铁锈溶于浓盐酸,滴入KMnO4溶液,紫色褪去 |
| C | 探究氢离子浓度对 相互转化的影响 相互转化的影响 | 向K2CrO4溶液中缓慢滴加硫酸,观察到溶液由黄色变为橙红色 |
| D | 证明Cl2、Br2、I2的氧化性 | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液,溶液先变橙色,后变蓝色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题。
(1)为探究 与
与 的还原性强弱,取适量制得的
的还原性强弱,取适量制得的 晶体,进行如下实验:
晶体,进行如下实验:
将适量 加入
加入 溶液中,若观察到
溶液中,若观察到___________ ,则可证明还原性 ;实际发现溶液产生红褐色沉淀,并闻到臭鸡蛋气味气体,请从平衡移动的角度解释上述现象:
;实际发现溶液产生红褐色沉淀,并闻到臭鸡蛋气味气体,请从平衡移动的角度解释上述现象:___________ 。
(2)为了证明 可以氧化
可以氧化 溶液中的
溶液中的 ,某同学设计了一个原电池装置,并正确绘制了其工作原理示意图,但不慎被污渍遮住了部分内容(如下图),请“复原”该示意图:
,某同学设计了一个原电池装置,并正确绘制了其工作原理示意图,但不慎被污渍遮住了部分内容(如下图),请“复原”该示意图:___________

(1)为探究
 与
与 的还原性强弱,取适量制得的
的还原性强弱,取适量制得的 晶体,进行如下实验:
晶体,进行如下实验:将适量
 加入
加入 溶液中,若观察到
溶液中,若观察到 ;实际发现溶液产生红褐色沉淀,并闻到臭鸡蛋气味气体,请从平衡移动的角度解释上述现象:
;实际发现溶液产生红褐色沉淀,并闻到臭鸡蛋气味气体,请从平衡移动的角度解释上述现象:(2)为了证明
 可以氧化
可以氧化 溶液中的
溶液中的 ,某同学设计了一个原电池装置,并正确绘制了其工作原理示意图,但不慎被污渍遮住了部分内容(如下图),请“复原”该示意图:
,某同学设计了一个原电池装置,并正确绘制了其工作原理示意图,但不慎被污渍遮住了部分内容(如下图),请“复原”该示意图:
您最近一年使用:0次
6 . 碳酸钠俗称纯碱,是一种重要的化工原料,在生活、生产和实验研究中均有广泛应用。某学习小组探究 溶液与盐溶液反应的产物,进行如下实验。
溶液与盐溶液反应的产物,进行如下实验。
(1)配制100mL 的
的 溶液。
溶液。
①配制溶液过程中用托盘天平称量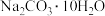 固体的质量为
固体的质量为_______ g。
②定容时,加蒸馏水不慎超过刻度线,处理的方法是_______ 。
(2)通过下列实验探究 溶液与盐溶液反应,记录实验现象如下表:
溶液与盐溶液反应,记录实验现象如下表:
为了探究白色沉淀的成分,设计了热分解实验,其装置如图所示:
①实验甲产生白色沉淀反应的离子方程式为_______ 。
②装置E的作用是_______ 。
③通过热分解实验可判断实验乙所得白色沉淀的成分为_______ (填化学式),实验乙反应的离子方程式为_______ 。
④实验丙所得白色沉淀的化学式可表示为 ,则
,则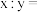
_______ 。
 溶液与盐溶液反应的产物,进行如下实验。
溶液与盐溶液反应的产物,进行如下实验。(1)配制100mL
 的
的 溶液。
溶液。①配制溶液过程中用托盘天平称量
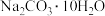 固体的质量为
固体的质量为②定容时,加蒸馏水不慎超过刻度线,处理的方法是
(2)通过下列实验探究
 溶液与盐溶液反应,记录实验现象如下表:
溶液与盐溶液反应,记录实验现象如下表:| 装置 | 实验 | 试剂a | 现象 |
| 甲 | 4mL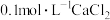 溶液 溶液 | 产生白色沉淀 |
| 乙 | 4mL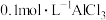 溶液 溶液 | 产生白色沉淀及大量气体 | |
| 丙 | 4mL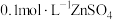 溶液 溶液 | 产生白色沉淀及大量气体 |

| 样品 | 加热前样品质量/g | 加热后样品质量/g | 装置C增重/g | 装置D增重/g |
| 实验乙样品 | 10.4 | 6.8 | 3.6 | 0 |
| 实验丙样品 | 22.4 | 16.2 | 1.8 | 4.4 |
②装置E的作用是
③通过热分解实验可判断实验乙所得白色沉淀的成分为
④实验丙所得白色沉淀的化学式可表示为
 ,则
,则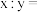
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题
(1)工业制胆矾时,将粗制 粉末(含
粉末(含 、
、 杂质)慢慢加入适量的稀
杂质)慢慢加入适量的稀 中完全溶解,除去杂质离子后,再经过一系列操作可得纯净的胆矾晶体。
中完全溶解,除去杂质离子后,再经过一系列操作可得纯净的胆矾晶体。
已知: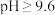 时,
时, 以
以 的形式完全沉淀:
的形式完全沉淀: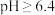 时,
时, 以
以 的形式完全沉淀:
的形式完全沉淀: 接近4时,
接近4时, 以
以 的形式完全沉淀.回答下列问题:
的形式完全沉淀.回答下列问题:
①为除去 ,可先加入
,可先加入________ ,(填编号)将 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为________________ ,后加入适当的________ (填编号)调节溶液的 使
使 沉淀。
沉淀。
A. B.
B. C.
C. D.
D.
②甲同学怀疑调整溶液 接近4是否能达到除去
接近4是否能达到除去 而不损失
而不损失 的目的,已知,常温下
的目的,已知,常温下 的溶度积
的溶度积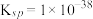 ,
, 的溶度积
的溶度积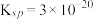 ,设溶液中
,设溶液中 的浓度为
的浓度为 ,则
,则 开始沉淀时溶液的
开始沉淀时溶液的 为
为________ , 完全沉淀时溶液的的
完全沉淀时溶液的的 为
为________ ,通过计算确定上述方案________ (填“可行”或“不可行”).
③ ,
, 溶液中由水电离出的
溶液中由水电离出的 是
是________ 。
(2)SOCl2是一种液态化合物,将其滴入水中,反应剧烈,液面上有白雾形成,并有带刺激性气味气体逸出,该气体可使品红溶液褪色。
①根据实验现象,写出SOCl2和H2O反应的化学方程式:________________ 。
②利用SOCl2和AlCl3•6H2O混合共热可制备无水AlCl3,试解释原因________________ 。
(1)工业制胆矾时,将粗制
 粉末(含
粉末(含 、
、 杂质)慢慢加入适量的稀
杂质)慢慢加入适量的稀 中完全溶解,除去杂质离子后,再经过一系列操作可得纯净的胆矾晶体。
中完全溶解,除去杂质离子后,再经过一系列操作可得纯净的胆矾晶体。已知:
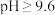 时,
时, 以
以 的形式完全沉淀:
的形式完全沉淀: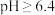 时,
时, 以
以 的形式完全沉淀:
的形式完全沉淀: 接近4时,
接近4时, 以
以 的形式完全沉淀.回答下列问题:
的形式完全沉淀.回答下列问题:①为除去
 ,可先加入
,可先加入 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为 使
使 沉淀。
沉淀。A.
 B.
B. C.
C. D.
D.
②甲同学怀疑调整溶液
 接近4是否能达到除去
接近4是否能达到除去 而不损失
而不损失 的目的,已知,常温下
的目的,已知,常温下 的溶度积
的溶度积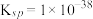 ,
, 的溶度积
的溶度积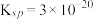 ,设溶液中
,设溶液中 的浓度为
的浓度为 ,则
,则 开始沉淀时溶液的
开始沉淀时溶液的 为
为 完全沉淀时溶液的的
完全沉淀时溶液的的 为
为③
 ,
, 溶液中由水电离出的
溶液中由水电离出的 是
是(2)SOCl2是一种液态化合物,将其滴入水中,反应剧烈,液面上有白雾形成,并有带刺激性气味气体逸出,该气体可使品红溶液褪色。
①根据实验现象,写出SOCl2和H2O反应的化学方程式:
②利用SOCl2和AlCl3•6H2O混合共热可制备无水AlCl3,试解释原因
您最近一年使用:0次
8 . 某同学按图示装置进行实验,下列有关现象和结论均正确的是
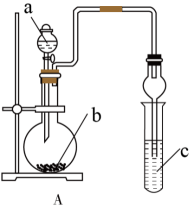

| a | b | c | 现象 | 结论 | |
| A | 浓氨水 | 氢氧化钠 | 硝酸银溶液 | 沉淀先生成后消失 | 有配合物生成 |
| B | 稀盐酸 | 大理石 | 苯酚钠溶液 | 溶液变浑浊 | 酸性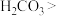 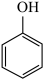 |
| C | 饱和食盐水 | 电石 | 酸性高锰酸钾溶液 | 溶液褪色 | 有乙炔生成 |
| D |  溶液 溶液 |  |  | 淡黄色沉淀生成 | 氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 某实验小组对FeCl3溶液与Na2SO3溶液的反应进行探究。
已知:铁氰化钾的化学式为K3[Fe(CN)6],用于检验Fe2+,遇Fe2+离子产生蓝色沉淀
【实验1】
(1)配制FeCl3溶液时,先将FeCl3溶于浓盐酸,再稀释至指定浓度。从化学平衡角度说明浓盐酸的作用:__________ 。
【探究现象i产生的原因】
(2)甲同学认为发生反应:2Fe3++3 +6H2O
+6H2O 2Fe(OH)3(胶体)+3H2SO3;他取少量红褐色溶液于试管中,继续滴加1mol/LNa2SO3溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是
2Fe(OH)3(胶体)+3H2SO3;他取少量红褐色溶液于试管中,继续滴加1mol/LNa2SO3溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是_______ (填化学式)。
(3)乙同学认为还发生了氧化还原反应。他取少许红褐色溶液于试管中,加入______ ,有白色沉淀产生,证明产物中含有 。
。
丙同学认为乙同学的实验不严谨,因为在上述过程中 可能被其它物质氧化。为了进一步确认
可能被其它物质氧化。为了进一步确认 被氧化的原因,丙同学设计了实验2。
被氧化的原因,丙同学设计了实验2。
【实验2】用如图装置(a、b均为石墨电极)进行实验。闭合开关后灵敏电流计指针偏转。
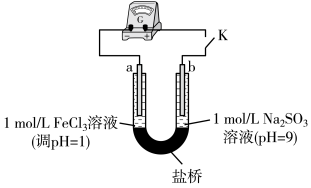
(4)实验2中正极的电极反应式为______ 。丙同学又用铁氰化钾溶液检验正极的产物,观察到有蓝色沉淀产生。他得出的结论是___________ 。
【解释现象ii产生的原因】
(5)综合上述结果,请从平衡移动角度解释,现象ii产生的原因为___________________ 。
已知:铁氰化钾的化学式为K3[Fe(CN)6],用于检验Fe2+,遇Fe2+离子产生蓝色沉淀
【实验1】
| 装置 | 实验现象 |
 | 现象i:一开始溶液颜色加深,由棕黄色变为红褐色。 现象ii:一段时间后溶液颜色变浅,变为浅黄色。 |
【探究现象i产生的原因】
(2)甲同学认为发生反应:2Fe3++3
 +6H2O
+6H2O 2Fe(OH)3(胶体)+3H2SO3;他取少量红褐色溶液于试管中,继续滴加1mol/LNa2SO3溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是
2Fe(OH)3(胶体)+3H2SO3;他取少量红褐色溶液于试管中,继续滴加1mol/LNa2SO3溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是(3)乙同学认为还发生了氧化还原反应。他取少许红褐色溶液于试管中,加入
 。
。丙同学认为乙同学的实验不严谨,因为在上述过程中
 可能被其它物质氧化。为了进一步确认
可能被其它物质氧化。为了进一步确认 被氧化的原因,丙同学设计了实验2。
被氧化的原因,丙同学设计了实验2。【实验2】用如图装置(a、b均为石墨电极)进行实验。闭合开关后灵敏电流计指针偏转。

(4)实验2中正极的电极反应式为
【解释现象ii产生的原因】
(5)综合上述结果,请从平衡移动角度解释,现象ii产生的原因为
您最近一年使用:0次
10 . 某实验小组为探究 与
与 反应后的产物,做如下探究实验。
反应后的产物,做如下探究实验。
【查阅资料】
① 为砖红色固体,不溶于水;
为砖红色固体,不溶于水;
②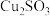 为黄色固体,不溶于水;
为黄色固体,不溶于水;
③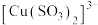 为无色配合离子、
为无色配合离子、 为无色配合离子、
为无色配合离子、 为深蓝色配合离子。
为深蓝色配合离子。
【实验探究】
实验1:①向2mL 的
的 溶液中滴加
溶液中滴加 的
的 溶液,开始出现黄色沉淀,但无气体产生。
溶液,开始出现黄色沉淀,但无气体产生。
②继续加入 溶液,最终沉淀消失。经检验,溶液中生成
溶液,最终沉淀消失。经检验,溶液中生成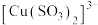 离子。
离子。
实验2:向90℃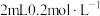 的
的 溶液中滴加
溶液中滴加 的
的 溶液,直接生成砖红色沉淀。
溶液,直接生成砖红色沉淀。
实验3:向2mL 的
的 溶液中滴加
溶液中滴加 的
的 溶液,开始阶段有蓝色沉淀出现。
溶液,开始阶段有蓝色沉淀出现。
(1)某同学认为实验1黄色沉淀中有少量 ,该同学认为是
,该同学认为是 、
、 相互促进水解产生的,用离子方程式表示生成
相互促进水解产生的,用离子方程式表示生成 沉淀的过程:
沉淀的过程:_______ 。
(2)若要进一步检验黄色沉淀中有Cu(OH)2,可采用的具体实验方法为_______ 。
(3)经检验,实验2所得溶液中有大量 、
、 生成。该实验中
生成。该实验中 表现
表现_______ 性,写出该实验中反应的离子方程式:_______ 。
(4)某同学设计了如图所示的电化学装置,探究 与
与 的反应。该装置中左侧烧杯中的石墨电极做
的反应。该装置中左侧烧杯中的石墨电极做_______ (填“正”或“负”)极,右侧烧杯中发生反应的电极反应式为_______ 。设计实验检验右侧烧杯中生成的阴离子,写出具体操作、现象和结论:_______ 。

 与
与 反应后的产物,做如下探究实验。
反应后的产物,做如下探究实验。【查阅资料】
①
 为砖红色固体,不溶于水;
为砖红色固体,不溶于水;②
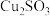 为黄色固体,不溶于水;
为黄色固体,不溶于水;③
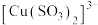 为无色配合离子、
为无色配合离子、 为无色配合离子、
为无色配合离子、 为深蓝色配合离子。
为深蓝色配合离子。【实验探究】
实验1:①向2mL
 的
的 溶液中滴加
溶液中滴加 的
的 溶液,开始出现黄色沉淀,但无气体产生。
溶液,开始出现黄色沉淀,但无气体产生。②继续加入
 溶液,最终沉淀消失。经检验,溶液中生成
溶液,最终沉淀消失。经检验,溶液中生成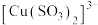 离子。
离子。实验2:向90℃
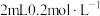 的
的 溶液中滴加
溶液中滴加 的
的 溶液,直接生成砖红色沉淀。
溶液,直接生成砖红色沉淀。实验3:向2mL
 的
的 溶液中滴加
溶液中滴加 的
的 溶液,开始阶段有蓝色沉淀出现。
溶液,开始阶段有蓝色沉淀出现。(1)某同学认为实验1黄色沉淀中有少量
 ,该同学认为是
,该同学认为是 、
、 相互促进水解产生的,用离子方程式表示生成
相互促进水解产生的,用离子方程式表示生成 沉淀的过程:
沉淀的过程:(2)若要进一步检验黄色沉淀中有Cu(OH)2,可采用的具体实验方法为
(3)经检验,实验2所得溶液中有大量
 、
、 生成。该实验中
生成。该实验中 表现
表现(4)某同学设计了如图所示的电化学装置,探究
 与
与 的反应。该装置中左侧烧杯中的石墨电极做
的反应。该装置中左侧烧杯中的石墨电极做
您最近一年使用:0次
2022-11-04更新
|
1531次组卷
|
4卷引用:广东省2023届高三一轮复习联考(二)广东卷化学试题
广东省2023届高三一轮复习联考(二)广东卷化学试题(已下线)热点情景汇编-专题十三 实验探究中的新思路(已下线)专题十六实验设计与探究实验广东省部分学校2022-2023学年高三上学期一轮复习联考(二)化学试题