名校
解题方法
1 . 已知亚磷酸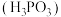 是二元弱酸。常温下,向
是二元弱酸。常温下,向 溶液中滴加
溶液中滴加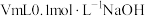 溶液,溶液的
溶液,溶液的 与
与 的关系如图所示。
的关系如图所示。

下列叙述错误的是
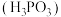 是二元弱酸。常温下,向
是二元弱酸。常温下,向 溶液中滴加
溶液中滴加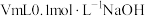 溶液,溶液的
溶液,溶液的 与
与 的关系如图所示。
的关系如图所示。
下列叙述错误的是
A. 时溶液中 时溶液中 |
B. |
C. 的平衡常数 的平衡常数 为 为 |
D.图中 |
您最近一年使用:0次
2024-02-08更新
|
90次组卷
|
2卷引用:河南省南阳市六校2023-2024学年高二上学期1月期末联考化学试题
名校
解题方法
2 . Ka、Kw、Kh、Ksp分别表示电离常数、水的离子积常数、水解常数、溶度积常数,下列判断不正确的是
A.室温下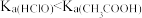 , , 的电离度一定比HClO的大 的电离度一定比HClO的大 |
B.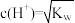 的溶液任何温度下均为中性 的溶液任何温度下均为中性 |
| C.已知25℃时,AgCl和砖红色沉淀Ag2CrO4的Ksp分别为1.8×10-10和2.0×10-12,则用AgNO3标准溶液滴定Cl-时,可采用K2CrO4为指示剂 |
| D.某温度下,一元弱酸HA的Ka越小,则NaA的Kh越大 |
您最近一年使用:0次
2023-12-25更新
|
488次组卷
|
8卷引用:河南省商丘市第一高级中学2022-2023学年高二下学期3月份考试化学试题
名校
解题方法
3 . 下列说法不正确的是
| A.在一定条件下,Na2S溶液加入CuSO4固体,HS-浓度减小 |
| B.加水稀释,水解常数Kh增大,pH减小 |
| C.25℃时,Ka(HCOOH)=1.0×10-4,该温度下HCOO-的水解常数为1.0×10-10 |
| D.某温度下,一元弱酸HA的Ka越小,则NaA的Kh越大 |
您最近一年使用:0次
2023-08-14更新
|
689次组卷
|
4卷引用:河南省宜阳县第一高级中学2023-2024学年高二上学期能力达标测试化学试题
解题方法
4 . 丙二酸( )是二元弱酸。298K时,向一定浓度的
)是二元弱酸。298K时,向一定浓度的 溶液中滴加盐酸,混合溶液中含碳粒子浓度pX与pH的关系如图所示。已知:
溶液中滴加盐酸,混合溶液中含碳粒子浓度pX与pH的关系如图所示。已知: ,
, 或
或 )下列叙述正确的是
)下列叙述正确的是

 )是二元弱酸。298K时,向一定浓度的
)是二元弱酸。298K时,向一定浓度的 溶液中滴加盐酸,混合溶液中含碳粒子浓度pX与pH的关系如图所示。已知:
溶液中滴加盐酸,混合溶液中含碳粒子浓度pX与pH的关系如图所示。已知: ,
, 或
或 )下列叙述正确的是
)下列叙述正确的是
A.直线 表示pH与 表示pH与 的关系 的关系 |
B. 稀溶液与等体积、等浓度的盐酸混合后, 稀溶液与等体积、等浓度的盐酸混合后, |
C.当 时,溶液pH=3.26 时,溶液pH=3.26 |
D. 的溶液中的溶质可能是 的溶液中的溶质可能是 和 和 |
您最近一年使用:0次
5 . 食用磷酸钾(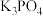 )可用作食品乳化剂,工业制备原理为:
)可用作食品乳化剂,工业制备原理为:
ⅰ. ,控制
,控制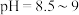 左右;
左右;
ⅱ.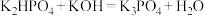 ,控制pH=14左右。
,控制pH=14左右。
已知常温下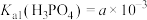 、
、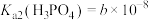 、
、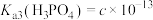 。
。
常温下,下列说法正确的是
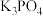 )可用作食品乳化剂,工业制备原理为:
)可用作食品乳化剂,工业制备原理为:ⅰ.
 ,控制
,控制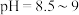 左右;
左右;ⅱ.
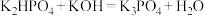 ,控制pH=14左右。
,控制pH=14左右。已知常温下
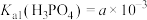 、
、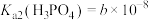 、
、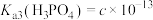 。
。常温下,下列说法正确的是
A. 溶液中由水电离出的氢离子浓度一定大于 溶液中由水电离出的氢离子浓度一定大于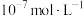 |
B.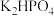 溶液中 溶液中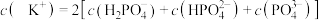 |
C.向 溶液中滴加少量KOH溶液,反应的离子方程式为 溶液中滴加少量KOH溶液,反应的离子方程式为 |
D.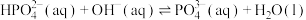 的化学平衡常数为10c 的化学平衡常数为10c |
您最近一年使用:0次
2023-06-21更新
|
65次组卷
|
2卷引用:河南省大联考2022-2023学年高二下学期阶段性测试(五)化学试题
名校
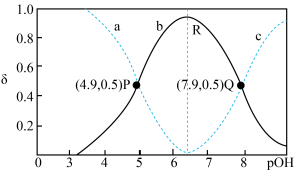
6 . 乙二胺 ( )是二元弱碱,在溶液中分步电离。25℃时,向一定浓度的乙二胺溶液中滴加稀盐酸,溶液中各含氮微粒的分布分数
)是二元弱碱,在溶液中分步电离。25℃时,向一定浓度的乙二胺溶液中滴加稀盐酸,溶液中各含氮微粒的分布分数 (平衡时某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液
(平衡时某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液 的变化如图所示。下列说法错误的是
的变化如图所示。下列说法错误的是
 )是二元弱碱,在溶液中分步电离。25℃时,向一定浓度的乙二胺溶液中滴加稀盐酸,溶液中各含氮微粒的分布分数
)是二元弱碱,在溶液中分步电离。25℃时,向一定浓度的乙二胺溶液中滴加稀盐酸,溶液中各含氮微粒的分布分数 (平衡时某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液
(平衡时某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液 的变化如图所示。下列说法错误的是
的变化如图所示。下列说法错误的是
A.曲线 表示 表示 微粒的分布分数 微粒的分布分数 随溶液 随溶液 的变化关系 的变化关系 |
B.常温下,R点溶液中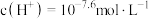 |
C.Q点溶液中的离子浓度关系: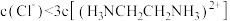 |
D.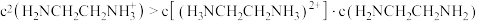 |
您最近一年使用:0次
2023-05-19更新
|
305次组卷
|
4卷引用:河南省洛阳市宜阳县第一高级中学2023-2024学年高二上学期清北园第六次能力达标测试化学试题
名校
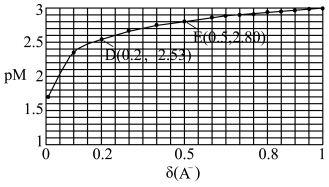
7 . HA是一元弱酸,微溶性盐 的饱和溶液中
的饱和溶液中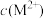 随
随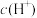 而变化,
而变化, 不发生水解。定义如下关系:
不发生水解。定义如下关系: ,
,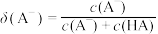 。25℃时,实验测得pM与
。25℃时,实验测得pM与 的关系如图所示,其中D点对应的
的关系如图所示,其中D点对应的 。已知
。已知 ,则下列说法不正确的是
,则下列说法不正确的是
 的饱和溶液中
的饱和溶液中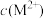 随
随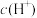 而变化,
而变化, 不发生水解。定义如下关系:
不发生水解。定义如下关系: ,
,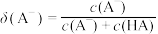 。25℃时,实验测得pM与
。25℃时,实验测得pM与 的关系如图所示,其中D点对应的
的关系如图所示,其中D点对应的 。已知
。已知 ,则下列说法不正确的是
,则下列说法不正确的是
A.25℃时,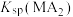 的数量级为 的数量级为 |
B.E点的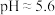 |
C.D点存在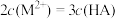 |
D.25℃时,HA的电离常数 为 为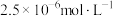 |
您最近一年使用:0次
名校
解题方法
8 . X、Y、Z、M、W五种主族元素位于前四周期,原子序数依次增大,且这五种元素的最外层电子数之和为16。其中X、Y、Z、M为短周期主族元素,M的最外层电子数为Z的两倍,只有Y、M位于同一主族,且只有Z、M位于同一周期。
回答下列问题:
(1)X、Y、M的有关化学键键能如表所示,简要分析和解释下列有关事实:
①Y与M位于同一主族,但Y元素形成的物质种类远多于M元素形成的物质种类,原因为______ 。
②稳定性:YX4_____ (填“>”或“<”)MX4。
(2)由Y原子与M原子以1∶1的个数比相互交替结合形成晶体(Q)。则Q的化学式为______ 。
(3)在元素周期表中,某些主族元素与其右下方的主族元素的有些性质是相似的,这种相似性被称为对角线规则,在前三周期元素中,若元素R与元素Z是“对角关系”,则在加热条件下,单质R与氧气发生反应的化学方程式为______ 。
(4)常温下,X3WO4的电离平衡常数如表所示:
①请根据结构与性质的关系解释X3WO4第一步电离大于第二步电离的原因:______ 。_______ (lg2≈0.3)。
回答下列问题:
(1)X、Y、M的有关化学键键能如表所示,简要分析和解释下列有关事实:
| 化学键 | Y-Y | Y-X | M-M | M-X |
| 键能/(kJ•mol-1) | 356 | 413 | 226 | 318 |
②稳定性:YX4
(2)由Y原子与M原子以1∶1的个数比相互交替结合形成晶体(Q)。则Q的化学式为
(3)在元素周期表中,某些主族元素与其右下方的主族元素的有些性质是相似的,这种相似性被称为对角线规则,在前三周期元素中,若元素R与元素Z是“对角关系”,则在加热条件下,单质R与氧气发生反应的化学方程式为
(4)常温下,X3WO4的电离平衡常数如表所示:
| 电离平衡常数 | Ka1 | Ka2 | Ka3 |
| X3WO4 | 5×10-3 | 2×10-7 | 4.0×10-12 |
②已知磷酸的结构式为 ,请画出X3WO4分子的结构:
,请画出X3WO4分子的结构:
您最近一年使用:0次
2023-04-16更新
|
110次组卷
|
4卷引用:河南省周口市项城市五校联考2022-2023学年高二下学期4月月考化学试题
名校
9 . 回答下列问题:
(1)已知25℃时, 的
的 mol·L
mol·L ,则当溶液中
,则当溶液中 时,溶液的
时,溶液的
_______ 。
(2)0.1 mol·L
 溶液中
溶液中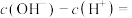
_______ (用含 、
、 的关系式表示)。
的关系式表示)。
(3)向 溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式:
溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式:_______ 。
(4)用电解法将 转化为燃料是实现碳循环的一种途径,原理如图所示。铜电极上产生
转化为燃料是实现碳循环的一种途径,原理如图所示。铜电极上产生 的电极反应式为
的电极反应式为_______ ,若阴极只产生HCOOH,则相同条件下Pt电极产生的 与Cu电极上产生的HCOOH的物质的量之比为
与Cu电极上产生的HCOOH的物质的量之比为_______ 。

(1)已知25℃时,
 的
的 mol·L
mol·L ,则当溶液中
,则当溶液中 时,溶液的
时,溶液的
(2)0.1 mol·L

 溶液中
溶液中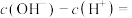
 、
、 的关系式表示)。
的关系式表示)。(3)向
 溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式:
溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式:(4)用电解法将
 转化为燃料是实现碳循环的一种途径,原理如图所示。铜电极上产生
转化为燃料是实现碳循环的一种途径,原理如图所示。铜电极上产生 的电极反应式为
的电极反应式为 与Cu电极上产生的HCOOH的物质的量之比为
与Cu电极上产生的HCOOH的物质的量之比为
您最近一年使用:0次
名校
10 . 乙二酸( 或HOOCCOOH)俗称草酸,是一种二元弱酸,在工业上可作漂白剂、鞣革剂,在实验研究和化学工业中应用广泛。
或HOOCCOOH)俗称草酸,是一种二元弱酸,在工业上可作漂白剂、鞣革剂,在实验研究和化学工业中应用广泛。
(1)草酸第一步电离的电离方程式为___________________________ 。
(2)草酸可用来测定未知浓度的 溶液(用草酸滴定
溶液(用草酸滴定 溶液)。
溶液)。
①实验过程中,草酸应用___________ (填“酸式”或“碱式”)滴定管盛装。
②判断达到滴定终点时的现象为_______________________________________________________ 。
③若滴定完成后仰视读数,则测得的 溶液浓度
溶液浓度___________ (“偏高”、“偏低”或“无影响”)。
(3)常温下,草酸溶液中微粒的物质的量分数随溶液pH的变化如图所示:
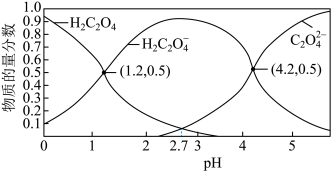
已知:常温下, 的电离平衡常数
的电离平衡常数 ,
, 。
。
①常温下,草酸的电离平衡常数
___________ 。
②相同条件下,物质的量浓度均为0.1 的
的 溶液的pH比
溶液的pH比 溶液的pH
溶液的pH__________ (填“大”或“小”)。
③常温下,向10mL 0.1
 溶液中逐滴加入0.1
溶液中逐滴加入0.1 KOH溶液,随着KOH溶液体积的增加,当溶液中
KOH溶液,随着KOH溶液体积的增加,当溶液中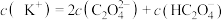 时,加入的V(KOH溶液)
时,加入的V(KOH溶液)___________ (填“>”、“=”或“<”)10mL,若加入KOH溶液体积为10mL溶液中 、
、 、
、 的浓度由大到小的顺序为
的浓度由大到小的顺序为________________________ 。
 或HOOCCOOH)俗称草酸,是一种二元弱酸,在工业上可作漂白剂、鞣革剂,在实验研究和化学工业中应用广泛。
或HOOCCOOH)俗称草酸,是一种二元弱酸,在工业上可作漂白剂、鞣革剂,在实验研究和化学工业中应用广泛。(1)草酸第一步电离的电离方程式为
(2)草酸可用来测定未知浓度的
 溶液(用草酸滴定
溶液(用草酸滴定 溶液)。
溶液)。①实验过程中,草酸应用
②判断达到滴定终点时的现象为
③若滴定完成后仰视读数,则测得的
 溶液浓度
溶液浓度(3)常温下,草酸溶液中微粒的物质的量分数随溶液pH的变化如图所示:

已知:常温下,
 的电离平衡常数
的电离平衡常数 ,
, 。
。①常温下,草酸的电离平衡常数

②相同条件下,物质的量浓度均为0.1
 的
的 溶液的pH比
溶液的pH比 溶液的pH
溶液的pH③常温下,向10mL 0.1

 溶液中逐滴加入0.1
溶液中逐滴加入0.1 KOH溶液,随着KOH溶液体积的增加,当溶液中
KOH溶液,随着KOH溶液体积的增加,当溶液中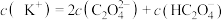 时,加入的V(KOH溶液)
时,加入的V(KOH溶液) 、
、 、
、 的浓度由大到小的顺序为
的浓度由大到小的顺序为
您最近一年使用:0次
2023-02-11更新
|
186次组卷
|
2卷引用:河南省名校2022-2023学年高二下学期开学考试化学试题



