名校
解题方法
1 . 回答下列问题。
(1)向滴有酚酞的氨水中加入少量的氯化铵固体,观察到的现象是___________ ,用平衡原理解释原因___________ 。
(2)常温下,0.1 mol/L 的NaOH溶液的pH=___________ ,0.05mol/L的硫酸的pH=___________ ,取一定体积的两溶液混合,所得混合液的pH=2,则所取硫酸溶液的体积与NaOH溶液的体积比为___________ 。
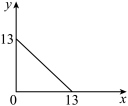
(3)某温度(t℃)下的溶液中,c(H+)=10-xmol/L,c(OH-)=10-ymol/L,x与y的关系如图所示,此温度时,水的离子积常数Kw为___________ ,则该温度t___________ 25℃(填“>”“<”或“=”)。
(4)25℃时,pH=3的酸酸溶液和pH=11的NaOH溶液中由水电离出的c(H+)之比为___________ 。
(1)向滴有酚酞的氨水中加入少量的氯化铵固体,观察到的现象是
(2)常温下,0.1 mol/L 的NaOH溶液的pH=
(3)某温度(t℃)下的溶液中,c(H+)=10-xmol/L,c(OH-)=10-ymol/L,x与y的关系如图所示,此温度时,水的离子积常数Kw为

(4)25℃时,pH=3的酸酸溶液和pH=11的NaOH溶液中由水电离出的c(H+)之比为
您最近一年使用:0次
名校
2 . 兴趣小组为探究FeCl3在溶液中显黄色的原因,进行如下实验。
下列说法不正确 的是
| 序号 | 操作 | 试剂a | 试剂b | 现象 |
| ① | 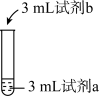 | 0.2mol/L FeCl3 | 蒸馏水 | 溶液为黄色 |
| ② | 0.2mol/L FeCl3 | 2mol/L盐酸 | 溶液为浅黄色 | |
| ③ | 0.2mol/L Fe(NO3)3 | 蒸馏水 | 溶液为浅黄色 | |
| ④ | 0.2mol/L Fe(NO3)3 | 2mol/L硝酸 | 溶液接近无色 |
| A.②中的溶液颜色比①中的浅,主要是因为Fe3+的水解平衡逆向移动 |
| B.由③④可知,Fe(NO3)3溶液显浅黄色与Fe3+水解有关 |
| C.由以上实验可推知,FeCl3溶液显黄色与Fe3+水解、Cl-存在均有关 |
| D.由以上实验可推知,导致②③溶液均为浅黄色的原因相同 |
您最近一年使用:0次
2023-11-02更新
|
376次组卷
|
6卷引用:北京市海淀区2023-2024学年高三上学期期中测试化学试题
名校
3 .  溶液中存在水解平衡:
溶液中存在水解平衡: 。下列说法错误的是
。下列说法错误的是
 溶液中存在水解平衡:
溶液中存在水解平衡: 。下列说法错误的是
。下列说法错误的是A.通入 ,溶液pH减小 ,溶液pH减小 | B.升高温度,平衡常数增大 |
| C.加水稀释,溶液中所有离子的浓度都减小 | D.加入 固体, 固体,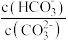 减小 减小 |
您最近一年使用:0次
2023-10-28更新
|
631次组卷
|
4卷引用:北京市第三中学2023-2024学年高二上学期期中练习化学试题
名校
解题方法
4 . 测定0.1
 溶液先升温再降温过程中的pH,数据如下表:
溶液先升温再降温过程中的pH,数据如下表:
实验过程中,取①、④时刻的溶液,加入盐酸酸化的 溶液做对比实验,④产生白色沉
溶液做对比实验,④产生白色沉
淀多。下列说法不正确 的是

 溶液先升温再降温过程中的pH,数据如下表:
溶液先升温再降温过程中的pH,数据如下表:时刻 | ① | ② | ③ | ④ |
温度/℃ | 25 | 30 | 40 | 25 |
pH | 9.66 | 9.52 | 9.37 | 9.25 |
 溶液做对比实验,④产生白色沉
溶液做对比实验,④产生白色沉淀多。下列说法
A. 溶液中共有7种微粒 溶液中共有7种微粒 |
B.④产生的白色沉淀是 |
C.①与④的 值相等 值相等 |
D.①→③的过程中,温度对水解平衡的影响比 的影响更大 的影响更大 |
您最近一年使用:0次
名校
解题方法
5 . 下列说法正确的是
| A.一般情况下,盐类越稀越易水解,所以稀释盐溶液,Kh(水解平衡常数)变大 |
| B.一般情况下,一元弱碱的Kb值越大碱性越弱 |
| C.Kw随着溶液中c(H+)和c(OH-)的改变而改变 |
| D.一般情况下,Ksp越大,难溶电解质在水中的溶解程度就越高 |
您最近一年使用:0次
2022-02-19更新
|
132次组卷
|
2卷引用:北京市怀柔区2021-2022学年高二上学期期末考试化学试题
名校
6 . 探究铝片与 溶液的反应。
溶液的反应。
下列说法不正确的是
 溶液的反应。
溶液的反应。| 实验 | 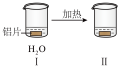 |  |
| 现象 | 无明显现象 | Ⅲ中铝片表面产生细小气泡 Ⅳ中出现白色浑浊,产生大量气泡(经检验为  和 和 ) ) |
A. 溶液中存在水解平衡: 溶液中存在水解平衡: |
B.若将打磨过的铝片加入Ⅰ中,加热后会出现气泡。再对比上图Ⅰ、Ⅲ,说明 溶液能破坏铝表面的保护膜 溶液能破坏铝表面的保护膜 |
C.推测出现白色浑浊的原因可能为: |
D.加热和 逸出对 逸出对 水解平衡移动方向的影响是相反的 水解平衡移动方向的影响是相反的 |
您最近一年使用:0次
2021-06-29更新
|
203次组卷
|
3卷引用: 北京市回民学校2023-2024学年高三上学期统练二化学试题
北京市回民学校2023-2024学年高三上学期统练二化学试题浙江省湖州市2020-2021学年高二下学期期末调研测试卷化学试题(已下线)3.3.2 影响盐类水解的因素-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)
名校
解题方法
7 . 有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)氧化成硫酸盐。运用该原理生产铜和绿矾(FeSO4﹒7H2O)的流程如下:
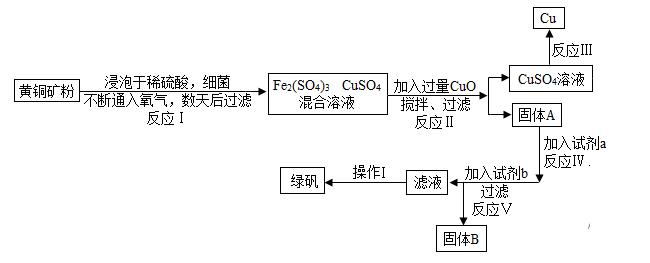
(1)已知:
加入CuO将溶液的pH调节到约为4,用平衡移动原理解释该操作的原因________ 。
(2)写出能实现反应III的化学方程式_______________ 。
(3)试剂b为___________________ 。
(4)反应|的化学方程式_______________________ 。

(1)已知:
| Fe2+ | Cu2+ | Fe3+ | |
| 开始转化为氢氧化物沉淀时的PH | 7.6 | 4.7 | 2.7 |
| 完全转化为氢氧化物沉淀时的PH | 9.6 | 6.7 | 3.7 |
加入CuO将溶液的pH调节到约为4,用平衡移动原理解释该操作的原因
(2)写出能实现反应III的化学方程式
(3)试剂b为
(4)反应|的化学方程式
您最近一年使用:0次
名校
解题方法
8 . 常温下,某溶液由amol/LCH3COONa和bmol/LCH3COOH组成的混合液,下列说法中正确的是( )
| A.该溶液一定呈酸性 | B.该溶液一定呈碱性 |
| C.该溶液一定呈中性 | D.CH3COONa会抑制CH3COOH的电离 |
您最近一年使用:0次
2020-07-05更新
|
116次组卷
|
2卷引用:北京市顺义区2019—2020学年高二下学期期末质量检测化学试题
名校
解题方法
9 . 下列叙述正确的是
| A.Na2CO3 溶液加水稀释后,恢复至原温度,pH 和 Kw 均减小 |
| B.0.1mol/L CH3COONa 溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C.在 KI 溶液中加入 AgCl 固体,溶液中 c(I-)减小 |
| D.室温下,pH=5 的 CH3COOH 溶液和 pH=5 的 NH4Cl 溶液中,溶液中 c(H+)不相等 |
您最近一年使用:0次
名校
10 . 下列各项比较中,一定相等的是
| A.相同质量的 Fe 完全转化为FeCl2和FeCl3 时转移的电子数 |
| B.相同质量的苯和乙炔所含的碳原子的数目 |
| C.标准状况下的 2.24 L HCl 气体和1 L 0.1 mol·L−1盐酸中所含Cl−的数目 |
D.相同物质的量浓度的NH4Cl和(NH4)2Fe(SO4)2溶液中 NH 的浓度 的浓度 |
您最近一年使用:0次
2020-07-01更新
|
89次组卷
|
2卷引用:北京市海淀区北京大学附中2020 届高三化学阶段性测试化学试题



