名校
1 . 碱式碳酸锰[Mn2(OH)2CO3]是一种不溶于水的固体,是制造其他含锰化合物的原料。工业上以方锰矿(主要成分为 MnO,还含有少量的 Fe3O4、Al2O3、CaO、SiO2)为原料制备碱式碳酸锰。
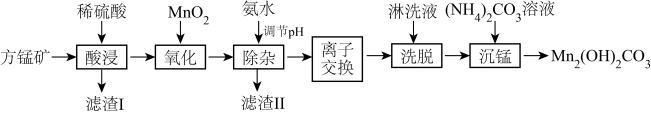
25℃时,相关物质的 Ksp如下表:
回答下列问题:
(1)“酸浸”时,滤渣I的成分是___________ (填化学式)。
(2)“氧化”时,该反应的离子方程式为___________ 。
(3)“除杂”时,使用氨水的目的是将 Fe3+和Al3+转化为沉淀而除去,则应调节溶液的pH≥______ ;若 A13+沉淀完全时,则溶液中 Fe3+的物质的量浓度为___________ mol·L-1(通常认为溶液中的离子浓度≤1×10-5mol·L-1沉淀完全)
(4)“离子交换”和“洗脱”时,发生反应:Mn2+ +2HR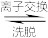 MnR2 +2H+(HR 是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应为
MnR2 +2H+(HR 是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应为___________ (填“硫酸”、“氢氧化钠溶液”或“蒸馏水”)。
(5)“沉锰”时,反应的离子方程式为___________ ,过滤、洗涤、干燥,得到Mn2(OH)2CO3,检验沉淀是否洗涤干净的操作是___________ 。
(6)为测定产品中锰的含量,取 a g 样品于烧杯中,加水溶解,加入足量的稀硫酸溶解,滴加过量的 0.1000 mol·L-1(NH4)2S2O8溶液将锰元素转化为 MnO ,充分反应后加热一段时间,冷却将烧杯中的溶液全部转移至 250mL 容量瓶中。取 25.00mL 于锥形瓶中,用0.1000mol·L-1FeSO4标准溶液滴定,达滴定终点时,消耗 FeSO4溶液的体积为 V mL。
,充分反应后加热一段时间,冷却将烧杯中的溶液全部转移至 250mL 容量瓶中。取 25.00mL 于锥形瓶中,用0.1000mol·L-1FeSO4标准溶液滴定,达滴定终点时,消耗 FeSO4溶液的体积为 V mL。
①滴定终点的现象是___________ 。
②该产品中锰的质量分数为___________ 。(用含 a、V 的式子表示)。

25℃时,相关物质的 Ksp如下表:
| 物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ca(OH)2 |
| Ksp | 2×10-13 | 5×10-17 | 3×10-39 | 1×10-32 | 6×10-6 |
(1)“酸浸”时,滤渣I的成分是
(2)“氧化”时,该反应的离子方程式为
(3)“除杂”时,使用氨水的目的是将 Fe3+和Al3+转化为沉淀而除去,则应调节溶液的pH≥
(4)“离子交换”和“洗脱”时,发生反应:Mn2+ +2HR
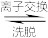 MnR2 +2H+(HR 是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应为
MnR2 +2H+(HR 是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应为(5)“沉锰”时,反应的离子方程式为
(6)为测定产品中锰的含量,取 a g 样品于烧杯中,加水溶解,加入足量的稀硫酸溶解,滴加过量的 0.1000 mol·L-1(NH4)2S2O8溶液将锰元素转化为 MnO
 ,充分反应后加热一段时间,冷却将烧杯中的溶液全部转移至 250mL 容量瓶中。取 25.00mL 于锥形瓶中,用0.1000mol·L-1FeSO4标准溶液滴定,达滴定终点时,消耗 FeSO4溶液的体积为 V mL。
,充分反应后加热一段时间,冷却将烧杯中的溶液全部转移至 250mL 容量瓶中。取 25.00mL 于锥形瓶中,用0.1000mol·L-1FeSO4标准溶液滴定,达滴定终点时,消耗 FeSO4溶液的体积为 V mL。①滴定终点的现象是
②该产品中锰的质量分数为
您最近半年使用:0次
2022-06-01更新
|
603次组卷
|
3卷引用:山西省太原市第五中学校2022届高三下学期二模理综化学试题
名校
2 . H2O2是一种绿色氧化还原试剂,在化学研究中应用广泛。某研究性学习小组设计如图所示实验装置,探究影响H2O2分解反应速率的因素。
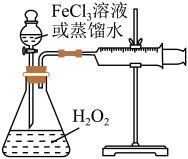
(1)①写出锥形瓶中反应的化学方程式________ 。
②设计实验方案:在不同条件下,测定_______ 。(要求所测得的数据能直接体现反应速率大小)
(2)探究影响H2O2分解反应速率的因素实验方案如下表所示,先向锥形瓶中加入质量分数为10%H2O2,再依次通过分液漏斗向锥形瓶中加入一定量的蒸馏水和FeCl3溶液,请回答问题:
①表格中a=_______ ,b=________ 。
②通过实验Ⅱ和Ⅲ探究浓度对反应速率影响。
(3)实验Ⅱ、Ⅲ中溶液颜色变深的原因是________ 。
(4)已知FeCl3溶液对H2O2的催化分解分为反应i和反应ii两步进行:
已知反应ii的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O;
①反应i离子方程式为_______ 。
②某同学设计实验证明催化过程中有Fe2+产生:取2mLH2O2溶液于试管中,向试管中滴加2滴FeCl3溶液,再滴加2滴_______ 溶液,产生蓝色沉淀。
(5)向实验Ⅱ中反应后的溶液滴加KSCN溶液,溶液变红色,2min后溶液红色褪去;继续滴加KSCN溶液,溶液又变红色,一段时间后又褪色;此时再向溶液中滴加盐酸酸化后的BaCl2溶液,产生白色沉淀。请分析溶液红色褪去的原因______ 。

(1)①写出锥形瓶中反应的化学方程式
②设计实验方案:在不同条件下,测定
(2)探究影响H2O2分解反应速率的因素实验方案如下表所示,先向锥形瓶中加入质量分数为10%H2O2,再依次通过分液漏斗向锥形瓶中加入一定量的蒸馏水和FeCl3溶液,请回答问题:
| 实验序号 | 10%H2O2/mL | 蒸馏水/mL | 0.2mol·LFeCl3溶液/mL | 现象 |
| I | 10 | a | 0 | 无明显变化 |
| Ⅱ | 10 | b | 2 | 锥形瓶变热,溶液迅速变红棕色,并有较多气泡产生;2min时,反应变缓,溶液颜色明显变浅 |
| Ⅲ | 5 | 5 | 2 | 锥形瓶变热,溶液变棕色,开始5s后产生较少的气泡;2min时,反应速度加快 |
②通过实验Ⅱ和Ⅲ探究浓度对反应速率影响。
(3)实验Ⅱ、Ⅲ中溶液颜色变深的原因是
(4)已知FeCl3溶液对H2O2的催化分解分为反应i和反应ii两步进行:
已知反应ii的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O;
①反应i离子方程式为
②某同学设计实验证明催化过程中有Fe2+产生:取2mLH2O2溶液于试管中,向试管中滴加2滴FeCl3溶液,再滴加2滴
(5)向实验Ⅱ中反应后的溶液滴加KSCN溶液,溶液变红色,2min后溶液红色褪去;继续滴加KSCN溶液,溶液又变红色,一段时间后又褪色;此时再向溶液中滴加盐酸酸化后的BaCl2溶液,产生白色沉淀。请分析溶液红色褪去的原因
您最近半年使用:0次
名校
解题方法
3 . 近日,科学家利用光催化剂 实现高选择性制备氢气。某小组以辉铋矿(主要成分是
实现高选择性制备氢气。某小组以辉铋矿(主要成分是 ,含少量
,含少量 、Bi、
、Bi、 和
和 等杂质)为原料制备钒酸铋(
等杂质)为原料制备钒酸铋( )的流程如下:
)的流程如下:

已知:
①滤液1中所含阳离子主要有 、
、 、
、 和
和 。
。
②几种氢氧化物沉淀的pH如表所示。
回答下列问题:
(1)滤渣2的主要成分是_______ (填化学式)。将辉铋矿粉碎过筛制成矿粉,其目的是_______ 。
(2)“酸洗”中用盐酸代替水的目的是_______ 。滤液3可以循环用于“_______ ”工序(填名称)。
(3)“氯化”的化学方程式为_______ 。
(4)“合成”过程中将 溶液和
溶液和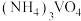 溶液混合容易形成
溶液混合容易形成 胶体,导致过滤困难。为防止生成胶体可采用的措施为
胶体,导致过滤困难。为防止生成胶体可采用的措施为_______ (任答一条)。
(5)已知辉铋矿中所含Bi元素的质量分数为a%,wt这种矿石经上述转化最终制得b kg ,则铋的收率为
,则铋的收率为_______ %( )。
)。
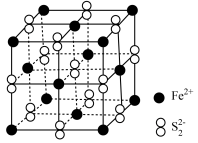
(6) 的立方晶胞结构如图所示。已知晶体密度为
的立方晶胞结构如图所示。已知晶体密度为 ,设
,设 为阿伏加德罗常数的值,则该晶体中与
为阿伏加德罗常数的值,则该晶体中与 距离最近且相等的
距离最近且相等的 有
有_______ 个,相邻2个 的核间距为
的核间距为_______ nm。
 实现高选择性制备氢气。某小组以辉铋矿(主要成分是
实现高选择性制备氢气。某小组以辉铋矿(主要成分是 ,含少量
,含少量 、Bi、
、Bi、 和
和 等杂质)为原料制备钒酸铋(
等杂质)为原料制备钒酸铋( )的流程如下:
)的流程如下:
已知:
①滤液1中所含阳离子主要有
 、
、 、
、 和
和 。
。②几种氢氧化物沉淀的pH如表所示。
| 氢氧化物 |  |  |  |
| 开始沉淀pH | 7.5 | 2.3 | 4.0 |
| 沉淀完全pH | 9.7 | 3.7 |
(1)滤渣2的主要成分是
(2)“酸洗”中用盐酸代替水的目的是
(3)“氯化”的化学方程式为
(4)“合成”过程中将
 溶液和
溶液和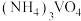 溶液混合容易形成
溶液混合容易形成 胶体,导致过滤困难。为防止生成胶体可采用的措施为
胶体,导致过滤困难。为防止生成胶体可采用的措施为(5)已知辉铋矿中所含Bi元素的质量分数为a%,wt这种矿石经上述转化最终制得b kg
 ,则铋的收率为
,则铋的收率为 )。
)。(6)
 的立方晶胞结构如图所示。已知晶体密度为
的立方晶胞结构如图所示。已知晶体密度为 ,设
,设 为阿伏加德罗常数的值,则该晶体中与
为阿伏加德罗常数的值,则该晶体中与 距离最近且相等的
距离最近且相等的 有
有 的核间距为
的核间距为
您最近半年使用:0次
名校
4 . 无水 是一种重要的化工原料,其熔点306℃、沸点316℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。一般采用低共熔混合物反应法(熔融法)制备高纯度的三氯化铁,其模拟反应装置如下:
是一种重要的化工原料,其熔点306℃、沸点316℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。一般采用低共熔混合物反应法(熔融法)制备高纯度的三氯化铁,其模拟反应装置如下:
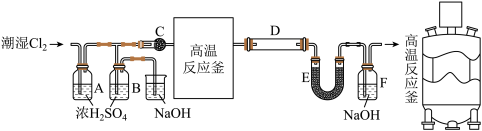
实验过程:在一个带有耐酸衬里的反应器中(即图中的高温反应釜),将70% 和30%KCl在600℃下共熔。再将铁屑溶解于共熔物中,再通入干燥氯气。反应生成的升华后导出,再经冷凝收集。
和30%KCl在600℃下共熔。再将铁屑溶解于共熔物中,再通入干燥氯气。反应生成的升华后导出,再经冷凝收集。
回答下列问题:
(1)C装置的名称为_______ ;
(2)当氯气通入时,A中有酸雾产生。为吸收酸雾,C中应盛放的物质为_______;(填字母)
(3)高温反应釜中发生反应的化学方程式为_______ ;
(4)E装置的作用为_______ ;
(5)为研究 的性质,某化学兴趣小组取一定质量的
的性质,某化学兴趣小组取一定质量的 (摩尔质量为
(摩尔质量为 )在惰性气体保护下受热分解时,所得固体产物的剩余质量分数(剩余质量与原样品质量的百分比)随温度变化的曲线如图所示。试利用图中信息并结合所学的知识,回答下列各问题:
)在惰性气体保护下受热分解时,所得固体产物的剩余质量分数(剩余质量与原样品质量的百分比)随温度变化的曲线如图所示。试利用图中信息并结合所学的知识,回答下列各问题:

已知:A为红褐色固体,B中含有三种元素,C为红棕色固体,D为黑色固体。
①固体产物的化学式B是_______ ,D是_______ ;
②由C得到D的化学方程式为_______ 。
 是一种重要的化工原料,其熔点306℃、沸点316℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。一般采用低共熔混合物反应法(熔融法)制备高纯度的三氯化铁,其模拟反应装置如下:
是一种重要的化工原料,其熔点306℃、沸点316℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。一般采用低共熔混合物反应法(熔融法)制备高纯度的三氯化铁,其模拟反应装置如下:
实验过程:在一个带有耐酸衬里的反应器中(即图中的高温反应釜),将70%
 和30%KCl在600℃下共熔。再将铁屑溶解于共熔物中,再通入干燥氯气。反应生成的升华后导出,再经冷凝收集。
和30%KCl在600℃下共熔。再将铁屑溶解于共熔物中,再通入干燥氯气。反应生成的升华后导出,再经冷凝收集。回答下列问题:
(1)C装置的名称为
(2)当氯气通入时,A中有酸雾产生。为吸收酸雾,C中应盛放的物质为_______;(填字母)
A. | B.CaO | C. | D.NaOH |
(4)E装置的作用为
(5)为研究
 的性质,某化学兴趣小组取一定质量的
的性质,某化学兴趣小组取一定质量的 (摩尔质量为
(摩尔质量为 )在惰性气体保护下受热分解时,所得固体产物的剩余质量分数(剩余质量与原样品质量的百分比)随温度变化的曲线如图所示。试利用图中信息并结合所学的知识,回答下列各问题:
)在惰性气体保护下受热分解时,所得固体产物的剩余质量分数(剩余质量与原样品质量的百分比)随温度变化的曲线如图所示。试利用图中信息并结合所学的知识,回答下列各问题:
已知:A为红褐色固体,B中含有三种元素,C为红棕色固体,D为黑色固体。
①固体产物的化学式B是
②由C得到D的化学方程式为
您最近半年使用:0次
2022-11-03更新
|
421次组卷
|
3卷引用:湖北省鄂东南联盟2022-2023学年高三上学期期中联考化学试题
名校
5 . 硫酸铜主要用作纺织品媒染剂、农业杀虫剂等,其晶体(CuSO4·xH2O)在不同温度下会逐步失去结晶水甚至分解。某小组对硫酸铜晶体性质进行探究,回答下列问题:
[探究一]验证硫酸铜晶体的分解产物
某小组同学对某温度下硫酸铜晶体的分解产物进行验证,设计了如下实验:
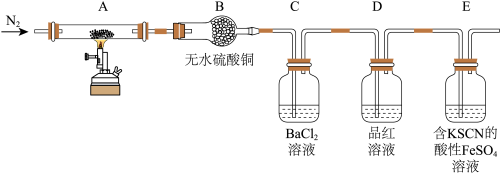
观察到的实验现象有:A中蓝色晶体逐渐变成白色粉末,最后变成黑色粉末;B中无水硫酸铜变蓝;C中产生白色沉淀;D中品红溶液褪色;E中溶液变为红色。
(1)装有无水硫酸铜的仪器名称为_______ ,C、D两装置位置_______ (填“ 能”或“不能”)交换。
(2)C中产生的沉淀的化学式为_______ ,E中Fe2+发生反应的离子方程式为______ 。
(3)该实验设计的不足之处是_______ 。
[探究二]测定硫酸铜晶体中结晶水含量
实验步骤:①称取mg硫酸铜晶体,用适量蒸馏水溶解,再滴加几滴酸A酸化。
②向①所得溶液中滴加足量BaCl2溶液,得到白色沉淀,将所得沉淀过滤、洗涤。
③将洗涤后的沉淀充分干燥后称得其质量为ag。
(4)步骤①酸A应该选择_______ ( 填“稀盐酸”或者“稀硫酸”),滴加酸A的目的是______ 。
(5)步骤②检验沉淀是否洗涤干净的方法是_______ 。
(6)根据实验数据,硫酸铜晶体( CuSO4·xH2O)中x=_______ (用含 m、a的代数式表示)。
[探究一]验证硫酸铜晶体的分解产物
某小组同学对某温度下硫酸铜晶体的分解产物进行验证,设计了如下实验:

观察到的实验现象有:A中蓝色晶体逐渐变成白色粉末,最后变成黑色粉末;B中无水硫酸铜变蓝;C中产生白色沉淀;D中品红溶液褪色;E中溶液变为红色。
(1)装有无水硫酸铜的仪器名称为
(2)C中产生的沉淀的化学式为
(3)该实验设计的不足之处是
[探究二]测定硫酸铜晶体中结晶水含量
实验步骤:①称取mg硫酸铜晶体,用适量蒸馏水溶解,再滴加几滴酸A酸化。
②向①所得溶液中滴加足量BaCl2溶液,得到白色沉淀,将所得沉淀过滤、洗涤。
③将洗涤后的沉淀充分干燥后称得其质量为ag。
(4)步骤①酸A应该选择
(5)步骤②检验沉淀是否洗涤干净的方法是
(6)根据实验数据,硫酸铜晶体( CuSO4·xH2O)中x=
您最近半年使用:0次
2023-03-22更新
|
372次组卷
|
3卷引用:四川省凉山彝族自治州2023届高三下学期第二次诊断检测理科综合化学试题
解题方法
6 . 新冠疫情期间,家庭常备84消毒液、医用酒精等。某瓶84消毒液所贴标签的部分内容见图。有关该瓶消毒液的说法正确的是
84 消毒液 [用途]适用于一般物品的表面消毒,含餐具、果蔬、白色织物等。可杀灭肠道致病菌、化脓性球菌。 [性状]无色透明液体 [有效成分]次氯酸 [规格]500mL/瓶,约505g [含量]氯含量为 6.00% [贮藏]阴凉处密封保存 |
| A.每瓶消毒液含次氯酸钠约505g |
| B.消毒液的密度为1.10g⋅cm-3 |
| C.密封保存的目的是防止次氯酸钠见光分解 |
D.每瓶消毒液中含氯微粒的物质的量浓度约为1.71 |
您最近半年使用:0次
名校
7 . 国家规定,排放的废水中氟的含量不得超过10.0mg·L-1,砷的含量不得超过0.5mg·L-1。硫酸工厂废水中除含有稀硫酸外,还含有H3AsO3、H2SiF6等物质。工业上常通过化学沉淀和氧化、吸附沉降处理废水,实现水体达标排放。
(1)化学沉淀:向废水中加入石灰乳[以Ca(OH)2为主]、过滤。滤渣中主要含有CaSO4、CaF2、SiO2和少量Ca3(AsO3)2。
①写出该过程中H2SiF6和石灰乳反应生成CaF2、SiO2的化学方程式:____ 。
②充分沉淀后测得废水中F-的含量为9.5mg·L-1,此时SO 的浓度为
的浓度为____ mol·L-1。[已知:Ksp(CaSO4)=5.0×10-5,Ksp(CaF2)=5.0×10-9]
(2)氧化、吸附沉降:利用NaClO和FeSO4进一步处理废水中残余的As(III)。
已知:i.NaClO能将As(III)氧化为As(V)、Fe(II)氧化为Fe(III)。形成的Fe(OH)3胶体吸附废水中的As(V)物种而沉降。
ii.溶液的pH对Fe(OH)3胶体表面所带电荷有影响。pH>7时,Fe(OH)3胶体表面带负电荷,pH越高,表面所带负电荷越多。
iii.As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。
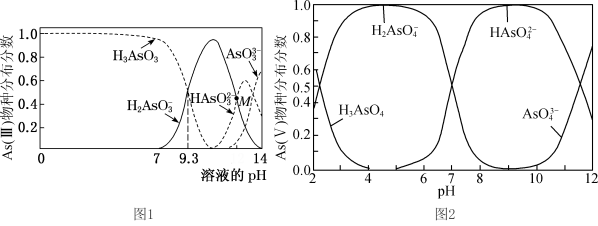
①向化学沉淀后的废水(pH≈8)中加入NaClO溶液,写出As(III)发生主要反应的离子方程式:____ 。
②H3AsO3第一步电离的电离常数为Ka1,则pKa1=____ (pKa1=-lgKa1)。
③如图1为向0.1mol/LH3AsO3溶液逐滴加入KOH溶液,含砷物种的分布分数图,下列说法正确的是____ 。
A.当n(H3AsO3):n(H2AsO )=1:1时,溶液呈碱性
)=1:1时,溶液呈碱性
B.pH在8.0~10.0时,反应的离子方程式为:H3AsO3+OH-=H2AsO +H2O
+H2O
C.M点对应的溶液中:c(H2AsO )+c(HAsO
)+c(HAsO )+c(AsO
)+c(AsO )+c(H3AsO3)=0.1mol·L-1
)+c(H3AsO3)=0.1mol·L-1
D.pH=12时,溶液中:c(H2AsO )+2c(HAsO
)+2c(HAsO )+3c(AsO
)+3c(AsO )+c(H3AsO3)>c(H+)+c(K+)
)+c(H3AsO3)>c(H+)+c(K+)
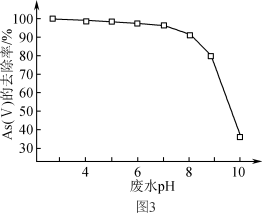
④废水的pH对As(V)的去除率的影响如图3所示。pH>8时,随着废水的pH增大,As(V)的去除率发生如图所示变化的原因是____ 。
(1)化学沉淀:向废水中加入石灰乳[以Ca(OH)2为主]、过滤。滤渣中主要含有CaSO4、CaF2、SiO2和少量Ca3(AsO3)2。
①写出该过程中H2SiF6和石灰乳反应生成CaF2、SiO2的化学方程式:
②充分沉淀后测得废水中F-的含量为9.5mg·L-1,此时SO
 的浓度为
的浓度为(2)氧化、吸附沉降:利用NaClO和FeSO4进一步处理废水中残余的As(III)。
已知:i.NaClO能将As(III)氧化为As(V)、Fe(II)氧化为Fe(III)。形成的Fe(OH)3胶体吸附废水中的As(V)物种而沉降。
ii.溶液的pH对Fe(OH)3胶体表面所带电荷有影响。pH>7时,Fe(OH)3胶体表面带负电荷,pH越高,表面所带负电荷越多。
iii.As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。

①向化学沉淀后的废水(pH≈8)中加入NaClO溶液,写出As(III)发生主要反应的离子方程式:
②H3AsO3第一步电离的电离常数为Ka1,则pKa1=
③如图1为向0.1mol/LH3AsO3溶液逐滴加入KOH溶液,含砷物种的分布分数图,下列说法正确的是
A.当n(H3AsO3):n(H2AsO
 )=1:1时,溶液呈碱性
)=1:1时,溶液呈碱性B.pH在8.0~10.0时,反应的离子方程式为:H3AsO3+OH-=H2AsO
 +H2O
+H2OC.M点对应的溶液中:c(H2AsO
 )+c(HAsO
)+c(HAsO )+c(AsO
)+c(AsO )+c(H3AsO3)=0.1mol·L-1
)+c(H3AsO3)=0.1mol·L-1D.pH=12时,溶液中:c(H2AsO
 )+2c(HAsO
)+2c(HAsO )+3c(AsO
)+3c(AsO )+c(H3AsO3)>c(H+)+c(K+)
)+c(H3AsO3)>c(H+)+c(K+)④废水的pH对As(V)的去除率的影响如图3所示。pH>8时,随着废水的pH增大,As(V)的去除率发生如图所示变化的原因是

您最近半年使用:0次
8 . 氯化钯是一种重要的催化剂,在石油化工和汽车尾气转化中应用广泛。钯(Pd)是一种不活泼金属,具有优良的吸氢功能,其氢氧化物具有两性。工业上采用如下图流程从固体二氯二氨合钯[Pd(NH3)2Cl2]中提取钯。
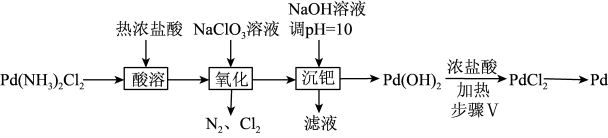
(1)为了加快“酸溶”的速率,可以采用哪些措施_______ (写出两条)。
(2)Pd(NH3)2Cl2中提供电子对形成配位键的原子是_______ (填元素符号)。
(3)“酸溶”生成(NH4)2PdCl4,“氧化”后,钯仍以PdCl 形式存在,则“氧化”过程中生成Cl2和N2的离子方程式为
形式存在,则“氧化”过程中生成Cl2和N2的离子方程式为_______ 。
(4)加NaOH溶液需控制pH=10,如pH>10,滤液中钯含量升高,其原因为_______ 。
(5)“步骤V”中需加浓盐酸并加热至100°C浓缩直至蒸干,加浓盐酸的目的是_______ 。
(6)已知金属钯密度为12.0g·cm-3,标准状况下,吸附的氢气是其体积的900倍,则此条件下钯的吸附容量R=_______ mL·g-1[R为单位质量(g)的钯所吸附氢气的体积(mL)]。

(1)为了加快“酸溶”的速率,可以采用哪些措施
(2)Pd(NH3)2Cl2中提供电子对形成配位键的原子是
(3)“酸溶”生成(NH4)2PdCl4,“氧化”后,钯仍以PdCl
 形式存在,则“氧化”过程中生成Cl2和N2的离子方程式为
形式存在,则“氧化”过程中生成Cl2和N2的离子方程式为(4)加NaOH溶液需控制pH=10,如pH>10,滤液中钯含量升高,其原因为
(5)“步骤V”中需加浓盐酸并加热至100°C浓缩直至蒸干,加浓盐酸的目的是
(6)已知金属钯密度为12.0g·cm-3,标准状况下,吸附的氢气是其体积的900倍,则此条件下钯的吸附容量R=
您最近半年使用:0次
名校
解题方法
9 . 研究 、
、 等大气污染物的处理具有重要意义。
等大气污染物的处理具有重要意义。
(1)某温度下,已知:
①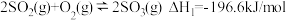
②
③
则
________ 。
(2)按投料比2∶1把 和
和 加入到一密闭容器中发生反应
加入到一密闭容器中发生反应 ,测得平衡时
,测得平衡时 的转化率的温度T、压强p的关系如图甲所示:
的转化率的温度T、压强p的关系如图甲所示:
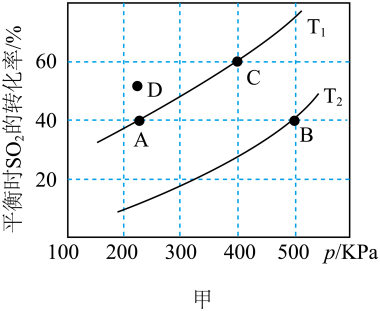
A、B两点对应的平衡常数大小关系为KA_______ KB(填“>”“<”或“=”,下同);温度为 时D点
时D点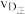 与
与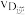 的大小关系为
的大小关系为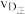
________ 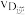 ;
;
(3)恒温恒容下,对于反应 ,测得平衡时
,测得平衡时 的体积分数与起始
的体积分数与起始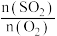 的关系如图乙所示,则当
的关系如图乙所示,则当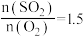 达到平衡状态时,
达到平衡状态时,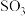 的体积分数是图乙中D、E、F三点中的
的体积分数是图乙中D、E、F三点中的_______ 点。A、B两点 转化率的大小关系为
转化率的大小关系为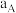
_______ (填“>”“<”或“=”) 。
。

(4)工业上脱硫脱硝还可采用电化学法,其中的一种方法是内电池模式(直接法),烟气中的组分直接在电池液中被吸收及在电极反应中被转化,采用内电池模式将 吸收在电池液中,并在电极反应中氧化为硫酸,在此反应过程中可得到质量分数为40%的硫酸。写出通入
吸收在电池液中,并在电极反应中氧化为硫酸,在此反应过程中可得到质量分数为40%的硫酸。写出通入 电极的反应式:
电极的反应式:_________ ;若40%的硫酸溶液吸收氨气获得 的稀溶液,测得常温下,该溶液的
的稀溶液,测得常温下,该溶液的 ,则
,则
________ (列出计算式已知该温度下 的
的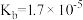 );若将该溶液蒸发掉一部分水后恢复室温,则
);若将该溶液蒸发掉一部分水后恢复室温,则 的值将
的值将_________ (填“变大”“不变”或“变小”)。
 、
、 等大气污染物的处理具有重要意义。
等大气污染物的处理具有重要意义。(1)某温度下,已知:
①
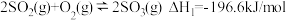
②

③

则

(2)按投料比2∶1把
 和
和 加入到一密闭容器中发生反应
加入到一密闭容器中发生反应 ,测得平衡时
,测得平衡时 的转化率的温度T、压强p的关系如图甲所示:
的转化率的温度T、压强p的关系如图甲所示:
A、B两点对应的平衡常数大小关系为KA
 时D点
时D点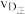 与
与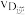 的大小关系为
的大小关系为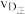
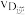 ;
;(3)恒温恒容下,对于反应
 ,测得平衡时
,测得平衡时 的体积分数与起始
的体积分数与起始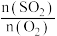 的关系如图乙所示,则当
的关系如图乙所示,则当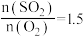 达到平衡状态时,
达到平衡状态时,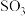 的体积分数是图乙中D、E、F三点中的
的体积分数是图乙中D、E、F三点中的 转化率的大小关系为
转化率的大小关系为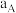
 。
。
(4)工业上脱硫脱硝还可采用电化学法,其中的一种方法是内电池模式(直接法),烟气中的组分直接在电池液中被吸收及在电极反应中被转化,采用内电池模式将
 吸收在电池液中,并在电极反应中氧化为硫酸,在此反应过程中可得到质量分数为40%的硫酸。写出通入
吸收在电池液中,并在电极反应中氧化为硫酸,在此反应过程中可得到质量分数为40%的硫酸。写出通入 电极的反应式:
电极的反应式: 的稀溶液,测得常温下,该溶液的
的稀溶液,测得常温下,该溶液的 ,则
,则
 的
的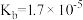 );若将该溶液蒸发掉一部分水后恢复室温,则
);若将该溶液蒸发掉一部分水后恢复室温,则 的值将
的值将
您最近半年使用:0次
10 . 水体中氮含量过高会对水中生物构成安全威胁,氨氮硝氮是氮的主要存在形态。
(1)某工业氨氮废水的处理流程如下图所示:
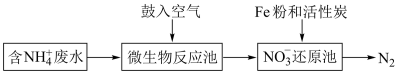
①写出“微生物反应池”中反应的离子方程式:___________ 。
②“NO 还原池”通过形成铁碳原电池对废水中的NO
还原池”通过形成铁碳原电池对废水中的NO 等进行处理,写出NO
等进行处理,写出NO 在正极发生的电极反应:
在正极发生的电极反应:___________ 。
(2)向氨氮废水中加入NaClO,可以将NH 最终氧化为N2。NaClO除去水中氨氮的反应过程如下:
最终氧化为N2。NaClO除去水中氨氮的反应过程如下:
i.ClO—+H2O OH-+HClO
OH-+HClO
ii.NH +H2O
+H2O NH3·H2O+H+
NH3·H2O+H+
ii.NH3·H2O+HClO=NH2Cl+2H2O
iv.……
v.H++OH—=H2O
①写出反应iv的离子方程式:___________ 。
②废水中氨氮去除率与初始pH有关。保持其他条件不变,随初始pH的升高,溶液中c(HClO)___________ (填“增大”“不变”或“减小”,下同),c(NH3·H2O)___________ 。
③研究发现,保持其他条件相同,废水中氨氮去除率随温度的升高先升高后降低。当温度>35℃时,氨氮去除率随溶液温度升高而降低的原因可能是___________ (答一条)。
(3)利用双离子交换膜电解法可以处理含NH4NO3的工业废水,并获得氨水和硝酸,原理如图所示:
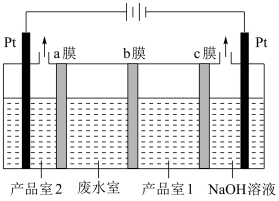
b膜属于___________ (填“阴”或“阳”)离子交换膜;为增强溶液的导电性,电解前产品室2中的溶液应是___________ 。
(1)某工业氨氮废水的处理流程如下图所示:

①写出“微生物反应池”中反应的离子方程式:
②“NO
 还原池”通过形成铁碳原电池对废水中的NO
还原池”通过形成铁碳原电池对废水中的NO 等进行处理,写出NO
等进行处理,写出NO 在正极发生的电极反应:
在正极发生的电极反应:(2)向氨氮废水中加入NaClO,可以将NH
 最终氧化为N2。NaClO除去水中氨氮的反应过程如下:
最终氧化为N2。NaClO除去水中氨氮的反应过程如下:i.ClO—+H2O
 OH-+HClO
OH-+HClOii.NH
 +H2O
+H2O NH3·H2O+H+
NH3·H2O+H+ii.NH3·H2O+HClO=NH2Cl+2H2O
iv.……
v.H++OH—=H2O
①写出反应iv的离子方程式:
②废水中氨氮去除率与初始pH有关。保持其他条件不变,随初始pH的升高,溶液中c(HClO)
③研究发现,保持其他条件相同,废水中氨氮去除率随温度的升高先升高后降低。当温度>35℃时,氨氮去除率随溶液温度升高而降低的原因可能是
(3)利用双离子交换膜电解法可以处理含NH4NO3的工业废水,并获得氨水和硝酸,原理如图所示:

b膜属于
您最近半年使用:0次



