1 . 宏观辨识与微观探析是化学学科核心素养之一,下列反应方程式书写错误的是
A.久置于空气中的 溶液变质: 溶液变质: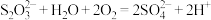 |
B.用醋酸和碘化钾淀粉溶液检验加碘盐中的 : : |
C.向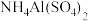 溶液中加入等物质的量的 溶液中加入等物质的量的 溶液: 溶液: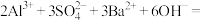 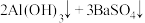 |
D.用饱和碳酸钠溶液处理锅炉水垢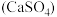 : : |
您最近一年使用:0次
2 . 常温下,分别向MnCl2、ZnCl2、CH3COOH溶液中滴加NaOH溶液,溶液pX[pX=-lgc(X),X代表Mn2+、Zn2+、OH-, ]与pH关系如图所示。已知:Ksp[Mn(OH)2]>Ksp[Zn(OH)2]。下列叙述正确的是
]与pH关系如图所示。已知:Ksp[Mn(OH)2]>Ksp[Zn(OH)2]。下列叙述正确的是
 ]与pH关系如图所示。已知:Ksp[Mn(OH)2]>Ksp[Zn(OH)2]。下列叙述正确的是
]与pH关系如图所示。已知:Ksp[Mn(OH)2]>Ksp[Zn(OH)2]。下列叙述正确的是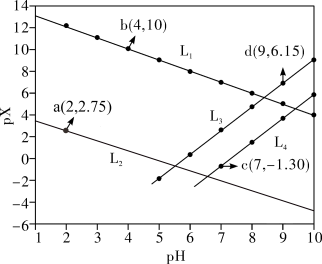
A.图中L2代表 ,L3代表Mn2+ ,L3代表Mn2+ |
| B.室温下,Ksp[Zn(OH)2]的数量级为10-13 |
C.同时产生两种沉淀时,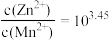 |
D.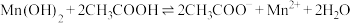 的平衡常数K=105.8 的平衡常数K=105.8 |
您最近一年使用:0次
7日内更新
|
56次组卷
|
2卷引用:江西省部分重点中学2024届高三下学期第二次联考化学试题
3 . 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 实验操作和现象 | 结论 | |
| A | 用pH试纸测得0.1 mol·L 的 的 溶液的 溶液的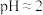 |  |
| B | 向某溶液中滴加足量稀盐酸,无沉淀生成,再滴入 溶液,产生白色沉淀 溶液,产生白色沉淀 | 该溶液中一定含 |
| C | 取少量丙烯醛于试管中,滴加溴水,溴水褪色 | 该有机物中含有碳碳双键 |
| D | 向同浓度的NaCl和 的稀溶液中滴加 的稀溶液中滴加 溶液,先出现白色沉淀,后出现砖红色沉淀。 溶液,先出现白色沉淀,后出现砖红色沉淀。 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 25℃时,难溶物M(OH)3和R(OH)2形成的饱和液中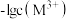 或
或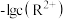 与pH的变化关系如图所示。设难溶电解质的溶解度单位为mol·L-1,下列说法正确的是
与pH的变化关系如图所示。设难溶电解质的溶解度单位为mol·L-1,下列说法正确的是
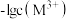 或
或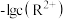 与pH的变化关系如图所示。设难溶电解质的溶解度单位为mol·L-1,下列说法正确的是
与pH的变化关系如图所示。设难溶电解质的溶解度单位为mol·L-1,下列说法正确的是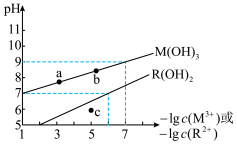
| A.25℃时,c点时的R(OH)2溶液为饱和溶液 |
| B.向M(OH)3饱和溶液中加入盐酸可使a点变到b点 |
C.pH=8时,M(OH)3的溶解度为 |
| D.浓度均为0.1mol/L的M3+和R2+,调节pH,当M(OH)3开始沉淀时,有R(OH)2沉淀生成 |
您最近一年使用:0次
2024-05-15更新
|
52次组卷
|
2卷引用:江西省九江市同文中学2023-2024学年高三下学期期中考试化学试题
名校
5 . 化学与生活生产密切相关。下列叙述正确的是
| A.漂白粉与盐酸混合使用可以提升消毒效果 | B.实验室电解水常加入少量稀盐酸增强导电性 |
C.核电站反应堆所用轴棒中含有的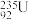 与 与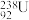 互为同素异形体 互为同素异形体 | D.常用含氟牙膏刷牙可坚周牙齿、预防龋齿 |
您最近一年使用:0次
名校
解题方法
6 . 氯化钡是重要的化工原料,是制备其他钡盐的主要中间原料,以毒重石(主要成分为 ,还含有
,还含有 及含Ca、Mg、Fe、Al的化合物)为原料制备
及含Ca、Mg、Fe、Al的化合物)为原料制备 的工艺流程如下:
的工艺流程如下: 、
、 、
、 、
、 形式存在于溶液中。
形式存在于溶液中。
回答下列问题:
(1)在“浸取”时,除温度、酸的浓度、液固比等因素影响钡的浸出率外,还有___________ 因素。
(2)下表列举了不同温度、盐酸的浓度、液固比下钡的浸出率实验数据,每个实验只改变一个条件:
分析表中数据,温度越高钡的浸出率越低的可能原因是___________ ;判断“浸取”的最佳液固比为___________ 。
(3)常温时,几种金属离子沉淀的pH如图所示,加 时发生反应的离子方程式为
时发生反应的离子方程式为___________ ;“调pH(Ⅰ)”时,调节溶液 ,则“滤渣Ⅱ”的主要成分为
,则“滤渣Ⅱ”的主要成分为___________ (填化学式)。___________ 。
 ,还含有
,还含有 及含Ca、Mg、Fe、Al的化合物)为原料制备
及含Ca、Mg、Fe、Al的化合物)为原料制备 的工艺流程如下:
的工艺流程如下: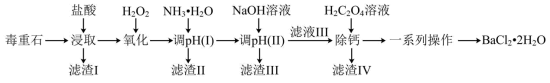
 、
、 、
、 、
、 形式存在于溶液中。
形式存在于溶液中。回答下列问题:
(1)在“浸取”时,除温度、酸的浓度、液固比等因素影响钡的浸出率外,还有
(2)下表列举了不同温度、盐酸的浓度、液固比下钡的浸出率实验数据,每个实验只改变一个条件:
| 改变的条件 | 温度(℃) | 盐酸的浓度(%) | 液固比 | ||||||||
| 30 | 55 | 75 | 10 | 15 | 20 | 25 | 3:1 | 4:1 | 5:1 | 6:1 | |
| 钡的浸出率(%) | 74.31 | 69.60 | 68.42 | 59.21 | 74.31 | 74.15 | 55.32 | 59.84 | 65.12 | 74.31 | 74.35 |
(3)常温时,几种金属离子沉淀的pH如图所示,加
 时发生反应的离子方程式为
时发生反应的离子方程式为 ,则“滤渣Ⅱ”的主要成分为
,则“滤渣Ⅱ”的主要成分为
您最近一年使用:0次
名校
7 . 常温下,CaSO4在水中的沉淀溶解平衡曲线如图所示,已知常温下Ksp(CaSO4)=9×10-6.下列说法正确的是

| A.升高温度曲线会往左下方移动 |
| B.b点加水可以变到b',且此时的Ksp(CaSO4)=9×10-6 |
| C.d点表示CaSO4的过饱和溶液 |
| D.加入Na2SO4(s),可以使溶液由c点变到a点 |
您最近一年使用:0次
解题方法
8 .  是生产多晶硅的副产物,遇水剧烈水解。利用
是生产多晶硅的副产物,遇水剧烈水解。利用 对废旧的锂电池正极材料
对废旧的锂电池正极材料 进行焙烧氯化处理(生成
进行焙烧氯化处理(生成 ),以回收
),以回收 ,工艺流程如图所示。
,工艺流程如图所示。

下列说法错误的是
 是生产多晶硅的副产物,遇水剧烈水解。利用
是生产多晶硅的副产物,遇水剧烈水解。利用 对废旧的锂电池正极材料
对废旧的锂电池正极材料 进行焙烧氯化处理(生成
进行焙烧氯化处理(生成 ),以回收
),以回收 ,工艺流程如图所示。
,工艺流程如图所示。
下列说法错误的是
A.“ 焙烧”时,加入 焙烧”时,加入 的作用是作还原剂 的作用是作还原剂 |
B.焙烧后应先除去过量的 ,避免水浸时产生大量白雾 ,避免水浸时产生大量白雾 |
C.“滤饼1”的主要成分是 |
D.“沉锂”时,发生反应的离子方程式为 |
您最近一年使用:0次
名校
9 . 下列反应的离子方程式书写正确的是
A.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-=2HClO+CO |
B.用纯碱溶液转化水垢中的CaSO4:CO (aq)+CaSO4(s)=SO (aq)+CaSO4(s)=SO (aq)+CaCO3(s) (aq)+CaCO3(s) |
C.磁性氧化铁溶于稀HNO3:Fe3O4+12H++NO =3Fe3++NO↑+6H2O =3Fe3++NO↑+6H2O |
D.电解MgCl2水溶液:2Cl-+2H2O 2OH-+Cl2↑+H2↑ 2OH-+Cl2↑+H2↑ |
您最近一年使用:0次
解题方法
10 . 根据下列实验操作和现象,得到的结论正确的是
实验操作和现象 | 实验结论 | |
A | 向 |
|
B | 向 |
|
C | 往 | 非金属性: |
D | 向 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 溶液中滴加3滴
溶液中滴加3滴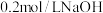 溶液,再滴加4滴
溶液,再滴加4滴 溶液,白色沉淀转化为红褐色
溶液,白色沉淀转化为红褐色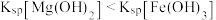
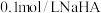 溶液中滴加酚酞溶液,溶液变为浅红色
溶液中滴加酚酞溶液,溶液变为浅红色 (
( 和
和 为
为 的电离平衡常数)
的电离平衡常数)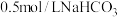 溶液中加入盐酸,将产生的气体通入
溶液中加入盐酸,将产生的气体通入 溶液中,
溶液中,
 悬浊液中滴入适量氨水,悬浊液变澄清
悬浊液中滴入适量氨水,悬浊液变澄清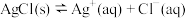 平衡正向移动
平衡正向移动

