1 . 已知:常温下 ,
,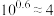 。向10
。向10 0.10
0.10
 溶液中滴加0.10
溶液中滴加0.10 的
的 溶液,滴加过程中
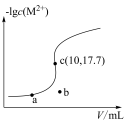
溶液,滴加过程中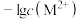 (M表示金属)与加入的溶液体积(V)的关系如图所示,下列说法正确的是
(M表示金属)与加入的溶液体积(V)的关系如图所示,下列说法正确的是
 ,
,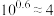 。向10
。向10 0.10
0.10
 溶液中滴加0.10
溶液中滴加0.10 的
的 溶液,滴加过程中
溶液,滴加过程中 (M表示金属)与加入的溶液体积(V)的关系如图所示,下列说法正确的是
(M表示金属)与加入的溶液体积(V)的关系如图所示,下列说法正确的是
A.常温下,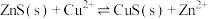 的平衡常数 的平衡常数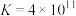 |
B.常温下, 饱和溶液中 饱和溶液中 的数量级为 的数量级为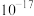 |
C.b点体系中, 的溶解速率大于其生成速率 的溶解速率大于其生成速率 |
D.若用 代替 代替 (其他不变),则c点应向下移动 (其他不变),则c点应向下移动 |
您最近一年使用:0次
2024-02-11更新
|
410次组卷
|
3卷引用:江西省宜春市宜丰中学2023-2024学年高二上学期1月月考化学试题
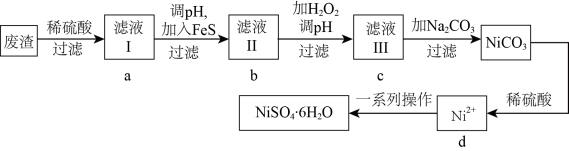
2 .  是一种绿色易溶于水的晶体,可由电镀废渣(除镍外,还含有铜、锌、铁等元素的化合物杂质)为原料获得。操作步骤如图:
是一种绿色易溶于水的晶体,可由电镀废渣(除镍外,还含有铜、锌、铁等元素的化合物杂质)为原料获得。操作步骤如图:
已知:各离子开始沉淀及完全沉淀时的 如表所示:
如表所示:
根据要求回答下列问题
(1)基态 原子核外电子的空间运动状态有
原子核外电子的空间运动状态有______________ 种,画出基态原子的价电子轨道表示式______________ 。
(2)向滤液Ⅰ中加入 固体是为了生成更难溶于水的硫化物沉淀而除去
固体是为了生成更难溶于水的硫化物沉淀而除去 、
、 等杂质,则除去
等杂质,则除去 的离子方程式为
的离子方程式为_______________________________________ ,当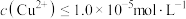 时,可认为
时,可认为 已沉淀完全,此时溶液中
已沉淀完全,此时溶液中 的浓度不小于
的浓度不小于_____________ 。[已知: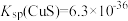 ]
]
(3)根据对滤液Ⅱ的操作作答:
①向滤液Ⅱ中加 的目的是将
的目的是将 氧化成
氧化成 ,试从结构的角度解释
,试从结构的角度解释 易被氧化为
易被氧化为 的原因
的原因__________________________ ;
②调节滤液Ⅱ的 ,
, 应控制在范围为
应控制在范围为__________________________ ;
③检验滤液Ⅲ中杂质金属离子是否除尽最合理的试剂是_______________________________________ 。
(4)滤液Ⅲ溶质的主要成分是 ,加
,加 过滤后得到
过滤后得到 固体,再加适量稀硫酸溶解又生成
固体,再加适量稀硫酸溶解又生成 ,这两步操作的目的是
,这两步操作的目的是_______________________________________ 。
 是一种绿色易溶于水的晶体,可由电镀废渣(除镍外,还含有铜、锌、铁等元素的化合物杂质)为原料获得。操作步骤如图:
是一种绿色易溶于水的晶体,可由电镀废渣(除镍外,还含有铜、锌、铁等元素的化合物杂质)为原料获得。操作步骤如图:
已知:各离子开始沉淀及完全沉淀时的
 如表所示:
如表所示:离子 | 开始沉淀时的 | 完全沉淀时的 |
| 6.3 | 9.7 |
| 2.2 | 3.2 |
| 6.4 | 8.4 |
(1)基态
 原子核外电子的空间运动状态有
原子核外电子的空间运动状态有(2)向滤液Ⅰ中加入
 固体是为了生成更难溶于水的硫化物沉淀而除去
固体是为了生成更难溶于水的硫化物沉淀而除去 、
、 等杂质,则除去
等杂质,则除去 的离子方程式为
的离子方程式为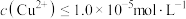 时,可认为
时,可认为 已沉淀完全,此时溶液中
已沉淀完全,此时溶液中 的浓度不小于
的浓度不小于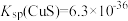 ]
](3)根据对滤液Ⅱ的操作作答:
①向滤液Ⅱ中加
 的目的是将
的目的是将 氧化成
氧化成 ,试从结构的角度解释
,试从结构的角度解释 易被氧化为
易被氧化为 的原因
的原因②调节滤液Ⅱ的
 ,
, 应控制在范围为
应控制在范围为③检验滤液Ⅲ中杂质金属离子是否除尽最合理的试剂是
(4)滤液Ⅲ溶质的主要成分是
 ,加
,加 过滤后得到
过滤后得到 固体,再加适量稀硫酸溶解又生成
固体,再加适量稀硫酸溶解又生成 ,这两步操作的目的是
,这两步操作的目的是
您最近一年使用:0次
名校
解题方法
3 . 下列实验操作和实验结论或目的均正确的是
选项 | 实验操作 | 实验结论或目的 |
A | 向含有酚酞的 | 证明 |
B | 等体积 | 证明HX酸性比HY强 |
C | 将氯水滴在湿润的pH试纸上,与标准比色卡对照 | 测定氯水的pH |
D | D.向 | 证明在相同温度下: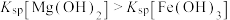 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-24更新
|
65次组卷
|
2卷引用:江西省宜春市丰城中学东校区(九中)2023-2024学年高二下学期开学考试化学试卷
名校
4 . 化学与生产、生活息息相关。下列有关说法错误的是
| A.酒曲酿酒,利用了催化剂使平衡正向移动的原理 |
| B.采用低温冷冻技术保存食物可减慢食物腐烂速率 |
| C.海港码头的钢管桩,可利用“外加电流法”防腐蚀 |
D.盐碱地(含较多 等)可通过施加适量石膏( 等)可通过施加适量石膏( ),降低土壤的碱性 ),降低土壤的碱性 |
您最近一年使用:0次
2024-01-22更新
|
71次组卷
|
3卷引用:江西省宜春市丰城中学东校区(九中)2023-2024学年高二下学期开学考试化学试卷
名校
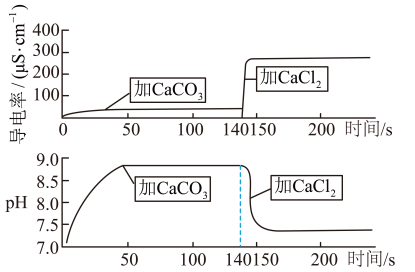
5 . 25℃时,往 蒸馏水中加入足量
蒸馏水中加入足量 粉末
粉末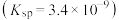 ,经过
,经过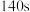 后往溶液中加入
后往溶液中加入 粉末(忽略温度变化),整个过程中溶液电导率和
粉末(忽略温度变化),整个过程中溶液电导率和 随时间的变化如图所示,下列说法中错误的是
随时间的变化如图所示,下列说法中错误的是
 蒸馏水中加入足量
蒸馏水中加入足量 粉末
粉末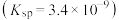 ,经过
,经过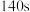 后往溶液中加入
后往溶液中加入 粉末(忽略温度变化),整个过程中溶液电导率和
粉末(忽略温度变化),整个过程中溶液电导率和 随时间的变化如图所示,下列说法中错误的是
随时间的变化如图所示,下列说法中错误的是
A.加入 粉末后,溶液 粉末后,溶液 上升的原因为 上升的原因为 |
B.加入 粉末后,溶液中的 粉末后,溶液中的 水解程度增大 水解程度增大 |
C. 时, 时,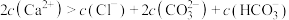 |
D. 时, 时,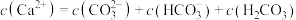 |
您最近一年使用:0次
2024-01-13更新
|
895次组卷
|
6卷引用:江西省宜春市宜丰中学2023-2024学年高二上学期1月月考化学试题
江西省宜春市宜丰中学2023-2024学年高二上学期1月月考化学试题辽宁省沈阳市部分高中2023-2024学年高三上学期教学质量监测(一)化学试题2024届辽宁省沈阳市高三教学质量检测(一模)化学试题(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)辽宁省沈阳市2024届高三一模化学试题四川省成都外国语学校2023-2024学年高三上学期期末考试理科综合试题-高中化学
6 . 下列有关说法中,正确的是
| A.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 |
| B.在Ca(OH)2(Ksp=5.5×10-6)、Mg(OH)2(Ksp=1.2×10-11)、AgCl(Ksp=1.56×10-10)三种物质中,AgCl的溶解度最小 |
C.已知BaSO4的Ksp=c(Ba2+)·c(SO ),所以在BaSO4溶液中有c(Ba2+)= c(SO ),所以在BaSO4溶液中有c(Ba2+)= c(SO )= )= |
| D.Ksp小的难溶物可以转变为Ksp更小的难溶物,不可以转变为Ksp更大的难溶物 |
您最近一年使用:0次
7 . 已知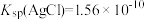 ,
,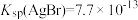 ,
, 。某溶液中含有
。某溶液中含有 、
、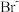 和
和 ,浓度均为0.010
,浓度均为0.010 ,向该溶液中逐滴加入0.010
,向该溶液中逐滴加入0.010 的
的 溶液时,三种阴离子产生沉淀的先后顺序为
溶液时,三种阴离子产生沉淀的先后顺序为
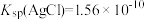 ,
,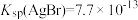 ,
, 。某溶液中含有
。某溶液中含有 、
、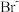 和
和 ,浓度均为0.010
,浓度均为0.010 ,向该溶液中逐滴加入0.010
,向该溶液中逐滴加入0.010 的
的 溶液时,三种阴离子产生沉淀的先后顺序为
溶液时,三种阴离子产生沉淀的先后顺序为A. | B. |
C. | D.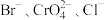 |
您最近一年使用:0次
2023-12-31更新
|
246次组卷
|
100卷引用:江西省靖安中学2020-2021学年高二上学期第二次月考化学试题
江西省靖安中学2020-2021学年高二上学期第二次月考化学试题2013年全国普通高等学校招生统一考试理科综合能力测试化学(新课标Ⅰ卷)(已下线)2013-2014学年湖南省常德市一中高二上学期第二次检测理科化学试卷(已下线)2013-2014重庆市重庆八中下学期高二期中考试化学试卷(已下线)2013-2014福建省安溪八中高二下学期期末考试化学试卷2014-2015河南省濮阳市一中高二上学期第三次质量检测化学试卷2014-2015河南省濮阳市一中高二上学期第三次月考化学试卷2014-2015湖北省武汉华中师大附高二上学期期末化学试卷2014-2015广西桂林市第十八中学高二下学期期中考试化学试卷2015-2016学年山西省太原五中高二上12月月考化学试卷12015-2016学年山西省太原五中高二上12月月考化学试卷22015-2016学年黑龙江省哈尔滨三中高二上期末化学试卷2015-2016学年贵州省凯里一中高二上学期期末化学试卷2015-2016学年宁夏育才中学高二上期末考试化学试卷2016届山东省寿光现代中学高三下学期开学检测化学试卷2016届山东省青岛市高三上学期期末考试化学试卷2015-2016学年湖南省株洲十八中高二上学期期末理化学试卷2015-2016学年福建省龙海市程溪中学高二下学期期中化学试卷2015-2016学年广西桂林十八学高二下期中化学试卷2016-2017学年河北省邯郸一中高二上期中化学卷2016-2017学年宁夏育才中学高二上月考二化学卷22016-2017学年西藏拉萨中学高二上期末化学试卷2016-2017学年河北省张家口市高二上学期期末考试化学试卷2016-2017学年河北省邯郸市高二上学期期末考试化学试卷广西桂林市桂林中学2016-2017学年高二下学期期中考试化学试题四川省成都市双流中学2016-2017学年高二5月月考化学试题内蒙古北京八中乌兰察布分校2016-2017学年高二下学期期末考试化学试题2018版化学(苏教版)高考总复习专题八对接高考精练--难溶电解质的沉淀溶解平衡福建省福州市第八中学2016-2017学年高二下学期期末考试(理)化学试题河北省定州中学2017-2018学年高二上学期开学考试化学试题贵州省遵义航天高级中学2017-2018学年高二上学期第三次月考理综(理)化学试题天津市静海县第一中学2017-2018学年高二12月学生学业能力调研考试化学试题山西省大同市第一中学2017-2018学年高二上学期期末考试化学试题(已下线)2018年11月15日 《每日一题》人教选修4-溶度积的应用【全国百强校】甘肃省天水市一中2018-2019学年高二(理)上学期第二学段考试化学试题安徽省滁州市定远县民族中学2018-2019学年高二上学期12月月考化学试题内蒙古集宁一中西校区2017-2018学年高二上学期期中考试化学试题云南省保山市第一中学2018-2019学年高二下学期期末化学试题安徽省太和第一中学2019-2020学年高二上学期第一次月考(飞越班)化学试题(已下线)2019年11月14日 《每日一题》人教版(选修4)——溶度积的应用夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——溶度积常数及相关计算(强化练习)重庆市凤鸣山中学2018-2019学年高二上学期期中考试化学试题湖北省黄冈市黄梅国际育才高级中学2019-2020学年高二上学期10月月考化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡 课时1 沉淀溶解平衡及其应用鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 课时1 溶解平衡及其应用(已下线)第03章 物质在水溶液中的行为 (B卷能力提升卷) -2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)内蒙古通辽市开鲁县第一中学2021届高三上学期第一次月考化学试题人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 方法帮黑龙江省鹤岗市第一中学2020-2021学年高二10月月考化学试题黑龙江绥化市第一中学2020-2021学年高二上学期第一次月考化学试题 (已下线)第03章 水溶液中的离子反应与平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)(已下线)易错17 难溶电解质的溶解平衡及应用-备战2021年高考化学一轮复习易错题(已下线)第28讲 难溶电解质的溶解平衡 (精练)-2021年高考化学一轮复习讲练测重庆市万州第三中学2020-2021学年高二上学期期中考试化学试题(已下线)3.4 难溶电解质的溶解平衡(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)吉林省长春市第二十九中学2020-2021学年高二上学期期末考试化学试题(已下线)练习14 难溶电解质的沉淀溶解平衡-2020-2021学年【补习教材·寒假作业】高二化学(苏教版)吉林省长春市清蒲中学2020-2021学年度高二上学期期末化学试题甘肃省民勤县第一中学2020-2021学年高二下学期(理)开学考试化学试题山西省潞城第一中学2020-2021学年高二下学期3月月考化学试卷题江苏省盐城市阜宁中学2020-2021学年高二下学期期中考试化学试题云南省玉溪市华宁二中2020-2021学年高二下学期期中考试化学试题四川省绵阳市2020-2021学年高二下学期期末考试化学试题(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)云南省陆良县2019届高三毕业班第二次教学质量摸底考化学试题(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第24讲 沉淀溶解平衡(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第5讲 沉淀溶解平衡-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)四川省绵阳市盐亭中学2021-2022学年高二下学期4月月考化学试题四川省遂宁市第二中学校2021-2022学年高二下学期半期考试化学试题山东省德州市2020-2021学年高二上学期反应原理月考(B)化学试题(已下线)考点29 沉淀溶解平衡-备战2023年高考化学一轮复习考点帮(全国通用)第四节 沉淀溶解平衡 第2课时 沉淀溶解平衡的应用(已下线)3.4.1 沉淀溶解平衡-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)四川省成都市第七中学2023届高三上学期零诊模拟考试化学试题湖南省长沙市明德中学2022-2023学年高二上学期期中考试化学试题广东省江门市第一中学2022-2023学年高二上学期第二次月考化学试题(已下线)3.4 沉淀溶解平衡-同步学习必备知识山东省淄博市桓台第二中学2021-2022学年高一9月月考化学试题河北省邯郸市永年区第二中学2022-2023学年高二上学期12月月考化学试题黑龙江省伊春市伊美区第二中学2022-2023学年高二上学期期中化学试题黑龙江省双鸭山市第一中学2022-2023学年高二下学期开学考试化学试题吉林省洮南市第一中学2022-2023学年高二上学期期末考试化学试题四川省内江市第六中学2022-2023学年高二下学期第一次月考(创新班)化学试题广东番禺中学2022-2023学年高二上学期期末测试化学试题(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)第2课时 沉淀的溶解与生成、转化及应用第1课时 沉淀溶解平衡与溶度积河南省郑州市宇华实验学校2023-2024学年高三上学期开学(摸底)考试化学试题第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 第2课时 沉淀溶解平衡的应用新疆奎屯市第一高级中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业07 沉淀溶解平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)四川省泸州市合江县马街中学校2023-2024学年高二上学期11月期中化学试题(已下线)专题06 沉淀溶解平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)陕西省咸阳市武功县普集高级中学2023-2024学年高二上学期12月月考化学试题陕西省汉中市西乡县第一中学2023-2024学年高二上学期12月月考化学试题宁夏石嘴山市第三中学2023-2024学年高二上学期第二次月考化学试题四川省眉山市仁寿县2023-2024学年高二上学期12月联考化学试题河北省衡水市安平中学2023-2024学年高二下学期开学考试化学试题
名校
8 . 下列实验操作、现象、解释或结论都正确的是
| 选项 | 操作 | 现象 | 解释或结论 |
| A | 在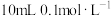 的 的 溶液中依次滴入几滴 溶液中依次滴入几滴 溶液和KI溶液 溶液和KI溶液 | 溶液先产生白色沉淀,后又产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 将 通入 通入 溶液 溶液 | 有白色沉淀生成 | 生成了 沉淀 沉淀 |
| C | 向某钠盐粉末上滴加浓盐酸,将产生的气体通入品红溶液 | 品红溶液褪色 | 该钠盐为 、 、 或 或 |
| D | 在 溶液中通入 溶液中通入 气体 气体 | 有沉淀生成 | 沉淀为 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-16更新
|
359次组卷
|
3卷引用:江西省上饶市清源学校2023-2024学年高二上学期12月考试化学试题
名校
解题方法
9 . MnO2是重要化工原料,由软锰矿制备MnO2的一种工艺流程如下:

资料:
①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2。
②金属离子沉淀的pH:
③该工艺条件下,MnO2与H2SO4不反应。
(1)溶出
①溶出前,软锰矿需研磨,目的是___________ 。
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:
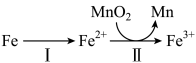
i.II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是___________ 。
ii.若I中Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2,而实际比值(0.9)小于2,原因是___________ 。
(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2后加入NH3·H2O,调溶液pH,说明试剂加入顺序及调节pH的原因:___________ 。
(3)电解
Mn2+纯化液经电解得MnO2,生成1molMnO2电子转移的数目为___________ 。
(4)产品纯度测定
向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,如热至充分反应,生成CO2,再滴加cmol/L KMnO4溶液至剩余Na2C2O4恰好完全反应,消耗KMnO4溶液的体积为dL,产品纯度为___________ (用质量分数表示)。[已知:MnO2及 均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]

资料:
①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2。
②金属离子沉淀的pH:
| Fe3+ | A13+ | Mn2+ | Fe2+ | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
(1)溶出
①溶出前,软锰矿需研磨,目的是
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:

i.II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是
ii.若I中Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2,而实际比值(0.9)小于2,原因是
(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2后加入NH3·H2O,调溶液pH,说明试剂加入顺序及调节pH的原因:
(3)电解
Mn2+纯化液经电解得MnO2,生成1molMnO2电子转移的数目为
(4)产品纯度测定
向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,如热至充分反应,生成CO2,再滴加cmol/L KMnO4溶液至剩余Na2C2O4恰好完全反应,消耗KMnO4溶液的体积为dL,产品纯度为
 均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
您最近一年使用:0次
2023-12-15更新
|
175次组卷
|
3卷引用:江西省上饶市广丰一中2023-2024学年高二上学期12月考试化学试卷
名校
10 . 将浓盐酸加到NaCl饱和溶液中,会析出NaCl晶体,对这种现象正确的解释是
| A.由于c平(Cl-)增加,使溶液中c平(Na+)·c平(Cl-)>Ksp(NaCl),故产生NaCl晶体 |
| B.HCl是强酸,所以它能使NaCl沉淀出来 |
| C.由于c平(Cl-)增加,使NaCl的溶解平衡向析出NaCl的方向移动,故有NaCl沉淀析出 |
| D.酸的存在,降低了盐的溶解度 |
您最近一年使用:0次
2023-08-26更新
|
464次组卷
|
4卷引用:江西省宜丰中学2023-2024学年高三上学期9月月考化学试题


 的HX和HY两种酸分别与足量的铁反应,排水法收集气体,HX放出的氢气多且反应速率快
的HX和HY两种酸分别与足量的铁反应,排水法收集气体,HX放出的氢气多且反应速率快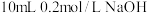 溶液中滴2滴
溶液中滴2滴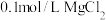 溶液,产生白色沉淀后再滴加2滴
溶液,产生白色沉淀后再滴加2滴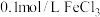 ,又生成红褐色沉淀
,又生成红褐色沉淀

