1 . 某温度时, 在水溶液中的沉淀溶解平衡曲线如图所示。下列说法正确的是
在水溶液中的沉淀溶解平衡曲线如图所示。下列说法正确的是

 在水溶液中的沉淀溶解平衡曲线如图所示。下列说法正确的是
在水溶液中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A.向 溶液中滴加 溶液中滴加 溶液不一定会生成沉淀 溶液不一定会生成沉淀 |
B.该温度下, 的溶度积常数 的溶度积常数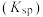 的数量级是 的数量级是 |
| C.可以通过改变温度或加入硫酸银固体使a点移动到b点 |
D.含有大量 的溶液中肯定不存在 的溶液中肯定不存在 |
您最近一年使用:0次
名校
2 . 工业.上用菱锰矿( )[含
)[含 、
、 、
、 等杂质]为原料制取二氧化锰,其流程示意图如下:
等杂质]为原料制取二氧化锰,其流程示意图如下:
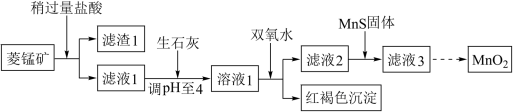
已知生成氢氧化物沉淀的 :
:
注:金属离子的起始浓度为
回答下列问题:
(1) 元素在周期表中位置是
元素在周期表中位置是__________ ,属于__________ 区元素(选填“s”、“p”、“d”或s")。
(2)含杂质的菱锰矿使用前需将其粉碎,主要目的是___________ ;盐酸溶解 的化学方程式是
的化学方程式是____________________ 。
(3)向溶液1中加入双氧水时,反应的离子方程式是______________________________ 。
(4)滤液2中加入稍过量的难溶电解质 ,以除去
,以除去 ,反应的离子方程式是
,反应的离子方程式是____________________ 。
(5)将 转化为
转化为 的一种方法是氧化法。其具体做法是用酸化的
的一种方法是氧化法。其具体做法是用酸化的 溶液将
溶液将 氧化,该反应的离子方程式:
氧化,该反应的离子方程式: __________
 。
。
(6)将 转化为
转化为 的另一种方法是电解法。
的另一种方法是电解法。
①生成 的电极反应式是
的电极反应式是______________________________ 。
②若在上述 溶液中加入一定量的
溶液中加入一定量的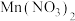 粉末,则无
粉末,则无 产生。其原因是
产生。其原因是____________________ 。
 )[含
)[含 、
、 、
、 等杂质]为原料制取二氧化锰,其流程示意图如下:
等杂质]为原料制取二氧化锰,其流程示意图如下:
已知生成氢氧化物沉淀的
 :
:
|
|
|
| |
开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |

回答下列问题:
(1)
 元素在周期表中位置是
元素在周期表中位置是(2)含杂质的菱锰矿使用前需将其粉碎,主要目的是
 的化学方程式是
的化学方程式是(3)向溶液1中加入双氧水时,反应的离子方程式是
(4)滤液2中加入稍过量的难溶电解质
 ,以除去
,以除去 ,反应的离子方程式是
,反应的离子方程式是(5)将
 转化为
转化为 的一种方法是氧化法。其具体做法是用酸化的
的一种方法是氧化法。其具体做法是用酸化的 溶液将
溶液将 氧化,该反应的离子方程式:
氧化,该反应的离子方程式:  。
。(6)将
 转化为
转化为 的另一种方法是电解法。
的另一种方法是电解法。①生成
 的电极反应式是
的电极反应式是②若在上述
 溶液中加入一定量的
溶液中加入一定量的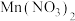 粉末,则无
粉末,则无 产生。其原因是
产生。其原因是
您最近一年使用:0次
名校
3 . 草酸镍晶体( )可用于制镍催化剂。工业上用废镍催化剂(主要成分为Al2O3、Ni、Fe、SiO2、CaO)制备草酸镍晶体的一种工艺流程如图所示:
)可用于制镍催化剂。工业上用废镍催化剂(主要成分为Al2O3、Ni、Fe、SiO2、CaO)制备草酸镍晶体的一种工艺流程如图所示:

已知:
①相关金属离子生成氢氧化物沉淀的pH如下表(开始沉淀的pH按金属离子浓度为 计算):
计算):
② ,
,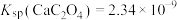 。
。
回答下列问题:
(1)基态镍原子的价层电子排布式为___________ 。
(2)试剂X可以是___________ ,
(3)调节pH的范围是___________ 。
(4)滤渣1的成分是___________ (写化学式),加入适量NH4F溶液的目的是___________ 。
(5)“沉镍”的离子方程式为___________ 。
(6)称取一定质量某镀镍试剂,配成100mL溶液,溶液中存在的离子为 、
、 、
、 ;准确量取10.00mL溶液,用
;准确量取10.00mL溶液,用 的EDTA标准溶液滴定其中的
的EDTA标准溶液滴定其中的 ,消耗EDTA标准溶液25.00mL。已知M2+为金属阳离子,与EDTA反应的方程式为:M2++EDTA4-=MEDTA2-。
,消耗EDTA标准溶液25.00mL。已知M2+为金属阳离子,与EDTA反应的方程式为:M2++EDTA4-=MEDTA2-。
①配制EDTA标准溶液需要注意蒸馏水的水质,水中若含 、
、 会使滴定时消耗的EDTA的体积
会使滴定时消耗的EDTA的体积___________ (填“偏大”“不变”或“偏小”)。
②该镀镍试剂中 的物质的量浓度为
的物质的量浓度为___________ mol/L。
 )可用于制镍催化剂。工业上用废镍催化剂(主要成分为Al2O3、Ni、Fe、SiO2、CaO)制备草酸镍晶体的一种工艺流程如图所示:
)可用于制镍催化剂。工业上用废镍催化剂(主要成分为Al2O3、Ni、Fe、SiO2、CaO)制备草酸镍晶体的一种工艺流程如图所示:
已知:
①相关金属离子生成氢氧化物沉淀的pH如下表(开始沉淀的pH按金属离子浓度为
 计算):
计算):| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
 | 1.1 | 3.2 |
 | 5.8 | 8.8 |
 | 3.0 | 5.0 |
 | 6.7 | 9.5 |
 ,
,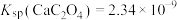 。
。回答下列问题:
(1)基态镍原子的价层电子排布式为
(2)试剂X可以是
(3)调节pH的范围是
(4)滤渣1的成分是
(5)“沉镍”的离子方程式为
(6)称取一定质量某镀镍试剂,配成100mL溶液,溶液中存在的离子为
 、
、 、
、 ;准确量取10.00mL溶液,用
;准确量取10.00mL溶液,用 的EDTA标准溶液滴定其中的
的EDTA标准溶液滴定其中的 ,消耗EDTA标准溶液25.00mL。已知M2+为金属阳离子,与EDTA反应的方程式为:M2++EDTA4-=MEDTA2-。
,消耗EDTA标准溶液25.00mL。已知M2+为金属阳离子,与EDTA反应的方程式为:M2++EDTA4-=MEDTA2-。①配制EDTA标准溶液需要注意蒸馏水的水质,水中若含
 、
、 会使滴定时消耗的EDTA的体积
会使滴定时消耗的EDTA的体积②该镀镍试剂中
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
名校
4 . 某温度下,向 溶液中滴加
溶液中滴加 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中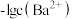 与
与 溶液体积
溶液体积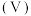 的关系如图所示,已知
的关系如图所示,已知 。下列说法正确的是
。下列说法正确的是
 溶液中滴加
溶液中滴加 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中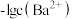 与
与 溶液体积
溶液体积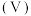 的关系如图所示,已知
的关系如图所示,已知 。下列说法正确的是
。下列说法正确的是
| A.溶液b点可以通过升高温度到达c点 |
B.该温度下 |
C.b点溶液中: |
D.若把 溶液换成等浓度 溶液换成等浓度 溶液,则曲线变为Ⅱ 溶液,则曲线变为Ⅱ |
您最近一年使用:0次
2023-05-04更新
|
454次组卷
|
4卷引用:四川省眉山车城中学 眉山市东坡区永寿高级中学校2023-2024学年高二上学期1月期末联考化学试题
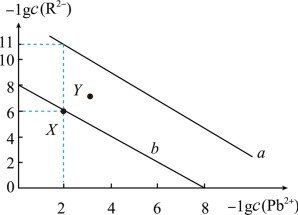
5 . 25°C时,PbR(R2-为 或
或 )的沉淀溶解平衡关系图如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法错误的是
)的沉淀溶解平衡关系图如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法错误的是
 或
或 )的沉淀溶解平衡关系图如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法错误的是
)的沉淀溶解平衡关系图如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法错误的是
| A.线b表示PbSO4 |
B.当PbSO4和PbCO3沉淀共存时,溶液中c( )和c( )和c( )的比是1×105 )的比是1×105 |
| C.向X点对应的饱和溶液中加入少量Pb(NO3)2,可转化为Y点对应的溶液 |
| D.Y点溶液是PbSO4的不饱和溶液 |
您最近一年使用:0次
6 .  是一种难溶电解质。常温下,用盐酸调节
是一种难溶电解质。常温下,用盐酸调节 浊液的pH,测得在不同pH条件下,体系中
浊液的pH,测得在不同pH条件下,体系中 与
与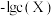 (X为
(X为 或
或 )的关系如图所示。下列说法不正确的是
)的关系如图所示。下列说法不正确的是

 是一种难溶电解质。常温下,用盐酸调节
是一种难溶电解质。常温下,用盐酸调节 浊液的pH,测得在不同pH条件下,体系中
浊液的pH,测得在不同pH条件下,体系中 与
与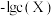 (X为
(X为 或
或 )的关系如图所示。下列说法不正确的是
)的关系如图所示。下列说法不正确的是
A.随着盐酸的加入, 不断溶解 不断溶解 |
B. 表示 表示 随 随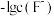 的变化曲线 的变化曲线 |
C. |
D. |
您最近一年使用:0次
2023-03-17更新
|
367次组卷
|
2卷引用:四川省仁寿第一中学校(北校区)2023-2024学年高三上学期期末考试理综试题-高中化学
名校
解题方法
7 . 下列实验方案的设计,不能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 验证 是弱电解质 是弱电解质 | 测量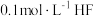 溶液的pH 溶液的pH |
| B | 验证牺牲阳极法 | 用导线连接Zn和Fe,浸入酸化的NaCl溶液中,用胶头滴管从Fe电极区域取少量溶液于试管中,滴入两滴铁氰化钾溶液 |
| C | 测定醋酸溶液的浓度 | 向未知浓度的醋酸溶液中加入甲基橙指示剂,用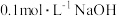 标准溶液滴定,记下指示剂变色时耗碱量并计算 标准溶液滴定,记下指示剂变色时耗碱量并计算 |
| D | 比较 和 和 的 的 大小 大小 | 向等浓度的 和KI混合溶液中逐滴滴加 和KI混合溶液中逐滴滴加 溶液,观察开始生成沉淀的颜色 溶液,观察开始生成沉淀的颜色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-16更新
|
114次组卷
|
2卷引用:四川省仁寿第一中学校南校区2023-2024学年高二上学期12月月考化学试题
8 . 根据下列实验操作和现象所得到的结论不正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 在两支试管中各加入4mL0.01 mol·L−1KMnO4酸性溶液和2 mL0.1mol·L−1H2C2O4溶液,再向其中一支试管中快速加入少量MnSO4固体,加有MnSO4的试管中溶液褪色较快 | Mn2+对该反应有催化作用 |
| B | 相同条件下,测定等浓度的Na2CO3溶液和Na2SO4溶液的pH,前者呈碱性,后者呈中性 | 非金属性:S>C |
| C | 向2mL浓度均为1.0mol·L−1的NaCl、NaI混合溶液中滴加2~3滴0.0l mol·L−1 AgNO3溶液,振荡,有黄色沉淀产生 | Ksp(AgCl)>Ksp(AgI) |
| D | 白铁皮(镀锌铁)出现刮痕后浸泡在饱和食盐水中,一段时间后滴加几滴K3[Fe(CN)6]溶液,无明显现象 | 该过程未发生氧化还原反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 化学与社会、生产、生活密切相关。下列说法正确的是
| A.医疗上用的“钡餐”其成分是碳酸钡,漂白粉的有效成分为次氯酸钙 |
| B.喝补铁剂(含Fe2+)时,加服维生素C效果更好,因维生素C具有还原性 |
| C.5G技术联通世界离不开光纤(光导纤维),光纤的主要成分是晶体硅 |
| D.MgO和Al2O3在工业上用于制作耐高温材料,也可用于电解法冶炼Mg、Al |
您最近一年使用:0次
名校
解题方法
10 . Zn是一种应用广泛的金属。用闪锌矿(主要成分为ZnS,还含有SiO2和少量FeS、CdS、PbS、砷化合物杂质等)为原料制备ZnSO4·7H2O的流程如图所示:

①形成氢氧化物沉淀的pH范围如下:
②ZnSO4·7H2O易溶于水,难溶于酒精。
回答下列问题:
(1)焙烧前应将闪锌矿粉碎,其作用是__ 。滤渣1的主要成分除SiO2外还有__ 。
(2)“氧化除杂”工序中为了不引入新杂质,还可选用的氧化剂是___ 。利用上述表格数据,计算Zn(OH)2的Ksp=__ (列出计算式)
(3)加入ZnO的作用是调节溶液的pH使Fe3+沉淀完全,若“氧化”后Zn2+浓度为1.0mol·L-1则应调节溶液的pH范围是__ 。
(4)制得的ZnSO4·7H2O需洗涤,洗涤晶体时应选用的试剂为__ 。
(5)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为__ 。
(6)回收所得的Cd可用于制造镍镉碱性二次电池,电池工作时,正极NiO(OH)转化为Ni(OH)2的电极反应式为___ 。

①形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
| 开始沉淀的pH(c=0.1mol·L-1) | 1.5 | 6.3 | 6.2 | 7.4 |
| 沉淀完全的pH(c=1.0×10−5mol·L-1) | 2.8 | 8.3 | 8.2 | 9.4 |
回答下列问题:
(1)焙烧前应将闪锌矿粉碎,其作用是
(2)“氧化除杂”工序中为了不引入新杂质,还可选用的氧化剂是
(3)加入ZnO的作用是调节溶液的pH使Fe3+沉淀完全,若“氧化”后Zn2+浓度为1.0mol·L-1则应调节溶液的pH范围是
(4)制得的ZnSO4·7H2O需洗涤,洗涤晶体时应选用的试剂为
(5)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为
(6)回收所得的Cd可用于制造镍镉碱性二次电池,电池工作时,正极NiO(OH)转化为Ni(OH)2的电极反应式为
您最近一年使用:0次
2020-12-16更新
|
455次组卷
|
3卷引用:四川省眉山市洪雅中学2021届高三12月月考理综化学试题
四川省眉山市洪雅中学2021届高三12月月考理综化学试题(已下线)培优08 制备类工业流程(提高练)-2021年高考化学大题培优练(新高考地区专用)甘肃省高台县第一中学2021-2022学年高二下学期6月月考化学试题







