1 . 下列反应的离子方程式错误的是
A.用惰性电极电解氯化镁溶液:2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
B.硫酸铵溶液显酸性: +H2O +H2O NH3•H2O+H+ NH3•H2O+H+ |
C.二元弱酸亚磷酸(H3PO3)溶液中滴加足量的NaOH溶液:H3PO3+2OH-=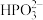 +2H2O +2H2O |
D.硫酸铜溶液遇到难溶的PbS转变为更难溶的CuS:Cu2+(aq)+ (aq)+PbS(s)=CuS(s)+PbSO4(s) (aq)+PbS(s)=CuS(s)+PbSO4(s) |
您最近一年使用:0次
2024-03-10更新
|
32次组卷
|
2卷引用:四川省绵阳中学2023-2024学年高二下学期开学化学试题
名校
2 . 下列说法中正确的是
| A.钡中毒患者可尽快使用苏打溶液洗胃,随即导泻使Ba2+转化为BaCO3而排出 |
B.珊瑚虫从海水中获取Ca2+和HCO ,经反应形成石灰石(CaCO3)外壳,逐渐形成珊瑚 ,经反应形成石灰石(CaCO3)外壳,逐渐形成珊瑚 |
C.泡沫灭火器原理3CO +2Al3++3H2O=2Al(OH)3 +3CO2 +2Al3++3H2O=2Al(OH)3 +3CO2 |
| D.使用含氟牙膏预防龋齿利用了盐类水解的原理 |
您最近一年使用:0次
名校
3 . 下列有关实验的现象和结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向浓度均为0.10 mol·L-1的KCl和KI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 向某浓度的K2CrO4溶液中缓慢滴加少许浓氢氧化钠溶液 | 溶液颜色由黄色变为橙红色 | 减小氢离子浓度,该溶液中的平衡向生成 的方向移动 的方向移动 |
| C | 向盛有某溶液的试管中滴加少量稀NaOH溶液 | 未产生使湿润的红色石蕊试纸变蓝的气体 | 该溶液中不含铵根 |
| D | 用pH计测定pH:①Na2CO3溶液②NaClO溶液 | pH:①>② | H2CO3酸性弱于HClO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-17更新
|
474次组卷
|
4卷引用:四川省江油市太白中学2023-2024学年高三上学期12月月考理综试题
名校
4 . 由软锰矿(主要成分是MnO2,还含有Al2O3、MgO、SiO2等杂质)制备高纯碳酸锰、硫酸锰的一种工艺流程如图所示。
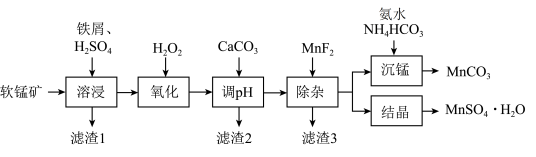
已知:①25℃时,Ksp(MnCO3)=1.8 10-11,Ksp(CaF2)=1.5
10-11,Ksp(CaF2)=1.5 10-10,Ksp(MgF2)=7.4
10-10,Ksp(MgF2)=7.4 10-11。
10-11。
②一定条件下,一些金属氢氧化物沉淀时的pH如表所示。
回答下列问题:
(1)除去铁屑表面油污,可采用的方法是___________ 。
(2)已知“溶浸”时,Fe不能还原MnO2,但Fe2+能还原MnO2得到Mn2+。Fe2+还原MnO2的离子方程式是___________ 。
(3)“氧化”时,过氧化氢的实际消耗量远大于理论消耗量,其原因可能是___________ 。
(4)用CaCO3 “调pH”虽然成本较低,但会引入Ca2+等杂质,若使用___________ (填化学式) “调pH”可避免此问题;调节pH步骤中,应控制的pH范围是___________ 。
(5)滤渣3的主要成分是___________ (填化学式)。
(6)“沉锰”时发生反应的离子方程式为___________ 。
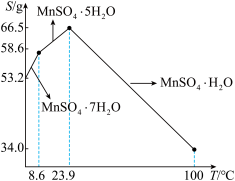
(7)硫酸锰在不同温度下的溶解度和该温度范围内析出晶体的组成如图所示。“结晶”是从“除杂”后过滤所得的滤液中获得MnSO4·H2O。其操作是___________ ,___________ ,洗涤,真空干燥。

已知:①25℃时,Ksp(MnCO3)=1.8
 10-11,Ksp(CaF2)=1.5
10-11,Ksp(CaF2)=1.5 10-10,Ksp(MgF2)=7.4
10-10,Ksp(MgF2)=7.4 10-11。
10-11。②一定条件下,一些金属氢氧化物沉淀时的pH如表所示。
| 金属氢氧化物 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | Al(OH)3 |
| 开始沉淀的pH | 6.8 | 2.3 | 8.1 | 3.4 |
| 完全沉淀的pH | 8.3 | 3.2 | 10 | 4.7 |
(1)除去铁屑表面油污,可采用的方法是
(2)已知“溶浸”时,Fe不能还原MnO2,但Fe2+能还原MnO2得到Mn2+。Fe2+还原MnO2的离子方程式是
(3)“氧化”时,过氧化氢的实际消耗量远大于理论消耗量,其原因可能是
(4)用CaCO3 “调pH”虽然成本较低,但会引入Ca2+等杂质,若使用
(5)滤渣3的主要成分是
(6)“沉锰”时发生反应的离子方程式为
(7)硫酸锰在不同温度下的溶解度和该温度范围内析出晶体的组成如图所示。“结晶”是从“除杂”后过滤所得的滤液中获得MnSO4·H2O。其操作是

您最近一年使用:0次
2023-11-05更新
|
305次组卷
|
2卷引用:四川省绵阳南山中学实验学校2023-2024学年高三(补习班)上学期11月月理科综合试题
解题方法
5 . 七水合硫酸镁(MgSO4•7H2O)在印染、造纸等领域应用广泛。以化工废弃物盐泥(主要成分为MgCO3•CaCO3,含少量NaCl与含铁化合物)为原料可制取七水合硫酸镁,回答下列问题:
(1)称取干燥盐泥6.90g于100mL烧杯中,加入蒸馏水,缓慢滴加3.0mol•L-1H2SO4溶液,不断搅拌,得到酸解浆液,主要反应的化学方程式为________ ;配制3.0mol•L-1H2SO4溶液时,用到的实验仪器除烧杯、玻璃棒、量筒外,还必须使用的仪器有________ (填标号)。
A. B.
B.  C.
C.  D.
D.
(2)加热酸解浆液,在搅拌下补加盐泥,调节浆液的pH接近6,继续加热煮沸,趁热过滤,滤渣的主要成分是________ 、________ ,继续加热煮沸的目的是________ 。
(3)要证明铁元素已除尽,实验操作及现象是:________ 。
(4)向(2)所得滤液中加入6mol•L-1NaOH溶液至沉淀完全,过滤,该操作的目的是________ ,将滤渣完全溶于3.0mol•L-1H2SO4溶液,经如下实验操作:加热蒸发、________ 、过滤、洗涤、干燥,得到七水合硫酸镁。
(5)实验中制得七水合硫酸镁产品的质量为3.69g,则盐泥中MgCO3•CaCO3的含量为________ %,将产品加热至77℃,测得固体失重率为43.9%,该温度下固体的化学式为________ 。
(1)称取干燥盐泥6.90g于100mL烧杯中,加入蒸馏水,缓慢滴加3.0mol•L-1H2SO4溶液,不断搅拌,得到酸解浆液,主要反应的化学方程式为
A.
 B.
B.  C.
C.  D.
D.
(2)加热酸解浆液,在搅拌下补加盐泥,调节浆液的pH接近6,继续加热煮沸,趁热过滤,滤渣的主要成分是
(3)要证明铁元素已除尽,实验操作及现象是:
(4)向(2)所得滤液中加入6mol•L-1NaOH溶液至沉淀完全,过滤,该操作的目的是
(5)实验中制得七水合硫酸镁产品的质量为3.69g,则盐泥中MgCO3•CaCO3的含量为
您最近一年使用:0次
6 . 某科研人员以废镍催化剂(主要成分为 ,另含
,另含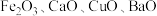 )为原料回收镍,工艺流程如图。
)为原料回收镍,工艺流程如图。 如表。
如表。
回答下列问题:
(1)浸出渣主要成分为___________ 、___________ 。(填化学式)
(2)“除铜”时, 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
(3)“氧化”的目的是将溶液中 氧化为
氧化为 ,写出该反应的离子方程式
,写出该反应的离子方程式___________ 。温度需控制在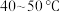 之间,该步骤温度不能太高的原因是
之间,该步骤温度不能太高的原因是___________ 。
(4)“调 ”时,
”时, 的控制范围为
的控制范围为___________ 。
(5)“除钙”后,若溶液中 浓度为
浓度为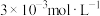 ,则
,则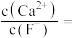
___________ 。[已知常温下, ]
]
(6)用可溶性碳酸盐,可以浸取 固体,在溶液浸取过程发生反应:
固体,在溶液浸取过程发生反应: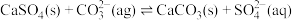 。已知:
。已知: 时,
时,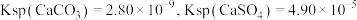 ,则此温度下该反应的平衡常数K为
,则此温度下该反应的平衡常数K为___________ (计算结果保留三位有效数字)。
 ,另含
,另含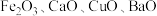 )为原料回收镍,工艺流程如图。
)为原料回收镍,工艺流程如图。
 如表。
如表。| 氢氧化物 |  |  |  |
开始沉淀的 | 1.5 | 6.5 | 7.7 |
沉淀完全的 | 3.7 | 9.7 | 9.2 |
(1)浸出渣主要成分为
(2)“除铜”时,
 与
与 反应的离子方程式为
反应的离子方程式为(3)“氧化”的目的是将溶液中
 氧化为
氧化为 ,写出该反应的离子方程式
,写出该反应的离子方程式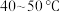 之间,该步骤温度不能太高的原因是
之间,该步骤温度不能太高的原因是(4)“调
 ”时,
”时, 的控制范围为
的控制范围为(5)“除钙”后,若溶液中
 浓度为
浓度为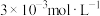 ,则
,则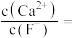
 ]
](6)用可溶性碳酸盐,可以浸取
 固体,在溶液浸取过程发生反应:
固体,在溶液浸取过程发生反应: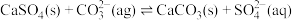 。已知:
。已知: 时,
时,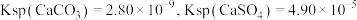 ,则此温度下该反应的平衡常数K为
,则此温度下该反应的平衡常数K为
您最近一年使用:0次
2023-09-16更新
|
868次组卷
|
4卷引用:四川省绵阳中学2023-2024学年高二下学期开学化学试题
名校
解题方法
7 . 铟(In)是一种稀散金属,常与其他金属矿石伴生,回收氧化锌烟尘(主要成分是ZnO,还含少量PbO、FeS、FeSiO3、 In2O3、 In2S3等)中的金属铟的工艺流程如下:
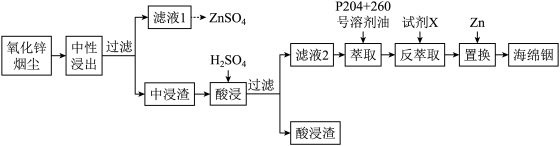
已知:室温下,金属离子开始沉淀和完全沉淀的pH如表所示。
回答下列问题:
(1)In2O3中In的化合价是_______________________ 。
(2)“中性浸出”的过程为:先加入稀硫酸和适量氧化剂MnO2氧化酸浸氧化锌烟尘,反应结束前半个小时加入CaO调整pH=5.0~5.2。
①FeSiO3与稀H2SO4反应的化学方程式为____________________________________________ 。
②氧化酸浸过程中,In2S3中的硫元素被MnO2氧化为 ,该反应的离子方程式为
,该反应的离子方程式为____________________ 。
③氧化剂用量对中性浸出效果的影响如图所示。最佳氧化剂用量为_________________ 。
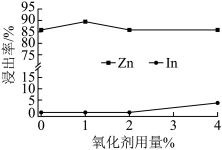
④“中浸渣”的主要成分为In(OH)3、________________ 。 (写化学式)
(3)萃取时,发生反应In3+ +3H2A2 In(HA2)3 +3H+,H2A2代表有机萃取剂。
In(HA2)3 +3H+,H2A2代表有机萃取剂。
①反萃取时,宜选用的试剂X为_____________________ (写化学式)
②实验室进行萃取和反萃取时,均需要使用的玻璃仪器有_________________________ 。
(4)“置换”后的滤液可返回________________________ (填“滤液 1”或“滤液2”)中利用。
(5)“置换”时锌粉的利用率为90%,若想获得6.9 kg海绵铟,需要使用锌粉___ _kg (结果保留1位小数)

已知:室温下,金属离子开始沉淀和完全沉淀的pH如表所示。
金属离子 | Fe3+ | Fe2+ | In3+ |
开始沉淀pH(离子浓度为0.1mol·L-1时) | 1.3 | 6 | 3 |
完全沉淀pH | 2.7 | 8 | 4.3 |
(1)In2O3中In的化合价是
(2)“中性浸出”的过程为:先加入稀硫酸和适量氧化剂MnO2氧化酸浸氧化锌烟尘,反应结束前半个小时加入CaO调整pH=5.0~5.2。
①FeSiO3与稀H2SO4反应的化学方程式为
②氧化酸浸过程中,In2S3中的硫元素被MnO2氧化为
 ,该反应的离子方程式为
,该反应的离子方程式为③氧化剂用量对中性浸出效果的影响如图所示。最佳氧化剂用量为

④“中浸渣”的主要成分为In(OH)3、
(3)萃取时,发生反应In3+ +3H2A2
 In(HA2)3 +3H+,H2A2代表有机萃取剂。
In(HA2)3 +3H+,H2A2代表有机萃取剂。①反萃取时,宜选用的试剂X为
②实验室进行萃取和反萃取时,均需要使用的玻璃仪器有
(4)“置换”后的滤液可返回
(5)“置换”时锌粉的利用率为90%,若想获得6.9 kg海绵铟,需要使用锌粉
您最近一年使用:0次
名校
解题方法
8 . 回答下列问题
(1)写出过量Mg(OH)2固体放入水中溶解形成饱和溶液时的溶解平衡表达式________________________________ ,向有Mg(OH)2沉淀的溶液中加入过量浓NH4Cl,溶液变澄清,相关反应的化学方程式为____________________________ ,已知室温时饱和的Mg(OH)2溶液的pH=10,则Mg(OH)2的溶度积为___________ 。
(2)明矾是KAl(SO4)2·12H2O,其溶液中离子浓度由大到小的顺序______________________ ;向明矾溶液中逐渐滴入Ba(OH)2 溶液至SO 离子恰好沉淀完全时,溶液的显
离子恰好沉淀完全时,溶液的显_______ 性(填酸、碱、中),离子反应的总方程式:_________________________________________________ 。
(3)为配制SbCl3溶液,取少量SbCl3固体,加2mL~3mL水溶解,此时却会产生白色沉淀Sb2O3,写出此时反应的化学方程式为:___________________________ ,故在配制SbCl3溶液时应加少量____________ 。
(1)写出过量Mg(OH)2固体放入水中溶解形成饱和溶液时的溶解平衡表达式
(2)明矾是KAl(SO4)2·12H2O,其溶液中离子浓度由大到小的顺序
 离子恰好沉淀完全时,溶液的显
离子恰好沉淀完全时,溶液的显(3)为配制SbCl3溶液,取少量SbCl3固体,加2mL~3mL水溶解,此时却会产生白色沉淀Sb2O3,写出此时反应的化学方程式为:
您最近一年使用:0次
名校
解题方法
9 . 根据下列实验操作,现象和结论都正确的是
| 实验操作 | 现象 | 结论 | |
| A | 等体积、pH=3的两种酸HA和HB,分别与足量Zn反应 | HA放出的氢气多 | 酸性:HA<HB |
| B | 向AgNO3溶液中依次滴加NaCl、KI溶液 | 依次出现白色、黄色沉淀 | 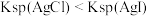 |
| C | 用pH试纸测定NaCl与NaF溶液的pH | 前者小于后者 | 非金属性:F<Cl |
| D | 用pH试纸测定饱和新制氯水的pH | pH试纸变红色 | 饱和新制氯水呈酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-15更新
|
281次组卷
|
2卷引用:四川省绵阳南山中学2023-2024学年高二下学期入学考试化学试题
名校
10 . 某温度下,向 溶液中滴加
溶液中滴加 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中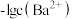 与
与 溶液体积
溶液体积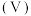 的关系如图所示,已知
的关系如图所示,已知 。下列说法正确的是
。下列说法正确的是
 溶液中滴加
溶液中滴加 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中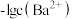 与
与 溶液体积
溶液体积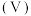 的关系如图所示,已知
的关系如图所示,已知 。下列说法正确的是
。下列说法正确的是
| A.溶液b点可以通过升高温度到达c点 |
B.该温度下 |
C.b点溶液中: |
D.若把 溶液换成等浓度 溶液换成等浓度 溶液,则曲线变为Ⅱ 溶液,则曲线变为Ⅱ |
您最近一年使用:0次
2023-05-04更新
|
454次组卷
|
4卷引用:四川省绵阳南山中学2023-2024学年高二上学期12月月考化学试题



