名校
1 . 工业上向锅炉里注入Na2CO3溶液浸泡,将水垢中的CaSO4转化为CaCO3,而后用盐酸去除。下列叙述不正确的是
| A.温度升高,Na2CO3溶液的Kw和c(OH-)均会增大 |
B.沉淀转化的离子方程式为CO (aq)+CaSO4(s)⇌CaCO3(s)+SO (aq)+CaSO4(s)⇌CaCO3(s)+SO (aq) (aq) |
| C.盐酸溶液中,CaCO3的溶解性大于CaSO4 |
| D.Na2CO3溶液遇CO2后,阴离子浓度均减小 |
您最近半年使用:0次
2021-03-14更新
|
1507次组卷
|
18卷引用:2015届四川省成都市高三第一次诊断性检测理综化学试卷
2015届四川省成都市高三第一次诊断性检测理综化学试卷2016届河北省衡水市冀州中学高三上一轮复习检测二化学试卷2015-2016学年黑龙江省鹤岗一中高二上期末考试化学试卷2015-2016学年天津市红桥区高二上学期期末考试化学试卷2016-2017学年湖北省武钢三中高二12月月考化学试卷2017届河北省冀州中学高三(高复班)上学期一轮检测(二)化学试卷(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)作业10 沉淀溶解平衡-2021年高二化学暑假作业(人教版2019)(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第15练 反应原理综合-2022年【寒假分层作业】高二化学(人教版2019选择性必修2)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练重庆市巫山县官渡中学2020-2021年高二下学期第二次月考化学试题(已下线)第22讲 沉淀溶解平衡的应用(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 第2课时 沉淀溶解平衡的应用(已下线)第5讲 难溶电解质的溶解平衡
名校
2 . 25℃时,下列4种盐的溶度积常数(Ksp)分别是:结合相关数据分析,下列说法错误的是
| Ag2SO4(白色) | Ag2S(黑色) | FeS(黑色) | MnS(肉色) |
| 1.4×10-5mol3·L-3 | 6.3×10-50mol3·L-3 | 3.3×10-18mol2·L-2 | 2.5×10-13mol2·L-2 |
| A.除去某溶液中的Ag+用Na2S溶液比Na2SO4溶液效果好 |
| B.25℃时,MnS的溶解度大于FeS的溶解度 |
| C.向少量FeS悬浊液中加入足量饱和MnCl2溶液,沉淀颜色会由黑色变为肉色 |
D.向Ag2S(s) 2Ag+(aq)+S2-(aq)平衡体系中加入少量Na2S固体,溶液中c(Ag+)增大 2Ag+(aq)+S2-(aq)平衡体系中加入少量Na2S固体,溶液中c(Ag+)增大 |
您最近半年使用:0次
名校
解题方法
3 . 根据下列实验操作和现象所得出的结论正确的是
实验内容 | 实验结论 | |
A | 向1mL0.1mol·L-1NaOH溶液中加入2mL0.1mol·L-1CuSO4溶液,振荡后滴加0.5mL葡萄糖溶液,加热未出现红色沉淀 | 葡萄糖中不含有醛基 |
B | 向1mL0.2mol·L-1NaOH溶液中滴入2滴0.1mol·L-1MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol·L-1FeCl3溶液,又生成红褐色沉淀 | 在相同温度下,Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
C | 测定同温度下相同物质的量浓度的碳酸钠和硫酸钠溶液的pH,前者大于后者 | 碳元素非金属性弱于硫 |
D | 向某溶液中滴加少量稀NaOH溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 溶液中不含 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2021-03-07更新
|
1876次组卷
|
5卷引用:江苏省苏州市相城区陆慕高级中学2021届高三上学期期中考试化学试卷
江苏省苏州市相城区陆慕高级中学2021届高三上学期期中考试化学试卷(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(选择题11-13)江苏省镇江第一中学2023-2024学年高三上学期期初阶段学情检测化学试题
解题方法
4 . 下列指定反应的离子方程式正确的是
A.酸化的NaIO3和NaI的溶液混合:I- +IO +6H+=I2 +3H2O +6H+=I2 +3H2O |
| B.实验室用氯化铝溶液和氨水制备氢氧化铝:Al3++3OH-=Al(OH)3↓ |
C.饱和Na2CO3溶液与CaSO4固体反应:CO (aq)+CaSO4(s) (aq)+CaSO4(s)  CaCO3(s)+SO CaCO3(s)+SO (aq) (aq) |
| D.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2 :Fe2++2OH-=Fe(OH)2 ↓ |
您最近半年使用:0次
名校
5 . 下列实验操作中,对应的现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向较浓的FeCl2溶液中滴入少量酸性KMnO4溶液 | KMnO4溶液紫色褪去 | Fe2+有还原性 |
| B | 分别向两支试管中加入同浓度、同体积的草酸溶液,再分别加入同体积、不同浓度的酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色时间不同 | 浓度不同反应速率不同 |
| C | 用pH试纸分别测定等浓度的NaClO和NaHCO3的pH值 | pH:NaClO>NaHCO3 | 酸性:H2CO3>HClO |
| D | 向浓度均为0.1 mol·L-1的MgCl2、CuCl2混合溶液中逐滴加入氨水 | 先出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2021-03-01更新
|
526次组卷
|
7卷引用:福建省福州第一中学2020届高三第二次测试理综化学试题
福建省福州第一中学2020届高三第二次测试理综化学试题(已下线)重点2 表格逻辑型实验方案的设计与评价-2021年高考化学【热点·重点·难点】专练(新高考)(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点35 化学实验方案的设计与评价-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考向35 实验的方案设计与评价-备战2022年高考化学一轮复习考点微专题广东省广州市中山大学附属中学2021届高三下学期3月月考化学试题新疆乌鲁木齐市高级中学2023-2024学年高二上学期1月期末化学试题
名校
6 . 下列化学原理的应用,主要用难溶电解质的溶解平衡原理解释的是
①稀醋酸中加入少量醋酸钠能抑制醋酸的电离 ②误将钡盐[BaCl2、Ba(NO3)2]当作食盐服用后,常用0.5%的Na2SO4溶液解毒 ③CuSO4溶液遇ZnS(闪锌矿)转化为CuS(铜蓝) ④碳酸钡不能作“钡餐”而硫酸钡则能 ⑤泡沫灭火器灭火的原理
①稀醋酸中加入少量醋酸钠能抑制醋酸的电离 ②误将钡盐[BaCl2、Ba(NO3)2]当作食盐服用后,常用0.5%的Na2SO4溶液解毒 ③CuSO4溶液遇ZnS(闪锌矿)转化为CuS(铜蓝) ④碳酸钡不能作“钡餐”而硫酸钡则能 ⑤泡沫灭火器灭火的原理
| A.①②③④⑤ | B.①②③ | C.③④⑤ | D.②③④ |
您最近半年使用:0次
7 . 镍行业发展蕴藏着巨大的潜力。某小组用废镍催化剂(成分为Al2O3、Ni、Fe、SiO2、CaO等)制备草酸镍晶体(NiC2O4·2H2O)的部分实验流程如下:

已知:①Ksp(CaF2)=1.6×10-10、Ksp[Fe(OH)2]=8.0×10-16、Ksp[Fe(OH)3]=4.0×10-38、Ksp[Al(OH)3]=2.7×10-34;
②认为残留在溶液中的离子浓度小于1×10-5mol/L即沉淀完全。
(1)“粉碎”的目的是___________ 。滤渣Ⅰ的成分有___________ (化学式)。
(2)在“调pH”过程中,应先加入H2O2,发生反应的离子方程式为___________ ,沉淀剂可选择___________ 。(填序号)
a.NiOb.NaOHc.Ni(OH)2d.NiCO3
为将Al3+、Fe3+沉淀完全,至少应调节pH到___________ (已知lg3≈0.5)。
(3)在“沉淀”过程中,Ca2+刚好沉淀完全时,溶液中c(F-)=___________ mol/L。
(4)将得到的草酸镍晶体在真空中加热至320℃分解,可重新制得单质镍,且还生成一种气体,请写出该制备过程的化学方程式:___________ 。

已知:①Ksp(CaF2)=1.6×10-10、Ksp[Fe(OH)2]=8.0×10-16、Ksp[Fe(OH)3]=4.0×10-38、Ksp[Al(OH)3]=2.7×10-34;
②认为残留在溶液中的离子浓度小于1×10-5mol/L即沉淀完全。
(1)“粉碎”的目的是
(2)在“调pH”过程中,应先加入H2O2,发生反应的离子方程式为
a.NiOb.NaOHc.Ni(OH)2d.NiCO3
为将Al3+、Fe3+沉淀完全,至少应调节pH到
(3)在“沉淀”过程中,Ca2+刚好沉淀完全时,溶液中c(F-)=
(4)将得到的草酸镍晶体在真空中加热至320℃分解,可重新制得单质镍,且还生成一种气体,请写出该制备过程的化学方程式:
您最近半年使用:0次
2021-02-08更新
|
341次组卷
|
3卷引用:四川省成都市第七中学2020-2021学年高二上学期12月阶段性测试化学试题
名校
解题方法
8 . 下列由实验得出的结论正确的是
| 选项 | 实验 | 结论 |
| A | 常温下,测得0.1mol/LNaA溶液的pH小于0.1mol/LNaB溶液的pH | 酸性:HA<HB |
| B | 向pH=3的醋酸溶液中,加入醋酸钠溶液,溶液pH增大 | 醋酸钠溶液呈碱性 |
| C | 向2支盛有5mL不同浓度的Na2S2O3溶液的试管中同时加入5mL0.1mol/L硫酸溶液,记录出现浑浊的时间 | 探究浓度对反应速率的影响 |
| D | 向盛有2mL0.1mol/LAgNO3的试管中滴加5滴0.1mol/LNaCl溶液,出现白色沉淀;再往试管中滴加5滴0.1mol/LKI溶液,出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2021-02-08更新
|
237次组卷
|
2卷引用:四川省成都市第七中学2020-2021学年高二上学期12月阶段性测试化学试题
名校
9 . 化学与人类生活、生产息息相关。下列说法错误的是
| A.用纯碱溶液清洗油污,加热可增强去污力 |
| B.可施加适量石膏降低盐碱地(含较多NaCl、Na2CO3)土壤的碱性 |
| C.可以利用水解反应获得纳米材料 |
| D.草木灰和铵态氮肥混合使用能使肥效增强 |
您最近半年使用:0次
2021-02-08更新
|
301次组卷
|
4卷引用:四川省成都市第七中学2020-2021学年高二上学期12月阶段性测试化学试题
名校
解题方法
10 . 以炼锌厂的烟道灰(主要成分为ZnO,还含有少量Fe2O3、CuO、SiO2、MnO等)为原料可生产草酸锌晶体(ZnC2O4·2H2O),其工艺流程如图所示:
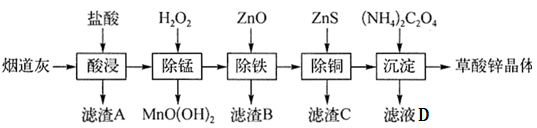
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
(1)酸浸后产生的金属阳离子主要有Zn2+,还有少量______ ;滤渣A的主要成分为______ (填化学式)。
(2)盐酸酸浸过程中,为了提高浸取效率,可采取的措施有______ (写出两条即可)。
(3)“除锰”过程中加入H2O2的作用为______ (用离子方程式表示)。
(4)“调pH”控制溶液的pH范围为3.3≤pH<5.4,滤渣B的成分有______ (填化学式)。
(5)生成滤渣C的离子方程式为______ 。
(6)滤液D和草酸锌晶体分离的操作为______ (写操作名称)。

有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 1.9 | 4.2 | 5.4 |
| 完全沉淀时的pH | 3.3 | 6.7 | 8.2 |
(2)盐酸酸浸过程中,为了提高浸取效率,可采取的措施有
(3)“除锰”过程中加入H2O2的作用为
(4)“调pH”控制溶液的pH范围为3.3≤pH<5.4,滤渣B的成分有
(5)生成滤渣C的离子方程式为
(6)滤液D和草酸锌晶体分离的操作为
您最近半年使用:0次
2021-02-08更新
|
142次组卷
|
2卷引用:河北省张家口市张垣联盟2020-2021学年高二上学期阶段检测化学试题



