1 . 科技乃兴国之重。下列说法正确的是
| A.“天问一号”实验舱所使用的铝合金熔点高于其各组分金属 |
| B.中国天眼望远镜所使用的高性能SiC属于有机高分子材料 |
| C.“歼-35”战斗机机翼所使用的“碳纤维布”(聚丙烯腈经碳化而成)与金刚石互为同素异形体 |
| D.港珠澳大桥使用环氧树脂作为防腐涂料,它可以减小海水与桥体金属间的腐蚀电流 |
您最近半年使用:0次
解题方法
2 . 只利用下列实验药品,不能达到实验目的的是
| 实验目的 | 实验药品 | |
| A | 探究温度对化学平衡的影响 |  与 与 混合气体、冷水、热水 混合气体、冷水、热水 |
| B | 验证乙醇的消去产物是乙烯 | 乙醇、酸性高锰酸钾溶液、浓硫酸 |
| C | 证明牺牲阳极法保护铁 |  、 、 、酸化的食盐水、 、酸化的食盐水、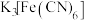 溶液 溶液 |
| D | 比较水和四氯化碳分子的极性 |  、 、 、 、 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
3 . 下列叙述Ⅰ和叙述Ⅱ均正确,且有因果关系的是
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | 石墨能导电且化学性质不活泼 | 阴极电保护法中可用石墨作辅助阳极 |
B | 煤中含有苯、甲苯等芳香烃 | 通过煤的干馏可获得苯、甲苯等芳香烃 |
C | 铝制容器和浓硫酸不反应 | 铝制容器用于存储、运输浓硫酸 |
D | 断裂氨分子中的化学键需要吸收热量 | 工业上用液氨作制冷剂 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-04-02更新
|
320次组卷
|
2卷引用:2024届山东省枣庄市高三下学期模拟考试(二调)化学试题
4 . 下列应用与氧化还原反应无关的是
| A.稀硝酸用于溶解铜锈 | B.铁粉暖贴用于冬天取暖 |
| C.青蒿素氢化制备双氢青蒿素 | D.三元催化器处理机动车尾气 |
您最近半年使用:0次
2024-04-02更新
|
254次组卷
|
2卷引用:2024届山东省枣庄市高三下学期模拟考试(二调)化学试题
5 . 锌及锌合金(如黄铜、白口铁等)广泛用于生产、生活。某小组拟以锌矿(主要成分是ZnS,含少量FeS等杂质)为原料采用多种方法冶炼锌的流程如下:
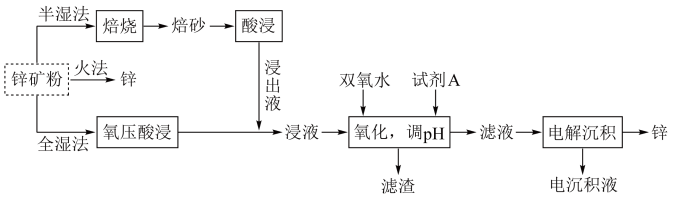
已知: 是两性氢氧化物,易溶于
是两性氢氧化物,易溶于 溶液,也溶于氨水,能发生相关反应:
溶液,也溶于氨水,能发生相关反应: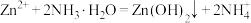 ,
,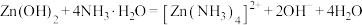 。
。
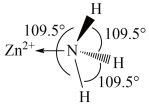
(1)已知 (结构如图所示)中
(结构如图所示)中 采用
采用 杂化,由此推知:
杂化,由此推知: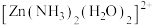 有
有___________ 种结构。NH3分子中键角为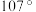 ,与
,与 中配体
中配体 键角不同的原因是
键角不同的原因是___________ 。
(2)明代宋应星著的《天工开物》中有关“升炼倭铅”的记载:“每炉甘石十斤,装载人一泥罐内,封裹泥固,……然后逐层用煤炭饼垫盛,其底铺薪,发火㲎红,……冷定毁罐取出。……即倭铅也。”(炉甘石主要成分是 ,倭铅即指
,倭铅即指 )。由此可知,古代炼锌方法类似上述三种方法中
)。由此可知,古代炼锌方法类似上述三种方法中___________ (填字母,下同)。
a.半湿法 b.火法 c.全湿法
上述三种方法中,最佳方法是___________ 。
(3)“氧压酸浸”即在一定浓度稀硫酸中加入锌矿粉,并在加压下通入 ,除生成
,除生成 外,还能回收非金属单质。写出主要反应的离子方程式:
外,还能回收非金属单质。写出主要反应的离子方程式:___________ 。
(4)若将“氧化、调 ”步骤改为直接用过量的
”步骤改为直接用过量的 或氨水进行除杂,该操作是否会对“电解沉积”过程造成影响,
或氨水进行除杂,该操作是否会对“电解沉积”过程造成影响,___________ (填“是”或“否”),请说明原因:___________ 。
(5)“电解沉积”(以情性材料为电极)中阳极反应式为___________ 。航母外壳常镶嵌一些锌块,这种保护航母的电化学方法叫___________ 。

已知:
 是两性氢氧化物,易溶于
是两性氢氧化物,易溶于 溶液,也溶于氨水,能发生相关反应:
溶液,也溶于氨水,能发生相关反应: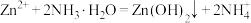 ,
,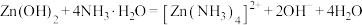 。
。(1)已知
 (结构如图所示)中
(结构如图所示)中 采用
采用 杂化,由此推知:
杂化,由此推知: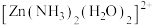 有
有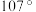 ,与
,与 中配体
中配体 键角不同的原因是
键角不同的原因是
(2)明代宋应星著的《天工开物》中有关“升炼倭铅”的记载:“每炉甘石十斤,装载人一泥罐内,封裹泥固,……然后逐层用煤炭饼垫盛,其底铺薪,发火㲎红,……冷定毁罐取出。……即倭铅也。”(炉甘石主要成分是
 ,倭铅即指
,倭铅即指 )。由此可知,古代炼锌方法类似上述三种方法中
)。由此可知,古代炼锌方法类似上述三种方法中a.半湿法 b.火法 c.全湿法
上述三种方法中,最佳方法是
(3)“氧压酸浸”即在一定浓度稀硫酸中加入锌矿粉,并在加压下通入
 ,除生成
,除生成 外,还能回收非金属单质。写出主要反应的离子方程式:
外,还能回收非金属单质。写出主要反应的离子方程式:(4)若将“氧化、调
 ”步骤改为直接用过量的
”步骤改为直接用过量的 或氨水进行除杂,该操作是否会对“电解沉积”过程造成影响,
或氨水进行除杂,该操作是否会对“电解沉积”过程造成影响,(5)“电解沉积”(以情性材料为电极)中阳极反应式为
您最近半年使用:0次
6 . 请按要求回答下列问题。
(1)25℃,pH=1的CH3COOH溶液中由水电离出的H+浓度约为_______ mol•L-1。
(2)如图烧杯中盛的是海水,铁腐蚀的速率最慢的是_______ (填标号)。
(3)用如图所示的装置研究电化学的相关问题(乙装置中X为阳离子交换膜)。
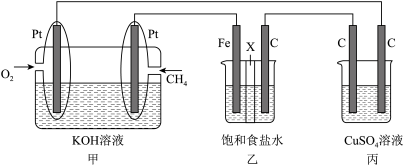
①甲装置中负极反应式为_______ 。
②乙装置中石墨电极上生成的气体为_______ (填化学式)。
③丙装置中CuSO4足量,工作一段时间后,溶液的pH_______ (填“变大”、“变小”或“不变”),反应的化学方程式为_______ ,若要将电解后的溶液复原,需加入一定量的_______ (填化学式)。
(1)25℃,pH=1的CH3COOH溶液中由水电离出的H+浓度约为
(2)如图烧杯中盛的是海水,铁腐蚀的速率最慢的是
A.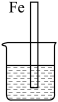 | B. | C.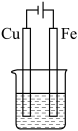 | D. |
(3)用如图所示的装置研究电化学的相关问题(乙装置中X为阳离子交换膜)。

①甲装置中负极反应式为
②乙装置中石墨电极上生成的气体为
③丙装置中CuSO4足量,工作一段时间后,溶液的pH
您最近半年使用:0次
7 . 下列说法正确的是
| A.电解精炼铜时溶液中的铜离子浓度不会减少 |
| B.电镀时,应把镀件置于电解池的阳极 |
| C.燃料电池发电比直接燃烧产生热量发电能量转换率高,且可组合成“绿色发电站” |
| D.电化学防护中牺牲阳极保护法利用了电解原理 |
您最近半年使用:0次
解题方法
8 . 美籍华裔化学家钱永健16岁时,凭借一个金属易受硫氰酸盐腐蚀的调查项目,荣获具有“少年诺贝尔奖”之称的著名奖项。下列说法正确的是
| A.金属腐蚀就是金属原子失去电子被还原的过程 |
| B.合金都比纯金属易被腐蚀 |
| C.将金属与外加直流电源的负极相连,可以防止金属被腐蚀 |
| D.镀锌铁比镀锡铁更容易被腐蚀 |
您最近半年使用:0次
9 . 铁、铜等金属在生产和生活中有着广泛的应用。回答下列问题:
(1)某研究性学习小组设计了如下图所示装置探究钢铁的腐蚀与防护,烧杯内液体均为饱和食盐水。
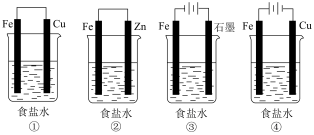
在相同条件下,四组装置中铁电极腐蚀最快的是___________ (填序号,下同);为防止金属被腐蚀,可以采用上述___________ 装置原理进行防护。
(2)钴酸锂电池是目前常见的锂离子二次电池,电池总反应为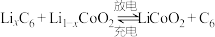 ,用它做电源按如图装置进行电解,通电后,d电极附近先出现白色沉淀(CuCl)。
,用它做电源按如图装置进行电解,通电后,d电极附近先出现白色沉淀(CuCl)。
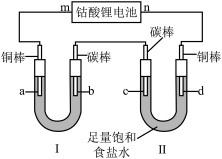
①放电时,负极反应式为___________ 。
②该电池充电时,n极接电源的___________ 极,试写出装置Ⅱ中d电极附近产生白色沉淀的反应式___________ 。
③电极a上的现象是___________ 。
④若装置I为铜上镀银,则装置I中U形管内的溶液为___________ (填化学式,下同),电解一段时间后,若铜棒上无气体产生,要使溶液恢复原状态,需加入___________ 。
(1)某研究性学习小组设计了如下图所示装置探究钢铁的腐蚀与防护,烧杯内液体均为饱和食盐水。

在相同条件下,四组装置中铁电极腐蚀最快的是
(2)钴酸锂电池是目前常见的锂离子二次电池,电池总反应为
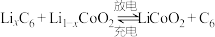 ,用它做电源按如图装置进行电解,通电后,d电极附近先出现白色沉淀(CuCl)。
,用它做电源按如图装置进行电解,通电后,d电极附近先出现白色沉淀(CuCl)。
①放电时,负极反应式为
②该电池充电时,n极接电源的
③电极a上的现象是
④若装置I为铜上镀银,则装置I中U形管内的溶液为
您最近半年使用:0次
10 . 用如图所示装置及试剂进行铁的电化学腐蚀实验探究,测定具支锥形瓶中压强和溶解氧随时间的变化关系,曲线如下。下列说法正确的是
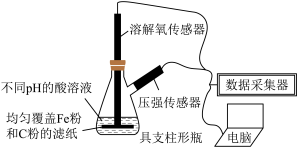



| A.pH=6.0时,只发生析氢腐蚀 |
B.整个过程中,负极电极反应式均为: |
| C.pH=2.0和pH=4.0时,同时发生析氢腐蚀和吸氧腐蚀 |
| D.将铁换成铜进行实验,pH=2.0时,压强随时间变化的曲线与铁完全相同 |
您最近半年使用:0次



