1 . 下列实验操作与实验现象及结论对应且正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将镀层有破坏的镀锌铁片放入酸化的3%NaCl溶液中,一段时间后,取溶液于试管中,滴加KSCN溶液 | 无红色出现 | 铁未被腐蚀,已破损的镀层锌仍能起到保护的作用 |
| B | 用湿润的淀粉碘化钾试纸鉴别NO2、溴蒸气 | 试纸变蓝 | 该气体为溴蒸气 |
| C | 向久置于空气中的Na2O2固体中滴加稀硫酸 | 有气泡产生 | Na2O2已变质成Na2CO3 |
| D | 向新制饱和氯水中加入过量的碳酸钙粉末,振荡 | 产生大量气泡 | 提高了新制氯水中次氯酸的浓度 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 化学与生产、生活和科技密切相关,下列说法错误的是
| A.北京冬奥会运动员“战袍”内层添加石墨烯片用于保暖,石墨烯和碳纳米管互为同分异构体 |
| B.华为自主研发的“麒麟”芯片与太阳能电池感光板所用材料均为晶体硅 |
| C.氮化硅陶瓷属于新型无机非金属材料, 可用于制造汽车发动机 |
| D.不锈钢中含有镍、铬等元素, 具有很强的抗腐蚀能力 |
您最近半年使用:0次
名校
3 . 电化学方法是化工生产及生活中常用的一种方法。回答下列问题:
I.二氧化氯( )为一种黄绿色气体,是国际上公认的高效、快速、安全的杀菌消毒剂。目前已开发出用电解法制取
)为一种黄绿色气体,是国际上公认的高效、快速、安全的杀菌消毒剂。目前已开发出用电解法制取 的新工艺如图所示:
的新工艺如图所示:
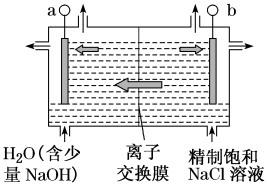
(1)图中用石墨作电极,在一定条件下电解饱和食盐水制取 。产生
。产生 的电极应连接电源的
的电极应连接电源的_______ (填“正极”或“负极”),对应的电极反应式为_______ 。
(2)a极区溶液的
_______ (填“增大”“减小”或“不变”)。
(3)图中离子交换膜应使用_______ (填“阴”或“阳”)离子交换膜。
Ⅱ.在日常生活中,金属腐蚀的现象普遍存在,某化学兴趣小组设计了如图所示的两套实验装置验证 的腐蚀与防护:
的腐蚀与防护:
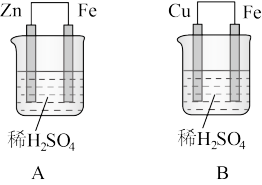
(4)图中能保护 不被腐蚀的是装置
不被腐蚀的是装置_______ (填“A”或“B”),其保护方法的名称是_______ 。
(5)另一装置中 极的电极反应式为
极的电极反应式为_______ ,检验其阳离子产物时加入_______ 溶液,产生特征蓝色沉淀,其反应离子方程式为_______ 。
I.二氧化氯(
 )为一种黄绿色气体,是国际上公认的高效、快速、安全的杀菌消毒剂。目前已开发出用电解法制取
)为一种黄绿色气体,是国际上公认的高效、快速、安全的杀菌消毒剂。目前已开发出用电解法制取 的新工艺如图所示:
的新工艺如图所示:
(1)图中用石墨作电极,在一定条件下电解饱和食盐水制取
 。产生
。产生 的电极应连接电源的
的电极应连接电源的(2)a极区溶液的

(3)图中离子交换膜应使用
Ⅱ.在日常生活中,金属腐蚀的现象普遍存在,某化学兴趣小组设计了如图所示的两套实验装置验证
 的腐蚀与防护:
的腐蚀与防护:
(4)图中能保护
 不被腐蚀的是装置
不被腐蚀的是装置(5)另一装置中
 极的电极反应式为
极的电极反应式为
您最近半年使用:0次
名校
4 . 电化学的发展对人类文明的进步起到了推动作用。
(Ⅰ)用如图装置研究化学能转化为电能的过程。

(1)连接前,该装置中主要的能量转化形式为:______ 能→______ 能。连接后,Cu表面电极反应式为_______ 。
(2)连接前后,装置中现象的差异有______ 。(任写两条)
(Ⅱ)用如图装置实现“Zn表面镀Cu”。
(3)需要将溶液改为______ (填写溶质化学式),此时,Cu发生的电极反应式为______ 。
(4)该装置连续工作ts后,测得Zn增重mg,这段时间内平均电流强度为ⅠA,则阿伏加德罗常数的数值可以表示为______ 。(已知:一个电子的电量为qC,电量(Q)与电流强度(Ⅰ)的关系为:Q=I•t)
(Ⅲ)研究金属的腐蚀过程及防腐蚀对人们的日常生活有重大意义。
(5)如图1中的铁棒为纯铁,则其腐蚀过程属于_______ 腐蚀。
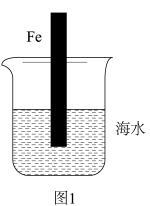
(6)如图1中的铁棒(含碳量为10.8%)越靠近烧杯底部发生电化学腐蚀就越______ (选填“轻微”、“严重”)。该实验说明_______ 因素会影响铁的腐蚀速率。腐蚀时正极的电极反应式为______ 。(已知:海水pH约为8.1)
(7)用图2研究铁的腐蚀过程。预测恒温条件下反应一段时间后,U形管内液面的变化情况。

(已知:起始时两管内液面相平,实验过程中铁丝始终不接触溶液,选填“左高右低”、“左低右高”或“几乎不变”)
该组实验目的:研究______ 、______ 等因素对铁的腐蚀过程产生影响。
(8)用图3所示装置研究铁的防腐蚀过程:

①K1、K2、K3只关闭一个,则铁腐蚀的速度最快的是只闭合______ (填“K1”、“K2”或“K3”下同)。
②为减缓铁的腐蚀,应只闭合______ ,该防护法称为______ 。
③只闭合K3,石墨电极附近的pH将______ (填“变大”、“变小”或“不变”)。
(9)图4为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。
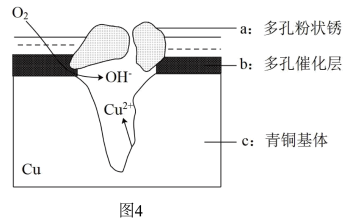
①腐蚀过程中,负极是______ (填“a”、“b”或“c”)。
②环境中的 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl。青铜器发生电化腐蚀并最终生成Cu2(OH)3Cl的总离子方程式为
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl。青铜器发生电化腐蚀并最终生成Cu2(OH)3Cl的总离子方程式为______ 。
(Ⅰ)用如图装置研究化学能转化为电能的过程。

(1)连接前,该装置中主要的能量转化形式为:
(2)连接前后,装置中现象的差异有
(Ⅱ)用如图装置实现“Zn表面镀Cu”。
(3)需要将溶液改为
(4)该装置连续工作ts后,测得Zn增重mg,这段时间内平均电流强度为ⅠA,则阿伏加德罗常数的数值可以表示为
(Ⅲ)研究金属的腐蚀过程及防腐蚀对人们的日常生活有重大意义。
(5)如图1中的铁棒为纯铁,则其腐蚀过程属于

(6)如图1中的铁棒(含碳量为10.8%)越靠近烧杯底部发生电化学腐蚀就越
(7)用图2研究铁的腐蚀过程。预测恒温条件下反应一段时间后,U形管内液面的变化情况。

(已知:起始时两管内液面相平,实验过程中铁丝始终不接触溶液,选填“左高右低”、“左低右高”或“几乎不变”)
| 溶液X | 浓硫酸 | 浓盐酸 | 稀硫酸 |
| 液面情况 |
(8)用图3所示装置研究铁的防腐蚀过程:

①K1、K2、K3只关闭一个,则铁腐蚀的速度最快的是只闭合
②为减缓铁的腐蚀,应只闭合
③只闭合K3,石墨电极附近的pH将
(9)图4为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。

①腐蚀过程中,负极是
②环境中的
 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl。青铜器发生电化腐蚀并最终生成Cu2(OH)3Cl的总离子方程式为
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl。青铜器发生电化腐蚀并最终生成Cu2(OH)3Cl的总离子方程式为
您最近半年使用:0次
解题方法
5 . 请回答:
(1)写出乙烯的结构式:_______ ;写出CaC2的电子式:______ 。
(2)取50mL过氧化氢水溶液,在少量I-存在下分解:2H2O2=2H2O+O2↑。
在一定温度下,测得O2的放出量(已折合成标况)如表:
20~40min,消耗H2O2的平均速率为______ mol•L-1•min-1。
(3)如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
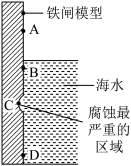
①该电化腐蚀称为______ (填“吸氧腐蚀”或“析氢腐蚀”)。
②图中A、B、C、D四个区域,生成铁锈最多的是______ (填字母)。
(1)写出乙烯的结构式:
(2)取50mL过氧化氢水溶液,在少量I-存在下分解:2H2O2=2H2O+O2↑。
在一定温度下,测得O2的放出量(已折合成标况)如表:
| t/min | 0 | 20 | 40 |
| V(O2)/L | 0 | 0.448 | 0.672 |
(3)如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。

①该电化腐蚀称为
②图中A、B、C、D四个区域,生成铁锈最多的是
您最近半年使用:0次
6 . 下列化学用语表述不正确的是
A.用硫化钠除去废水中的汞离子: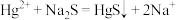 |
B. 与 与 混合产生黄色沉淀: 混合产生黄色沉淀: |
C.钢铁发生吸氧腐蚀,正极反应: |
D.Na和Cl形成离子键的过程: |
您最近半年使用:0次
名校
解题方法
7 . 下列实验装置或操作设计正确,且能达到实验目的的是
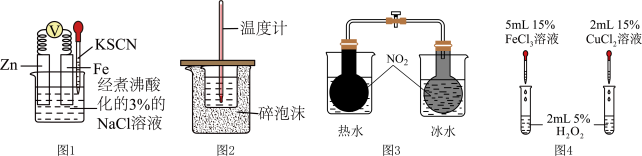

| A.如图1实验,验证牺牲阳极的阴极保护法 |
| B.如图2实验,进行中和热的测定 |
| C.如图3实验,探究温度对平衡移动的影响 |
| D.如图4实验,比较Fe3+和Cu2+对H2O2分解的催化效果 |
您最近半年使用:0次
名校
解题方法
8 . 下列说法中正确的是
A.一定温度下,向体积不变的反应体系 中通入CO2,平衡后 中通入CO2,平衡后 增大 增大 |
| B.常温常压下能发生自发反应的两种物质,在常温常压下一定不能大量共存 |
C.金属的化学腐蚀实质是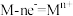 ,电子直接转移给氧化剂 ,电子直接转移给氧化剂 |
D.在KMnO4酸性溶液做电解质的原电池中, 一定向负极移动 一定向负极移动 |
您最近半年使用:0次
名校
解题方法
9 . 2022年6月17日,首艘自主设计建造的弹射型航空母舰命名为“中国人民解放军海军福建舰”,舷号“18”,为我国第三艘航空母舰。下列有关说法正确的是
| A.为屏蔽自身不被定位,舰体采用高强度耐腐蚀低磁钢,其熔点高于纯铁 |
| B.雷达系统相控阵化所用碳化硅属于新型有机物 |
| C.在舰体表面刷漆涂上中国海军灰白色涂装,目的之一是防止金属腐蚀 |
| D.航空母舰的燃料都是重油,为混合物,主要成分属于酯类 |
您最近半年使用:0次
2023-05-30更新
|
153次组卷
|
8卷引用:上海市静安区2022-2023学年高三下学期二模测试化学试题
上海市静安区2022-2023学年高三下学期二模测试化学试题(已下线)专题01 化学与STSE(已下线)上海市静安区2022-2023学年高三下学期二模变式题(选择题1-5)湖北省十堰市郧阳中学、恩施高中、随州二中、襄阳三中2022-2023学年高二下学期5月联考化学试题福建省德化一中、永安一中、漳平一中三校协作2023届高三下学期5月适应性考试化学试题辽宁省铁岭市昌图县第一高级中学2022-2023学年高一下学期期末考试化学试题(已下线)选择题6-102023届宁夏回族自治区石嘴山市第三中学高三下学期第三次模拟考试理综试题
名校
10 . 完成下列问题
(1)CO、 均为大气污染物,利用催化剂处理污染气体成为煤化工的热点问题,在一定温度时,有催化剂存在的条件下,密闭容器中CO与
均为大气污染物,利用催化剂处理污染气体成为煤化工的热点问题,在一定温度时,有催化剂存在的条件下,密闭容器中CO与 转化为与
转化为与 、
、 ,其相关反应为:
,其相关反应为: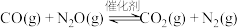

已知:①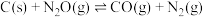
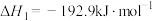
②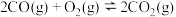
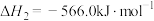
③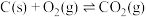
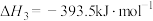
则反应
___________ 。
(2)为了减少对环境的污染,煤在燃烧前要进行脱硫处理。电解脱硫的基本原理如图所示。
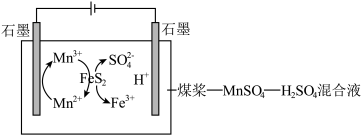
①阳极的电极反应式为___________ 。
② 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是___________ 。
③电解过程中,当有 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大___________ mol(不考虑溶液中水的体积变化)。
(3)常温下,用压强传感器探究铁在 的醋酸溶液中发生腐蚀的装置及得到图像如图所示。
的醋酸溶液中发生腐蚀的装置及得到图像如图所示。

①根据图像a所示,请简单描述锥形瓶中气体压强的变化:___________ 。
②分析两个图像中曲线变化,描述铁粉腐蚀的过程正确的是___________ (填字母)。
A.前100秒,发生的是析氢腐蚀,100秒之后才发生吸氧腐蚀
B.整个过程中,吸氧腐蚀一直都在进行
C.物质的氧化性往往与其浓度有关,100秒之后溶液中 氧化性小于氧气
氧化性小于氧气
(1)CO、
 均为大气污染物,利用催化剂处理污染气体成为煤化工的热点问题,在一定温度时,有催化剂存在的条件下,密闭容器中CO与
均为大气污染物,利用催化剂处理污染气体成为煤化工的热点问题,在一定温度时,有催化剂存在的条件下,密闭容器中CO与 转化为与
转化为与 、
、 ,其相关反应为:
,其相关反应为: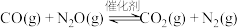

已知:①
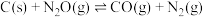
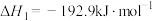
②
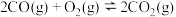
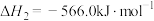
③
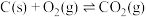
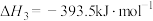
则反应

(2)为了减少对环境的污染,煤在燃烧前要进行脱硫处理。电解脱硫的基本原理如图所示。

①阳极的电极反应式为
②
 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是③电解过程中,当有
 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大(3)常温下,用压强传感器探究铁在
 的醋酸溶液中发生腐蚀的装置及得到图像如图所示。
的醋酸溶液中发生腐蚀的装置及得到图像如图所示。
①根据图像a所示,请简单描述锥形瓶中气体压强的变化:
②分析两个图像中曲线变化,描述铁粉腐蚀的过程正确的是
A.前100秒,发生的是析氢腐蚀,100秒之后才发生吸氧腐蚀
B.整个过程中,吸氧腐蚀一直都在进行
C.物质的氧化性往往与其浓度有关,100秒之后溶液中
 氧化性小于氧气
氧化性小于氧气
您最近半年使用:0次
2023-05-30更新
|
49次组卷
|
2卷引用:山东省滨州市部分学校2022-2023学年高一下学期5月联考化学试题



