名校
1 . 利用电化学原理可以处理地下水中的硝酸根离子并回收氨氮,其模拟装置如图所示。下列叙述错误的是

| A.通电一段时间后,阳极区溶液的pH升高 |
| B.离子交换膜为阳离子交换膜 |
C.a极的电极反应式为 |
D.每转移2mol  ,生成标准状况下11.2L气体 ,生成标准状况下11.2L气体 |
您最近一年使用:0次
解题方法
2 .  是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。
【 的制备】
的制备】
(1)用下图装置制备 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是___________ 。 ;
;___________ 。
【 的性质探究】
的性质探究】
资料:i. 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成
,在近中性条件下被还原成 。
。
ii.单质硫可溶于 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。
某小组研究 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。
(3)①甲同学取实验Ⅰ中少量溶液进行实验,检测有 ,得出
,得出 被氧化成
被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是___________ 。
②同学讨论后,设计了如下实验,证实该条件下 的确可以将
的确可以将 氧化成
氧化成 。
。___________ 。
b.连通后电流计指针偏转,一段时间后,___________ (填操作和现象)。
(4)实验I的现象与资料i不相符,其原因是新生成的产物( )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是___________ 。
(5)实验II的现象与资料也不完全相符,丙同学猜想原因与(4)中所述原因相似,其原因是___________ ,请设计验证此猜想的实验方案___________ 。
(6)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与___________ 等因素有关。
 是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。【
 的制备】
的制备】(1)用下图装置制备
 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是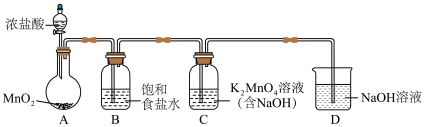
 ;
;【
 的性质探究】
的性质探究】资料:i.
 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成
,在近中性条件下被还原成 。
。ii.单质硫可溶于
 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。某小组研究
 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。| 实验序号 | 实验过程 | 实验现象 |
| Ⅰ |
| 紫色变浅( ),生成棕褐色沉淀( ),生成棕褐色沉淀( ) ) |
| Ⅱ |
| 溶液呈淡黄色( ),生成浅粉色沉淀(MnS) ),生成浅粉色沉淀(MnS) |
(3)①甲同学取实验Ⅰ中少量溶液进行实验,检测有
 ,得出
,得出 被氧化成
被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是②同学讨论后,设计了如下实验,证实该条件下
 的确可以将
的确可以将 氧化成
氧化成 。
。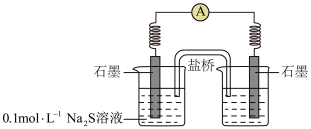
b.连通后电流计指针偏转,一段时间后,
(4)实验I的现象与资料i不相符,其原因是新生成的产物(
 )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是(5)实验II的现象与资料也不完全相符,丙同学猜想原因与(4)中所述原因相似,其原因是
(6)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与
您最近一年使用:0次
3 . 下列装置及操作能达到实验目的的是
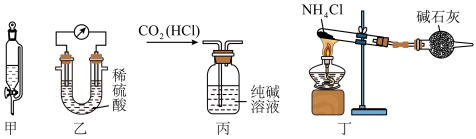
| A.利用甲装置用四氯化碳萃取碘水中的碘 | B.利用乙装置验证金属镁、铝的活泼性 |
C.利用丙装置除去 气体中混有的少量HCl 气体中混有的少量HCl | D.利用丁装置制备少量 |
您最近一年使用:0次
名校
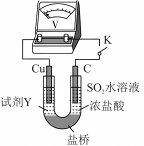
4 . 某小组探究 在盐酸中分别与铜单质和铜离子的反应,从改变氧化产物、还原产物浓度的角度分析物质氧化性和还原性的变化规律。
在盐酸中分别与铜单质和铜离子的反应,从改变氧化产物、还原产物浓度的角度分析物质氧化性和还原性的变化规律。
I.探究 在盐酸中与
在盐酸中与 的反应
的反应
用如下装置(夹持、加热仪器略)制备 ,将
,将 通入
通入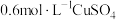 溶液。通
溶液。通 一段时间,C中无明显现象;打开活塞b,加入一定体积浓盐酸后,持续通入
一段时间,C中无明显现象;打开活塞b,加入一定体积浓盐酸后,持续通入 ,C中溶液变棕黄色。
,C中溶液变棕黄色。___________ ,为除去 中含有的少量硫酸酸雾,并观察气流速率,B中盛放试剂X是
中含有的少量硫酸酸雾,并观察气流速率,B中盛放试剂X是___________ 。装置C中盛放浓盐酸的仪器名称为___________ 。
(2)资料:CuCl难溶于水,在浓盐酸溶液中存在平衡:CuCl(白色)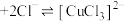 。补充实验证实棕黄色溶液中含
。补充实验证实棕黄色溶液中含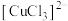 ,实验方案为
,实验方案为___________ 。
(3)一个氧化还原反应包括氧化反应和还原反应两个过程(即两个半反应), 与
与 溶液反应生成
溶液反应生成 和
和 的过程可分为下面两个半反应:
的过程可分为下面两个半反应:
氧化反应:___________ ;还原反应: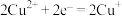 。
。
根据还原反应式,分析加入浓盐酸前后实验现象有差异的可能原因___________ 。
(4)综上分析, 在盐酸中与
在盐酸中与 反应生成
反应生成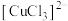 的离子方程式为
的离子方程式为___________ 。
实验结论:综合上述实验可知,还原反应中,降低生成物浓度,氧化剂的氧化性增强。
II.探究 在盐酸中与Cu单质的反应
在盐酸中与Cu单质的反应
将装置C中 溶液替换成Cu片和
溶液替换成Cu片和 溶液,重复上述操作。未加浓盐酸之前,无明显现象。加浓盐酸之后,溶液变为棕黄色,并有黑色固体生成。
溶液,重复上述操作。未加浓盐酸之前,无明显现象。加浓盐酸之后,溶液变为棕黄色,并有黑色固体生成。
(5)经检验黑色固体是 ,
, 在盐酸中与Cu单质反应的离子方程式为
在盐酸中与Cu单质反应的离子方程式为___________ 。
(6)为了进一步探究影响铜单质还原性的因素,进行了如下实验:
实验ii中,Cu片附近溶液变棕黄色。a是___________ ,b是___________ 。
综合上述实验可知:氧化反应中,降低生成物浓度,还原剂的还原性增强。
 在盐酸中分别与铜单质和铜离子的反应,从改变氧化产物、还原产物浓度的角度分析物质氧化性和还原性的变化规律。
在盐酸中分别与铜单质和铜离子的反应,从改变氧化产物、还原产物浓度的角度分析物质氧化性和还原性的变化规律。I.探究
 在盐酸中与
在盐酸中与 的反应
的反应用如下装置(夹持、加热仪器略)制备
 ,将
,将 通入
通入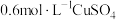 溶液。通
溶液。通 一段时间,C中无明显现象;打开活塞b,加入一定体积浓盐酸后,持续通入
一段时间,C中无明显现象;打开活塞b,加入一定体积浓盐酸后,持续通入 ,C中溶液变棕黄色。
,C中溶液变棕黄色。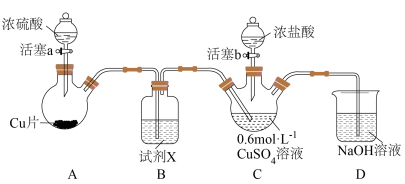
 中含有的少量硫酸酸雾,并观察气流速率,B中盛放试剂X是
中含有的少量硫酸酸雾,并观察气流速率,B中盛放试剂X是(2)资料:CuCl难溶于水,在浓盐酸溶液中存在平衡:CuCl(白色)
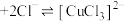 。补充实验证实棕黄色溶液中含
。补充实验证实棕黄色溶液中含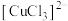 ,实验方案为
,实验方案为(3)一个氧化还原反应包括氧化反应和还原反应两个过程(即两个半反应),
 与
与 溶液反应生成
溶液反应生成 和
和 的过程可分为下面两个半反应:
的过程可分为下面两个半反应:氧化反应:
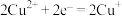 。
。根据还原反应式,分析加入浓盐酸前后实验现象有差异的可能原因
(4)综上分析,
 在盐酸中与
在盐酸中与 反应生成
反应生成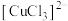 的离子方程式为
的离子方程式为实验结论:综合上述实验可知,还原反应中,降低生成物浓度,氧化剂的氧化性增强。
II.探究
 在盐酸中与Cu单质的反应
在盐酸中与Cu单质的反应将装置C中
 溶液替换成Cu片和
溶液替换成Cu片和 溶液,重复上述操作。未加浓盐酸之前,无明显现象。加浓盐酸之后,溶液变为棕黄色,并有黑色固体生成。
溶液,重复上述操作。未加浓盐酸之前,无明显现象。加浓盐酸之后,溶液变为棕黄色,并有黑色固体生成。(5)经检验黑色固体是
 ,
, 在盐酸中与Cu单质反应的离子方程式为
在盐酸中与Cu单质反应的离子方程式为(6)为了进一步探究影响铜单质还原性的因素,进行了如下实验:
| 序号 | 实验装置图 | 试剂Y | 电压表 |
| i |
|  溶液 溶液 | 指针几乎不偏转 |
| ii | a | 指针明显偏转 | |
| iii | a+b | 指针偏转幅度更大 |
综合上述实验可知:氧化反应中,降低生成物浓度,还原剂的还原性增强。
您最近一年使用:0次
名校
解题方法
5 . 科学家称他们正在研制的铝电池未来有望取代锂电池。银铝电池具有能量密度高的优点,电池装置如图;电池放电时的反应为: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是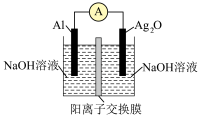
A. 电极发生还原反应 电极发生还原反应 |
| B.阳离子交换膜允许阳离子和电子通过 |
C.当导线中通过 电子时,负极区溶液质量减小 电子时,负极区溶液质量减小 |
D.正极电极反应式为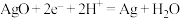 |
您最近一年使用:0次
2024-04-23更新
|
876次组卷
|
3卷引用:题型8 反应热 电化学的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)
(已下线)题型8 反应热 电化学的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)天津市河北区2024届高三总复习质量检测(一)化学试题2024届陕西省西安中学高三下学期第七次模拟考试理综试题-高中化学
名校
6 . 下列对实验的叙述正确的是

| A.图甲,盐桥(装有含KCI饱和溶液的琼脂)中的Cl-移向CuSO4溶液 |
| B.图乙,可用来探究催化剂对化学反应速率的影响 |
| C.图丙,可用来制取少量CO2气体 |
| D.图丁,可用来验证浓硫酸具有脱水性、强氧化性,SO2具有漂白性、还原性 |
您最近一年使用:0次
2024-04-22更新
|
487次组卷
|
5卷引用:单项选择题6-10
(已下线)单项选择题6-102024届河北省高三下学期部分学校4月质量检测化学试题(已下线)化学(天津卷03)-2024年高考化学押题预测卷2024届河北省衡水董子高级中学 昌黎第一中学高三下学期联考质量检测化学试题湖南省长沙市周南中学2024届高三下学期第三次模拟考试化学试题
名校
7 . 锂离子电池及其迭代产品依然是目前世界上主流的手机电池。科学家近期研发的一种新型的Ca—LiFePO4可充电电池的原理示意图如图,电池反应为: ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是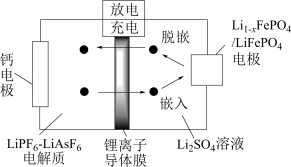
| A.放电时,钙电极为负极,发生还原反应 |
B.充电时, / / 电极的电极反应式为 电极的电极反应式为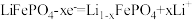 |
| C.锂离子导体膜的作用是允许Li+和水分子通过,同时保证Li+定向移动以形成电流 |
| D.充电时,当转移0.2mol电子时,理论上阴极室中电解质的质量减轻4.0g |
您最近一年使用:0次
2024-04-21更新
|
313次组卷
|
5卷引用:T12-电化学原理
解题方法
8 . 在 浓溶液中及空气存在下,矿砂中的单质银发生吸氧腐蚀生成
浓溶液中及空气存在下,矿砂中的单质银发生吸氧腐蚀生成 ,再加入锌粉生成
,再加入锌粉生成 和纯度较高的单质银,下列说法不正确的是
和纯度较高的单质银,下列说法不正确的是
 浓溶液中及空气存在下,矿砂中的单质银发生吸氧腐蚀生成
浓溶液中及空气存在下,矿砂中的单质银发生吸氧腐蚀生成 ,再加入锌粉生成
,再加入锌粉生成 和纯度较高的单质银,下列说法不正确的是
和纯度较高的单质银,下列说法不正确的是A.提高 浓度有利于单质银的溶解 浓度有利于单质银的溶解 |
B.正极发生的电极反应式为: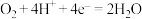 |
C.随着腐蚀的进行,溶液的 增大 增大 |
| D.加入锌粉反应后,溶液中阴离子总浓度降低 |
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
9 . (氮是空气中含量最多的元素,在自然界中的存在十分广泛,实验小组对不同含氮物质做了相关研究。
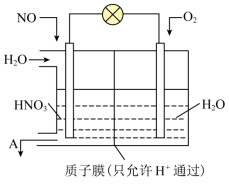
(1)利用电化学原理脱硝可同时获得电能,其工作原理如图所示。则负极发生的电极反应式为___________ ,当外电路中有2mol电子通过时,理论上通过质子膜的微粒的物质的量为___________ 。
(1)利用电化学原理脱硝可同时获得电能,其工作原理如图所示。则负极发生的电极反应式为
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
10 . 利用 催化加氢制二甲醚,可以实现
催化加氢制二甲醚,可以实现 的再利用,涉及以下主要反应:
的再利用,涉及以下主要反应:
I.

Ⅱ.

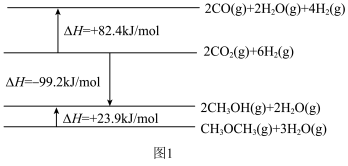
相关物质及能量变化的示意图如图1所示。
(1)如图所示是绿色电源“二甲醚( )燃料电池”的工作原理示意图(a、b均为多孔性
)燃料电池”的工作原理示意图(a、b均为多孔性 电极)。负极是
电极)。负极是___________ (填写“a”或“b”),该电极的电极反应式是___________ ,若有 氢离子通过质子交换膜,则b电极在标准状况下吸收
氢离子通过质子交换膜,则b电极在标准状况下吸收___________  氧气。
氧气。
 催化加氢制二甲醚,可以实现
催化加氢制二甲醚,可以实现 的再利用,涉及以下主要反应:
的再利用,涉及以下主要反应:I.


Ⅱ.


相关物质及能量变化的示意图如图1所示。
(1)如图所示是绿色电源“二甲醚(
 )燃料电池”的工作原理示意图(a、b均为多孔性
)燃料电池”的工作原理示意图(a、b均为多孔性 电极)。负极是
电极)。负极是 氢离子通过质子交换膜,则b电极在标准状况下吸收
氢离子通过质子交换膜,则b电极在标准状况下吸收 氧气。
氧气。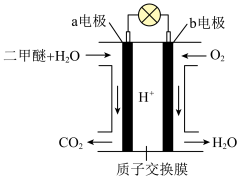
您最近一年使用:0次