名校
解题方法
1 . 下列根据实验操作及现象进行的分析和推断中,不正确 的是
操作 |
|
现象 | 一段时间后:①中,铁钉裸露在外的附近区域变红;②中…… |
A. 的琼脂水溶液为离子导体 的琼脂水溶液为离子导体 |
B.①中变红是因为发生反应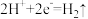 ,促进了水的电离 ,促进了水的电离 |
| C.②中可观察到铁钉裸露在外的附近区域变蓝,铜丝附近区域变红 |
D.①和②中发生的氧化反应均可表示为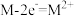 (M代表锌或铁) (M代表锌或铁) |
您最近一年使用:0次
解题方法
2 . Ⅰ、 的资源化可以推动经济高质量发展和生态环境质量的持续改善,回答下列问题:
的资源化可以推动经济高质量发展和生态环境质量的持续改善,回答下列问题:
(1) 和
和 都是主要的温室气体。发生催化重整反应
都是主要的温室气体。发生催化重整反应

已知 时,相关物质的燃烧热数据如下表:
时,相关物质的燃烧热数据如下表:
反应的
___________ 
(2)将原料按初始组成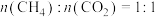 充入密闭容器中,保持体系压强为
充入密闭容器中,保持体系压强为 发生反应。达到平衡时,
发生反应。达到平衡时, 体积分数与温度的关系如图所示:
体积分数与温度的关系如图所示: 的体积分数,则
的体积分数,则___________ 点对应的平衡常数最小,理由是___________
(3)在恒温恒容装置中通入等体积 和
和 ,发生上述反应,起始压强为p,
,发生上述反应,起始压强为p, 的平衡转化率为
的平衡转化率为 。达平衡时,容器内总压为
。达平衡时,容器内总压为___________ 。该反应的平衡常数
___________ (用平衡分压代替平衡浓度计算,分压 总压×物质的量分数,用
总压×物质的量分数,用 、
、 表达,并化为最简式)。
表达,并化为最简式)。
(4)其他条件相同,在不同催化剂(A、B)作用下, 的产率随反应温度的变化如图所示:
的产率随反应温度的变化如图所示: 、
、 表示,则
表示,则
___________  (填“>”“<”或“=”下同)。
(填“>”“<”或“=”下同)。
②y点对应的
___________ z点对应的 。
。
Ⅱ.运用电化学原理可以很好利用 资源。
资源。
(5)火星大气由 的二氧化碳气体组成,火星探测器采用
的二氧化碳气体组成,火星探测器采用 电池供电,其反应机理如下图:
电池供电,其反应机理如下图: 电极反应式:
电极反应式:___________ 。
 的资源化可以推动经济高质量发展和生态环境质量的持续改善,回答下列问题:
的资源化可以推动经济高质量发展和生态环境质量的持续改善,回答下列问题:(1)
 和
和 都是主要的温室气体。发生催化重整反应
都是主要的温室气体。发生催化重整反应

已知
 时,相关物质的燃烧热数据如下表:
时,相关物质的燃烧热数据如下表:| 物质 |  |  |  |
燃烧热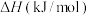 |  |  |  |


(2)将原料按初始组成
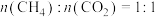 充入密闭容器中,保持体系压强为
充入密闭容器中,保持体系压强为 发生反应。达到平衡时,
发生反应。达到平衡时, 体积分数与温度的关系如图所示:
体积分数与温度的关系如图所示: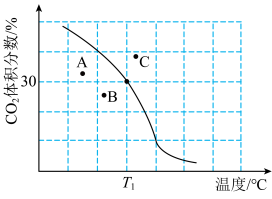
 的体积分数,则
的体积分数,则(3)在恒温恒容装置中通入等体积
 和
和 ,发生上述反应,起始压强为p,
,发生上述反应,起始压强为p, 的平衡转化率为
的平衡转化率为 。达平衡时,容器内总压为
。达平衡时,容器内总压为
 总压×物质的量分数,用
总压×物质的量分数,用 、
、 表达,并化为最简式)。
表达,并化为最简式)。(4)其他条件相同,在不同催化剂(A、B)作用下,
 的产率随反应温度的变化如图所示:
的产率随反应温度的变化如图所示: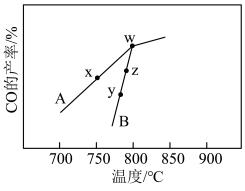
 、
、 表示,则
表示,则
 (填“>”“<”或“=”下同)。
(填“>”“<”或“=”下同)。②y点对应的

 。
。Ⅱ.运用电化学原理可以很好利用
 资源。
资源。(5)火星大气由
 的二氧化碳气体组成,火星探测器采用
的二氧化碳气体组成,火星探测器采用 电池供电,其反应机理如下图:
电池供电,其反应机理如下图:
 电极反应式:
电极反应式:
您最近一年使用:0次
2024-02-25更新
|
863次组卷
|
6卷引用:大题预测卷02 (新高考通用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
(已下线)大题预测卷02 (新高考通用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)(已下线)大题04 化学反应原理综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)江西省上饶市2024届高三下学期第一次高考模拟考试化学试题(已下线)专题10 化学反应原理综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)专题10 化学反应原理综合题-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)江西省宜春市上高县2023-2024学年高三下学期5月月考化学试题
名校
3 . 科学家设计了一种具有石墨正极的高容量可充电 电池,原理如图所示。氯化铝(
电池,原理如图所示。氯化铝( )溶解在亚硫酰氯(
)溶解在亚硫酰氯( )中,以氟化物(LiFSI)为溶剂。下列叙述正确的是
)中,以氟化物(LiFSI)为溶剂。下列叙述正确的是
 电池,原理如图所示。氯化铝(
电池,原理如图所示。氯化铝( )溶解在亚硫酰氯(
)溶解在亚硫酰氯( )中,以氟化物(LiFSI)为溶剂。下列叙述正确的是
)中,以氟化物(LiFSI)为溶剂。下列叙述正确的是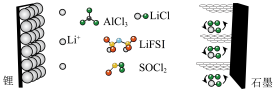
A.放电时,电解质溶液可以是 水溶液 水溶液 |
B.放电时,石墨极的电极反应式为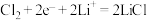 |
| C.充电时,石墨极与电源负极连接 |
D.充电时,转移 个电子时锂电极理论上消耗14g锂 个电子时锂电极理论上消耗14g锂 |
您最近一年使用:0次
2024-02-25更新
|
192次组卷
|
6卷引用:T12-电化学基础
名校
4 . 一种新型短路膜电池分离CO2装置如下图所示。下列说法中正确的是
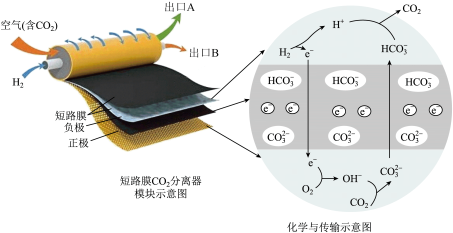

| A.负极反应为:H2−2e−+2OH−=H2O |
| B.正极反应消耗22.4LO2,理论上需要转移4mol电子 |
| C.短路膜和常见的离子交换膜不同,它既能传递离子,还可以传递电子 |
| D.该装置用于空气中CO2的捕获,CO2最终由出口A流出 |
您最近一年使用:0次
名校
5 . 合成氨有着重要的实际价值,一直是科学家们研究的课题。
(1)基于物理性质写出氨的一种用途:_______ 。
(2)工业合成氨常用工艺条件:Fe作催化剂,控制温度773K,压强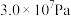 ,原料中
,原料中 和
和 物质的量之比为1:2.8
物质的量之比为1:2.8
①调控反应。从动力学角度和热力学角度选择反应条件,其中选择“两难”(两个分析角度影响不一致)的反应条件是_______ ,该反应条件最终选择上述给出工艺条件的主要原因是_______ 。
②催化机理。Fe作催化剂,反应是在Fe表面活性位点进行的,历程经历了吸附 和
和 、发生反应、
、发生反应、 脱附三个阶段。其中,
脱附三个阶段。其中, 的吸附分解反应活化能高,是决速步骤。研究发现,
的吸附分解反应活化能高,是决速步骤。研究发现, 浓度越大,反应速率越小,原因是
浓度越大,反应速率越小,原因是_______ 。写出一种降低氨浓度的最实用可行方法:_______ 。
(3)在密闭容器中模拟合成氨反应: 。将
。将 的混合气投入恒压反应容器进行反应,在压强
的混合气投入恒压反应容器进行反应,在压强 、
、 、
、 下,分别测得
下,分别测得 的平衡体积分数
的平衡体积分数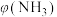 随温度变化如下图所示。
随温度变化如下图所示。 、
、 、
、 中,最大的是
中,最大的是_______ ,A点 的转化率为
的转化率为_______ 。
②已知温度为 时,
时, 。维持温度为
。维持温度为 ,若要使
,若要使 的平衡转化率达到30%,则恒压反应容器的总压强至少为
的平衡转化率达到30%,则恒压反应容器的总压强至少为_______ MPa.(保留小数点后2位)
(4)电化学合成氨。可利用氮还原反应在更温和的条件下将 和
和 转化为
转化为 。研究人员发现,选用三己基十四烷基磷离子作为电解质的阳离子,与叶立德能够很好的完成电化学循环。该电化学装置的工作原理如下图所示。
。研究人员发现,选用三己基十四烷基磷离子作为电解质的阳离子,与叶立德能够很好的完成电化学循环。该电化学装置的工作原理如下图所示。
注:Rn为烃基。_______ 。
②写出图中左边电极区由 生成
生成 的总反应式:
的总反应式:_______ 。
(1)基于物理性质写出氨的一种用途:
(2)工业合成氨常用工艺条件:Fe作催化剂,控制温度773K,压强
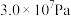 ,原料中
,原料中 和
和 物质的量之比为1:2.8
物质的量之比为1:2.8①调控反应。从动力学角度和热力学角度选择反应条件,其中选择“两难”(两个分析角度影响不一致)的反应条件是
②催化机理。Fe作催化剂,反应是在Fe表面活性位点进行的,历程经历了吸附
 和
和 、发生反应、
、发生反应、 脱附三个阶段。其中,
脱附三个阶段。其中, 的吸附分解反应活化能高,是决速步骤。研究发现,
的吸附分解反应活化能高,是决速步骤。研究发现, 浓度越大,反应速率越小,原因是
浓度越大,反应速率越小,原因是(3)在密闭容器中模拟合成氨反应:
 。将
。将 的混合气投入恒压反应容器进行反应,在压强
的混合气投入恒压反应容器进行反应,在压强 、
、 、
、 下,分别测得
下,分别测得 的平衡体积分数
的平衡体积分数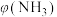 随温度变化如下图所示。
随温度变化如下图所示。
 、
、 、
、 中,最大的是
中,最大的是 的转化率为
的转化率为②已知温度为
 时,
时, 。维持温度为
。维持温度为 ,若要使
,若要使 的平衡转化率达到30%,则恒压反应容器的总压强至少为
的平衡转化率达到30%,则恒压反应容器的总压强至少为(4)电化学合成氨。可利用氮还原反应在更温和的条件下将
 和
和 转化为
转化为 。研究人员发现,选用三己基十四烷基磷离子作为电解质的阳离子,与叶立德能够很好的完成电化学循环。该电化学装置的工作原理如下图所示。
。研究人员发现,选用三己基十四烷基磷离子作为电解质的阳离子,与叶立德能够很好的完成电化学循环。该电化学装置的工作原理如下图所示。注:Rn为烃基。

②写出图中左边电极区由
 生成
生成 的总反应式:
的总反应式:
您最近一年使用:0次
名校
6 . 铜基催化剂催化甲醇水蒸气重整制氢是液体燃料制氢的重要方向,主要包含甲醇水蒸气重整反应、甲醇分解反应和水气变换反应,具体反应方程式如下:
Ⅰ.

Ⅱ.

Ⅲ.

回答下列问题:
(1)则
___________  。
。
(2)有利于提高甲醇平衡转化率的是___________ (填标号)。
A.增加 的用量 B.恒温恒压条件下通入Ar
的用量 B.恒温恒压条件下通入Ar
C.升高温度 D.选择更高效的催化剂 E.及时分离出
(3)一定条件下,向压强为 的恒压密闭容器中通入
的恒压密闭容器中通入 、
、 物质的量比为
物质的量比为 的混合气体,发生上述反应,达到平衡时,容器中
的混合气体,发生上述反应,达到平衡时,容器中 、
、 ,此时
,此时 的产率为
的产率为___________ ,反应Ⅱ的以分压表示的化学平衡常数 为
为___________ (用含 的代数式表示)。
的代数式表示)。
(4)液相空速表示进料速度的快慢。不同温度下,平衡时甲醇转化率和CO浓度随甲醇液相空速的变化如图所示。随温度升高,CO浓度变化的原因是___________ ,制氢产物可以用于车载燃料电池,CO含量太高会对电池产生巨大危害。甲醇水蒸气重整制氢的适宜条件是___________ ℃,___________  。
。 自由迁移的固体电解质氢氧燃料电池中,
自由迁移的固体电解质氢氧燃料电池中, 放电的电极反应式为
放电的电极反应式为___________ 。
Ⅰ.


Ⅱ.


Ⅲ.


回答下列问题:
(1)则

 。
。(2)有利于提高甲醇平衡转化率的是
A.增加
 的用量 B.恒温恒压条件下通入Ar
的用量 B.恒温恒压条件下通入ArC.升高温度 D.选择更高效的催化剂 E.及时分离出

(3)一定条件下,向压强为
 的恒压密闭容器中通入
的恒压密闭容器中通入 、
、 物质的量比为
物质的量比为 的混合气体,发生上述反应,达到平衡时,容器中
的混合气体,发生上述反应,达到平衡时,容器中 、
、 ,此时
,此时 的产率为
的产率为 为
为 的代数式表示)。
的代数式表示)。(4)液相空速表示进料速度的快慢。不同温度下,平衡时甲醇转化率和CO浓度随甲醇液相空速的变化如图所示。随温度升高,CO浓度变化的原因是
 。
。
 自由迁移的固体电解质氢氧燃料电池中,
自由迁移的固体电解质氢氧燃料电池中, 放电的电极反应式为
放电的电极反应式为
您最近一年使用:0次
2024-02-22更新
|
199次组卷
|
3卷引用:T17-原理综合题
名校
解题方法
7 . 化学与生活密切相关,下列生活常识不能用对应的化学知识解释的是
选项 | 生活常识 | 化学知识 |
A | 铜、铝电线连接起来使用易出现断电现象 | 易形成原电池加速金属的锈蚀 |
B | 银质首饰变黑后可放在铝盆盛放的盐水中可恢复光亮 | 反应为: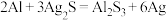 |
C | 护肤品中添加丙三醇 | 丙三醇有吸水性 |
D | 用热的纯碱溶液清洗油污 | 油脂在热的纯碱溶液中更易发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 .  电池电催化还原
电池电催化还原 生成
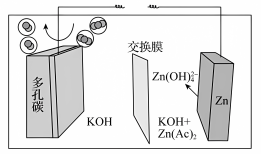
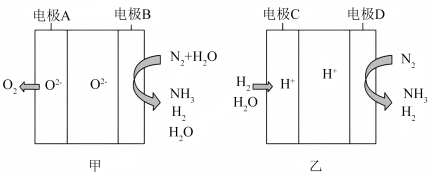
生成 作电源,用电解法制氨气的可能装置如图所示。下列有关说法错误的是
作电源,用电解法制氨气的可能装置如图所示。下列有关说法错误的是
 电池电催化还原
电池电催化还原 生成
生成 作电源,用电解法制氨气的可能装置如图所示。下列有关说法错误的是
作电源,用电解法制氨气的可能装置如图所示。下列有关说法错误的是

A. 电极的电极反应式为 电极的电极反应式为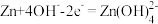 ,制氨时, ,制氨时, 电极连接电极B和电极D 电极连接电极B和电极D |
B.电极B的副产物 可循环至电极C,未反应完的 可循环至电极C,未反应完的 可循环使用,提高原料利用率 可循环使用,提高原料利用率 |
C.多孔碳的电极反应式为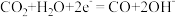 |
D.利用甲装置制氨时,消耗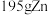 时,可生成标准状况下 时,可生成标准状况下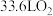 和 和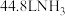 |
您最近一年使用:0次
解题方法
9 . 一种新型可充电钠离子电池,放电时原理如图所示。
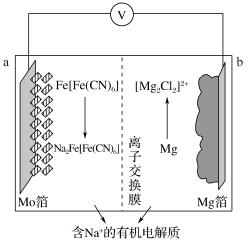
下列说法正确的是

下列说法正确的是
| A.充电时,b电极与外接电源正极相连 |
| B.离子交换膜为阴离子交换膜 |
C.充电时,a极反应式为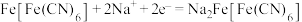 |
D.放电时,当外电路转移 电子,b极区电解质溶液质量减少 电子,b极区电解质溶液质量减少 |
您最近一年使用:0次
解题方法
10 .  转化利用对化解全球环境生态危机助力全球“碳达峰、碳中和”目标的实现具有重要意义。化学工作者致力于将
转化利用对化解全球环境生态危机助力全球“碳达峰、碳中和”目标的实现具有重要意义。化学工作者致力于将 转化为各种化工原料。
转化为各种化工原料。
Ⅰ.早在二十世纪初,工业上以 和
和 为原料在一定温度和压强下合成尿素。反应分两步:①
为原料在一定温度和压强下合成尿素。反应分两步:① 和
和 生成
生成 ;②
;② 分解生成尿素。
分解生成尿素。
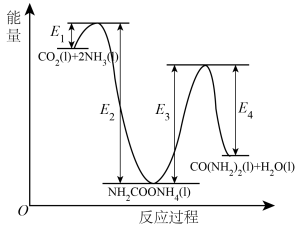
(1)活化能:反应①反应___________ ②(填“>”、“<”或“=”);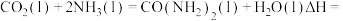
___________ (用含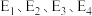 的式子表示)。
的式子表示)。
II.我国科学家研究 电池,取得了重大科研成果。
电池,取得了重大科研成果。 电池中,反应产物为
电池中,反应产物为 ;和单质碳,正极
;和单质碳,正极 电还原后与锂离子结合形成
电还原后与锂离子结合形成 按以下4个步骤进行:
按以下4个步骤进行:
① ;
;
②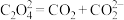 ;
;
③___________;
④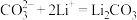
(2)写出步骤③中 与
与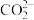 反应的离子方程式
反应的离子方程式___________ 。
III.利用 和重整技术可获得合成气(主要成分为
和重整技术可获得合成气(主要成分为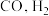 ),重整过程中反应的热化学方程式如下:
),重整过程中反应的热化学方程式如下:
反应i: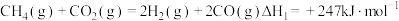
反应ii: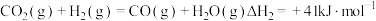
不同配比随温度变化对出口合成气中 的影响如下图所示
的影响如下图所示
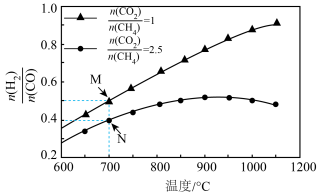
(3)对于反应 ,试比较
,试比较 点和
点和 点
点 的转化率:
的转化率:
___________  (填“>”、“<”或“=”下同);平衡常数
(填“>”、“<”或“=”下同);平衡常数
___________  ,当
,当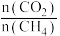 一定,有利于提高
一定,有利于提高 平衡转化率的反应条件是
平衡转化率的反应条件是___________ (填序号)。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
(4)当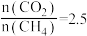 ,温度高于
,温度高于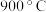 ,
, 减小的原因可能是
减小的原因可能是___________ 。
 转化利用对化解全球环境生态危机助力全球“碳达峰、碳中和”目标的实现具有重要意义。化学工作者致力于将
转化利用对化解全球环境生态危机助力全球“碳达峰、碳中和”目标的实现具有重要意义。化学工作者致力于将 转化为各种化工原料。
转化为各种化工原料。Ⅰ.早在二十世纪初,工业上以
 和
和 为原料在一定温度和压强下合成尿素。反应分两步:①
为原料在一定温度和压强下合成尿素。反应分两步:① 和
和 生成
生成 ;②
;② 分解生成尿素。
分解生成尿素。
(1)活化能:反应①反应
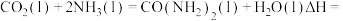
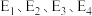 的式子表示)。
的式子表示)。II.我国科学家研究
 电池,取得了重大科研成果。
电池,取得了重大科研成果。 电池中,反应产物为
电池中,反应产物为 ;和单质碳,正极
;和单质碳,正极 电还原后与锂离子结合形成
电还原后与锂离子结合形成 按以下4个步骤进行:
按以下4个步骤进行:①
 ;
;②
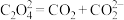 ;
;③___________;
④
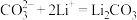
(2)写出步骤③中
 与
与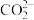 反应的离子方程式
反应的离子方程式III.利用
 和重整技术可获得合成气(主要成分为
和重整技术可获得合成气(主要成分为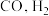 ),重整过程中反应的热化学方程式如下:
),重整过程中反应的热化学方程式如下:反应i:
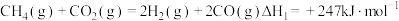
反应ii:
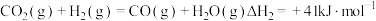
不同配比随温度变化对出口合成气中
 的影响如下图所示
的影响如下图所示
(3)对于反应
 ,试比较
,试比较 点和
点和 点
点 的转化率:
的转化率:
 (填“>”、“<”或“=”下同);平衡常数
(填“>”、“<”或“=”下同);平衡常数
 ,当
,当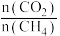 一定,有利于提高
一定,有利于提高 平衡转化率的反应条件是
平衡转化率的反应条件是A.高温高压 B.高温低压 C.低温高压 D.低温低压
(4)当
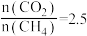 ,温度高于
,温度高于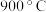 ,
, 减小的原因可能是
减小的原因可能是
您最近一年使用:0次