1 . 原电池是将化学能转化为电能的装置,某兴趣小组利用数据采集器和传感器等仪器对原电池进行实验探究。
I.能量变化探究
将上表的现象和结论补充完整
(1)_____________
(2)__________ 、__________
II.原电池电压影响因素的测定
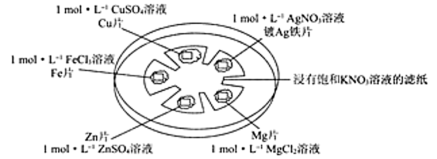
如图所示,在培养皿中进行微型实验,用浸有饱和KNO3溶液的滤纸充当盐桥,在滤纸间隔位置放置金属片,并滴三滴相应溶液,用电压传感器的两个探头分别与不同的金属表面接触形成闭合回路,测定电压。
(3)准确配制一定物质的量浓度的溶液时,操作X应在__________ (填字母)之间。
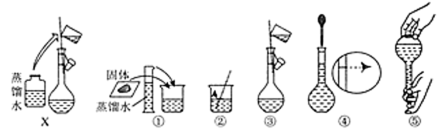
A.②③ B.③④ C.④⑤
(4)以上五种金属的活动性由活泼到不活泼的顺序为_________________ 。
(5)实验条件下,连接不同金属片时所得数据见下表,表中Y极代表__________ (填“正”或“负”)极,预测表中Ag和Zn相连接时,测得电压的数值a可能的范围为____________ ;Fe和Mg相连接时,Z极的电极反应式为__________ ,Y极的电极反应式为____________ 。
I.能量变化探究
| 实验操作 | 数据及图象 | 现象与结论 |
| 将60mL1mol/LCuSO4溶液置于100mL烧杯中,向其中加入1g镁粉 | 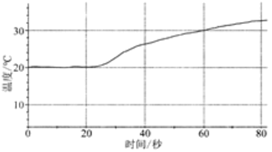 | (1)反应过程中,化学能直接转化为 能; |
| 将60mL1mol/LCuSO4溶液置于100mL烧杯中,平行插入铜片和镁片,与电流传感器形成闭合回路 | 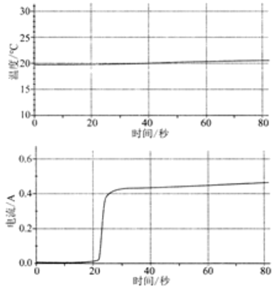 | (2)体系温度变化很小,原因是 ;反应过程中,镁片和铜片的质量变化分别为: ; |
(1)
(2)
II.原电池电压影响因素的测定
如图所示,在培养皿中进行微型实验,用浸有饱和KNO3溶液的滤纸充当盐桥,在滤纸间隔位置放置金属片,并滴三滴相应溶液,用电压传感器的两个探头分别与不同的金属表面接触形成闭合回路,测定电压。

(3)准确配制一定物质的量浓度的溶液时,操作X应在

A.②③ B.③④ C.④⑤
(4)以上五种金属的活动性由活泼到不活泼的顺序为
(5)实验条件下,连接不同金属片时所得数据见下表,表中Y极代表
| Y极 | Z极 | 测得电压/V |
| Ag | Fe | 1.009 |
| Ag | Zn | a |
| Ag | Mg | 2.114 |
| Fe | Zn | 0.473 |
| Fe | Mg | 1.111 |
| Zn | Mg | 0.636 |
您最近一年使用:0次
名校
解题方法
2 . “水”电池是一种利用淡水与海水之间含盐量差别进行发电的电池,其总反应为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,如图以“水”电池为电源电解酸性FeCl2溶液,X电极附近溶液先变黄,下列有关分析不正确的是( )
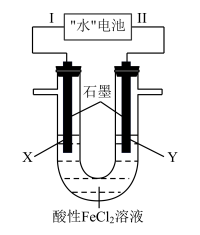

| A.该装置只涉及两种能量之间的转化 |
| B.在线路中安装电压调节装置,可通过现象判断Fe2+和Cl-的还原性强弱 |
| C.“水”电池内Na+不断向正极移动 |
| D.Ⅱ为负极,其电极反应式为Ag+Cl--e-=AgCl |
您最近一年使用:0次
2020-07-08更新
|
75次组卷
|
3卷引用:河南省许昌市第三高级中学2019-2020学年高一下学期期末考试化学试题
解题方法
3 . 浓差电池是一种利用电解质溶液浓度差产生电势差而形成的电池。理论上当电解质溶液的浓度相等时停止放电。图1为浓差电池,图2为电渗析法制备磷酸二氢钠,用浓差电池作电源完成电渗析法制备磷酸二氢钠。下列说法错误的是
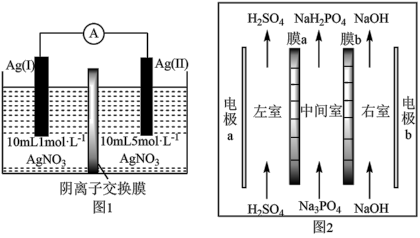

| A.电极a应与Ag(II)相连 |
| B.电渗析装置中膜a为阳离子交换膜 |
| C.电池从开始到停止放电,理论上可制备2.4gNaH2PO4 |
| D.电渗析过程中左、右室中H2SO4和NaOH的浓度均增大 |
您最近一年使用:0次
4 . 电化学原理在电池制造、能量转换、物质合成等方面应用广泛。请回答下列问题。
(1)若用图甲装置,依据反应 设计原电池,则X电极材料应为
设计原电池,则X电极材料应为___________ (填化学式),石墨电极的电极反应为___________ 。将石墨电极换成Fe电极后,电池总反应变为___________ 。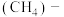 空气燃料电池,其工作原理如图乙所示,a、b均为惰性电极。a为
空气燃料电池,其工作原理如图乙所示,a、b均为惰性电极。a为___________ 极,正极的电极反应为___________ 。当通入4.48L(标准状况)甲烷气体时,测得电路中转移1.1mol电子,则甲烷的利用率为___________ 。 还原CO电化学法制备甲醇
还原CO电化学法制备甲醇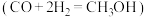 的工作原理如图丙所示,通入
的工作原理如图丙所示,通入 的一端是电池的
的一端是电池的___________ (填“正”或“负”)极,电池工作过程中 通过质子膜向
通过质子膜向___________ (填“左”或“右”)移动,通入CO的一端发生的电极反应为___________ 。
(1)若用图甲装置,依据反应
 设计原电池,则X电极材料应为
设计原电池,则X电极材料应为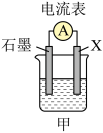
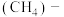 空气燃料电池,其工作原理如图乙所示,a、b均为惰性电极。a为
空气燃料电池,其工作原理如图乙所示,a、b均为惰性电极。a为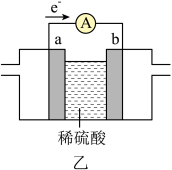
 还原CO电化学法制备甲醇
还原CO电化学法制备甲醇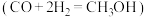 的工作原理如图丙所示,通入
的工作原理如图丙所示,通入 的一端是电池的
的一端是电池的 通过质子膜向
通过质子膜向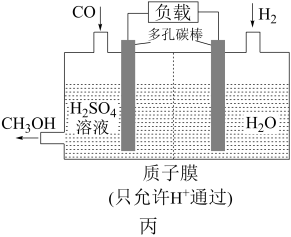
您最近一年使用:0次
名校
解题方法
5 . 根据题中提供的信息,请回答下列问题:
(1)学习原电池原理后,小江同学根据反应 设计了一个原电池并得到老师的肯定,则小江同学选用的负极材料是
设计了一个原电池并得到老师的肯定,则小江同学选用的负极材料是______ ,正极材料可能是______ (填一种)。
(2)小河同学设计了如图所示的原电池,利用不同的电解质溶液进行实验。______ 。
②当以NaOH溶液作为电解质溶液时,电流表指针也发生了偏转,若负极失去1mol电子,理论上负极的质量变化为______ g。
(3)燃料电池是一种高效化学电池,以稀硫酸为电解质溶液的氢氧燃料电池的工作原理如图所示,a和b都是Pt电极(惰性电极)。______ 。
②该电池工作时,电解质溶液中 的移动方向是
的移动方向是______ 。(填“a向b”或“b向a”,下同),外电路中电子的流动方向是______ 。
③若将a极通入的气体换为 ,同时将电解质溶液换为NaOH溶液,则a极的电极反应式为
,同时将电解质溶液换为NaOH溶液,则a极的电极反应式为______ 。当a极有1mol 发生反应时,理论上b极参加反应的氧气在标准状况下的体积为
发生反应时,理论上b极参加反应的氧气在标准状况下的体积为______ L。
(4)小海同学在做氢气的制备实验时,用锌粒和稀硫酸为原料,结果发现反应速率较慢。其他同学给出以下建议,其中能加快制备 的反应速率的有______(填字母)。
的反应速率的有______(填字母)。
(1)学习原电池原理后,小江同学根据反应
 设计了一个原电池并得到老师的肯定,则小江同学选用的负极材料是
设计了一个原电池并得到老师的肯定,则小江同学选用的负极材料是(2)小河同学设计了如图所示的原电池,利用不同的电解质溶液进行实验。

②当以NaOH溶液作为电解质溶液时,电流表指针也发生了偏转,若负极失去1mol电子,理论上负极的质量变化为
(3)燃料电池是一种高效化学电池,以稀硫酸为电解质溶液的氢氧燃料电池的工作原理如图所示,a和b都是Pt电极(惰性电极)。

②该电池工作时,电解质溶液中
 的移动方向是
的移动方向是③若将a极通入的气体换为
 ,同时将电解质溶液换为NaOH溶液,则a极的电极反应式为
,同时将电解质溶液换为NaOH溶液,则a极的电极反应式为 发生反应时,理论上b极参加反应的氧气在标准状况下的体积为
发生反应时,理论上b极参加反应的氧气在标准状况下的体积为(4)小海同学在做氢气的制备实验时,用锌粒和稀硫酸为原料,结果发现反应速率较慢。其他同学给出以下建议,其中能加快制备
 的反应速率的有______(填字母)。
的反应速率的有______(填字母)。| A.将稀硫酸换成质量分数为98%的浓硫酸 | B.向反应液中滴入几滴硫酸铜溶液 |
| C.改换合适的装置并适当加热 | D.将锌粒换成质量相等的锌粉 |
您最近一年使用:0次
名校
解题方法
6 . 下图是原电池的装置图。请回答下列问题:___________ ,反应进行一段时间后,溶液C的酸性___________ (填“增强”“减弱”或“基本不变”)。
(2)若将反应 设计成如上图所示的原电池装置,则A极(负极)材料为
设计成如上图所示的原电池装置,则A极(负极)材料为___________ ,B极的电极反应式为___________ 。
(3)若A极为Zn,B极为Cu,溶液C为 溶液,则Cu极发生
溶液,则Cu极发生___________ 反应,电极反应式为___________ 。反应过程中,溶液中的
___________ (填“变大”“变小”或“不变”)。
(4)CO与 反应还可制备甲醇(
反应还可制备甲醇( ),
), 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构如图所示。
组合形成的质子交换膜燃料电池的结构如图所示。 ,若线路中转移2mol电子,则该
,若线路中转移2mol电子,则该 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为___________ L。
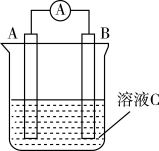
(2)若将反应
 设计成如上图所示的原电池装置,则A极(负极)材料为
设计成如上图所示的原电池装置,则A极(负极)材料为(3)若A极为Zn,B极为Cu,溶液C为
 溶液,则Cu极发生
溶液,则Cu极发生
(4)CO与
 反应还可制备甲醇(
反应还可制备甲醇( ),
), 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构如图所示。
组合形成的质子交换膜燃料电池的结构如图所示。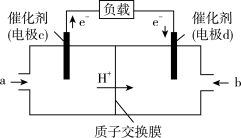
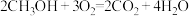 ,若线路中转移2mol电子,则该
,若线路中转移2mol电子,则该 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
2024-07-03更新
|
209次组卷
|
3卷引用:河南省安阳市林州市第一中学2023-2024学年高一下学期6月月考化学试题
7 . 用废料Ce2O3制备Ce(SO4)2的工作原理示意图如图1所示[电源为可充电锂离子电池,该电池放电时的反应为 ]。下列说法错误的是
]。下列说法错误的是
 ]。下列说法错误的是
]。下列说法错误的是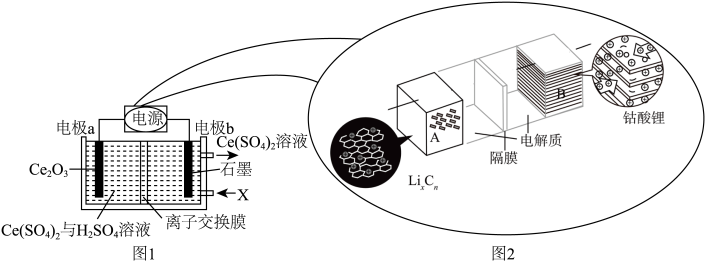
| A.图1中的离子交换膜为阳离子交换膜 |
B.图2装置充电时,电极B的电极反应式为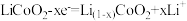 |
| C.图1装置工作一段时间后,电极a区溶液的质量减小 |
| D.锂离子电池电动汽车可有效减少光化学烟雾污染 |
您最近一年使用:0次
2023-05-18更新
|
304次组卷
|
3卷引用:2023届河南省郑州市重点校高三下学期5月联考理科综合试题
名校
解题方法
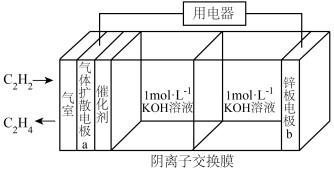
8 . 乙炔制乙烯是煤化工路线的重要途径之一,如图是利用电化学装置制备 的工作原理示意图,下列说法正确的是
的工作原理示意图,下列说法正确的是
 的工作原理示意图,下列说法正确的是
的工作原理示意图,下列说法正确的是
| A.电极电势:a极<b极 |
| B.电子移动方向:电极b→用电器→电极a→KOH溶液→电极b |
C.电极a上的电极反应式为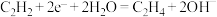 |
| D.放电一段时间后,正极室溶液pH不会发生变化 |
您最近一年使用:0次
2024-01-31更新
|
109次组卷
|
2卷引用:河南省南阳市桐柏县实验高中2024届高三上学期阶段检测化学试题(12月)
名校
解题方法
9 . 图1为浓差电池,图2为电渗析法制备磷酸二氢钠,用浓差电池为电源完成电渗析法制备磷酸二氢钠。下列说法错误 的是


| A.电极a应与Ag(II)相连 |
| B.电渗析装置中膜b为阳离子交换膜 |
| C.电渗析过程中左、右室中H2SO4和NaOH的浓度均增大 |
| D.电池从开始到停止放电,理论上可制备2.4gNaH2PO4 |
您最近一年使用:0次
2023-11-23更新
|
329次组卷
|
2卷引用:河南省郑州市实验中学2023-2024学年高三上学期期中考试化学试题
名校
解题方法
10 . “双碳(即碳达峰与碳中和)”要求加快降低碳排放步伐,引导绿色技术创新,提高产业和经济的全球竞争力。电催化 制备高附加值的化学品既能满足“双碳”要求,又能实现
制备高附加值的化学品既能满足“双碳”要求,又能实现 的资源化利用。回答下列问题:
的资源化利用。回答下列问题:
(1)杭州亚运会采用零碳甲醇点燃亚运主火炬,零碳甲醇是指采用 为原料制备的甲醇。利用质子交换膜进行废水处理,产生的
为原料制备的甲醇。利用质子交换膜进行废水处理,产生的 进行电催化合成甲醇的工作原理如图1、图2所示,这实现了废水处理的无废碳过程。
进行电催化合成甲醇的工作原理如图1、图2所示,这实现了废水处理的无废碳过程。 的移动方向是
的移动方向是___________ (填“向左移动”或“向右移动”)。
②图2中,生成甲醇的电极为___________ (填“阳极”或“阴极”),其电极反应式为___________ 。
③若图2中的“直流电源”用图1装置代替,则电极A连接___________ (填“C”或“D”)极。
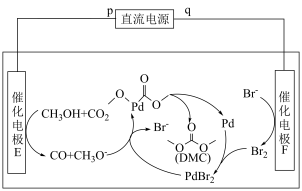
(2)科技工作者设计了如图所示的电化学装置,该装置在室温下即能以 和甲醇为原料合成碳酸二甲酯(
和甲醇为原料合成碳酸二甲酯( )。
)。___________ (填“p”或“q”)。
②电解总过程的化学方程式为___________ 。
③该电化学反应机理中,充当氧化剂的物质有___________ (填一种,填化学式或结构简式)。
(3)通过阴离子交换膜及合适的催化剂,先使 电催化转化为乙烯,乙烯再与氯碱电化学体系结合制备高附加值的环氧乙烷的工作原理如图所示:
电催化转化为乙烯,乙烯再与氯碱电化学体系结合制备高附加值的环氧乙烷的工作原理如图所示:___________ (填“阴”或“阳”)极产物。
②电极H上生成67.2L(标准状况) 时,理论上氯碱电化学体系可得到
时,理论上氯碱电化学体系可得到___________ g环氧乙烷。
 制备高附加值的化学品既能满足“双碳”要求,又能实现
制备高附加值的化学品既能满足“双碳”要求,又能实现 的资源化利用。回答下列问题:
的资源化利用。回答下列问题:(1)杭州亚运会采用零碳甲醇点燃亚运主火炬,零碳甲醇是指采用
 为原料制备的甲醇。利用质子交换膜进行废水处理,产生的
为原料制备的甲醇。利用质子交换膜进行废水处理,产生的 进行电催化合成甲醇的工作原理如图1、图2所示,这实现了废水处理的无废碳过程。
进行电催化合成甲醇的工作原理如图1、图2所示,这实现了废水处理的无废碳过程。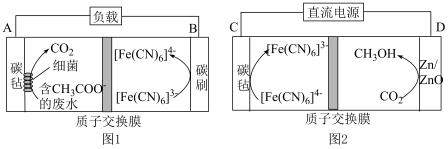
 的移动方向是
的移动方向是②图2中,生成甲醇的电极为
③若图2中的“直流电源”用图1装置代替,则电极A连接
(2)科技工作者设计了如图所示的电化学装置,该装置在室温下即能以
 和甲醇为原料合成碳酸二甲酯(
和甲醇为原料合成碳酸二甲酯( )。
)。
②电解总过程的化学方程式为
③该电化学反应机理中,充当氧化剂的物质有
(3)通过阴离子交换膜及合适的催化剂,先使
 电催化转化为乙烯,乙烯再与氯碱电化学体系结合制备高附加值的环氧乙烷的工作原理如图所示:
电催化转化为乙烯,乙烯再与氯碱电化学体系结合制备高附加值的环氧乙烷的工作原理如图所示: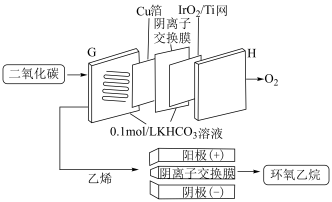
②电极H上生成67.2L(标准状况)
 时,理论上氯碱电化学体系可得到
时,理论上氯碱电化学体系可得到
您最近一年使用:0次
2024-01-07更新
|
108次组卷
|
2卷引用:河南省驻马店市遂平县第一高级中学2023-2024学年高二上学期期中考试化学试卷



